какие капли для ушей лучше при боли
Сейчас вы узнаете про капли в уши.
На самом деле вопрос совершенно не для практического применения, а для теоретических знаний.Потому что до тех пор, пока врач не посмотрит ухо, определить целесообразность тех или иных капель не получится.
Итак, для чего нужны капли?
Противогрибковые капли, например, Кандибиотик, можно применять при грибковом отите, и больше ни при каком другом. Их тоже нельзя использовать при наличии перфорации в ухе.
Капли антибактериальные, например, Нормакс и Отофа, нужны, напротив, в той ситуации, когда есть перфорация в барабанной перепонке. Во всех остальных случаях капать их бесполезно, ведь капли не проникают через барабанную перепонку и просто не смогут добраться до очага инфекции при среднем отите с отсутствием перфорации.
Капли, в составе которых есть антибиотик и стероиды, например, Софрадекс, нужны при некоторых видах наружных отитов, вызванных бактериями. Их тоже нельзя при нарушении целостности барабанной перепонки и бесполезно капать при среднем отите.
Потому не покупаем капли без назначения врача и по совету аптекаря. Аптекарь не смотрит уши!
Антимикробная терапия острого среднего отита в педиатрической практике
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонно
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонность к рецидивированию [1]. Острый средний отит — это остро развившееся воспаление полостей среднего уха (барабанной полости, сосцевидного отростка, слуховой трубы), проявляющееся одним или несколькими симптомами (боль в ухе, повышение температуры тела, выделения из уха, у маленьких детей понос, тошнота).
Довольно часто ОСО являются так называемым бактериальным осложнением острых респираторных вирусных инфекций (ОРВИ). При этом может отсутствовать болевой синдром и снижение слуха, а симптомы наблюдающейся общей интоксикации нередко расцениваются врачом как клиническое проявление основного заболевания. Острое воспаление среднего уха выявляется у 19,7% детей, больных ОРВИ (обследовано 3567 пациентов) [8].
При типичном остром среднем отите воспалительный процесс в полостях среднего уха не выходит за рамки выстилающей их слизистой оболочки. Отражающая этот процесс патолого-анатомическая картина достаточно типична и характеризуется отеком, капиллярной гиперемией и лейкоцитарной инфильтрацией слизистой оболочки, особенно ее субэпителиального слоя. А в эпителиальном, покровном слое отмечается некоторое увеличение числа продуцирующих слизь бокаловидных клеток, поэтому в экссудате, образующемся при остром воспалении среднего уха, всегда есть та или иная примесь слизи. В совокупности указанные изменения приводят к выраженной гиперплазии слизистой оболочки среднего уха, особенно в барабанной полости, где ее толщина способна увеличиваться в 30 раз и более. Происходит накопление экссудата, который поначалу может быть серозным, затем серомукозным и далее — мукозно-гнойным и гнойным. Слуховые косточки, которые оказываются погруженными в утолщенную слизистую оболочку барабанной полости и скопившийся в ней экссудат, в значительной степени теряют свою подвижность, что вместе с тугоподвижностью воспалительно-измененной барабанной перепонки обусловливает существенное ухудшение слуховой функции. При увеличении количества экссудата в среднем ухе, давление, оказываемое им на барабанную перепонку, повышается, и это приводит к нарушению микроциркуляции, трофическим и некротическим изменениям барабанной перепонки, следствием которых является образование ее перфорации и появление трансмеатальной отореи.
В детском возрасте острый средний отит имеет ряд особенностей и возникает чаще, чем у взрослых, прежде всего из-за анатомо-физиологических особенностей: более широкая, короткая и горизонтально расположенная слуховая труба, наличие аденоидных вегетаций, более быстрое нарушение функции мерцательного эпителия при воспалении. Несформированный иммунитет может приводить к реактивному и часто осложненному течению детских инфекционных заболеваний. В младенческом возрасте увеличивается риск развития внутричерепных осложнений из-за незаращения каменисто-чешуйчатой щели височной кости, через которую инфекция может проникать в полость черепа, поражая мозговые структуры. Следует отметить, что диагностика отита у детей раннего возраста осложнена из-за ограниченного вербального контакта и затруднений при отоскопии [3].
Основными профилактическими мероприятиями острого среднего отита являются предупреждение и своевременное лечение простудных заболеваний, обучение правильному туалету носа (поочередно правой и левой половин).
Лечение острого среднего отита должно быть комплексным и включать адекватные терапевтические мероприятия, которые можно разделить на местные и общие. Для уменьшения отека в области носоглоточного устья слуховой трубы и восстановления ее вентиляционной и дренирующей функций используют назальные сосудосуживающие капли (Нафтизин, Тизин и т. п.), которые необходимо закапывать в нос при запрокинутой назад голове. Обязательным является лечение сопутствующего ринита или риносинусита. Препараты, вводимые в слуховой проход, должны быть комбинированными и обладать противовоспалительным действием, противобактериальным и противогрибковым, антиаллергическим и обезболивающим эффектами. В ряде случаев, в частности при тяжелом течении отита, необходимо прибегать к антибиотикам системного действия.
При выборе лекарственного средства следует учитывать эпидемиологическую ситуацию, особенности клинической картины, возраст пациента, наличие сопутствующих заболеваний, сведения о ранее проводимой антибактериальной терапии и переносимости лекарственных препаратов.
Антибиотик, применяемый для терапии отитов, должен обладать не только высокой эффективностью, широким спектром антибактериального действия и хорошим проникновением в очаг воспаления, но и низкой токсичностью, удобством приема.
Микробиологическая диагностика средних отитов основана на бактериологическом исследовании содержимого среднего уха, полученного при парацентезе или тимпанопункции. Исследования, проведенные в США, Европе и Японии, показали, что самым распространенным возбудителем острого среднего отита является Streptococcus pneumoniae, на втором месте — нетипируемые штаммы Haemophilus influenzae, на третьем месте — Moraxella catarrhalis. Менее чем 10% ОСО вызываются другими микроорганизмами, например стрептококками группы А и Staphylococcus aureus. Этиология ОСО не может быть установлена по клинической картине, однако следует отметить, что пневмококковый ОСО обычно протекает тяжелее, чаще приводит к развитию осложнений и не склонен к саморазрешению. Из 90 серотипов S. pneumoniae только несколько вызывают ОСО. Наиболее распространены из них серотипы 19, 23, 6, 14, 3 и 18. Использование вакцины, содержащей капсульные полисахариды 7–8 наиболее часто встречаемых серотипов S. pneumoniae, способно предотвратить более чем 80% ОСО пневмококковой этиологии. Большинство штаммов H. influenzae, вызывающих ОСО, являются нетипируемыми. По современным данным, около 20–50% H. influenzae, выделяемых при ОСО, продуцируют бета-лактамазы [9].
Результаты многочисленных многолетних исследований сходны с результатами зарубежных авторов и показывают, что наиболее вероятными возбудителями острого среднего отита в России являются St. aureus, St. epidermidis, S. pneumoniae и H. influenzae, несколько реже Streptococcus pyogenes, S. viridans, M. catarrhalis анаэробы.
В лечении ОСО многочисленными исследованиями достоверно доказана эффективность цефалоспоринов как антибактериальных препаратов широкого спектра действия, в частности Cупракса (цефиксима) — представителя 3-го поколения цефалоспоринов. Супракс обладает высоким уровнем антибактериальной активности, улучшенными фармакокинетическими свойствами, расширенным, по сравнению с цефалоспоринами предыдущих поколений, спектром действия. Бактерицидное действие препарата обусловлено ингибированием пептидогликана — основного структурного компонента клеточной стенки бактерий. Биодоступность препарата (около 50%) позволяет исключить парентеральный путь введения. Максимальная концентрация в крови достигается уже через 4 ч. Супракс хорошо проникает в место инфицирования. Период полувыведения зависит от дозы и составляет 3–4 ч, а в тканях препарат задерживается на более длительный срок, что позволяет принимать его 1 раз в сутки. Препарат хорошо переносится больными. Эти свойства Супракса позволяют считать целесообразным его применение в детской оториноларингологической практике.
Было проведено обследование и лечение 30 детей с ОСО 7–12 лет (девочек — 14, мальчиков — 16). Всем пациентам проводили лечение Супраксом из расчета 5 мг/кг 2 раза в сутки в течение 6 дней.
В качестве контрольных использовали результаты, полученные при наблюдении за аналогичной в количественном и возрастном отношении группой детей, получавших амоксициллина клавуланат (2 дозировочные ложечки по 5 мл (312 мг) 3 раза в сутки парентерально в течение 6 дней).
Обследование включало: ЛОР-осмотр, аудиометрию, тимпанометрию, компьютерную томографию околоносовых пазух, рентгенографию височных костей по Шюллеру и Майеру, клинический анализ крови, бактериологическое исследование отделяемого из слухового прохода при наличии перфорации барабанной перепонки.
По данным микробиологического исследования отделяемого, полученного из слухового прохода у 18 детей обеих групп, среди возбудителей преобладал S. pneumoniae — у 11 детей, реже встречались St. aureus — у 4, H. influenzae — у 2 пациентов, в одном случае роста микрофлоры получено не было.
В результате лечения зафиксировано уменьшение клинических проявлений и положительная динамика объективных критериев заболевания у детей из основной и контрольной групп (тимпанометрия, аудиометрия, клинический анализ крови). Эффективность Супракса была сравнимой с амоксициллина клавуланатом, считающимся препаратом выбора при ОСО [6].
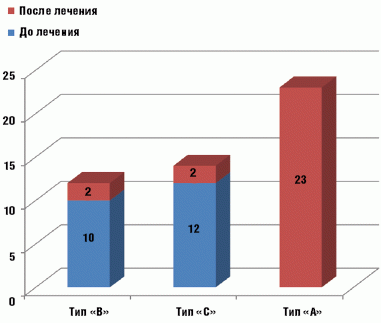
В основной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 10, «С» у 12 детей, 8 детям тимпанометрия не проводилась из-за наличия перфорации. По окончании курса лечения Супраксом кондуктивная тугоухость сохранялась у 7 пациентов, тимпанограмма «А» зафиксирована у 23, «В» у 2 и «С» у 2 пациентов, 3 детям тимпанометрия не проводилась из-за наличия перфорации (рис. 1).
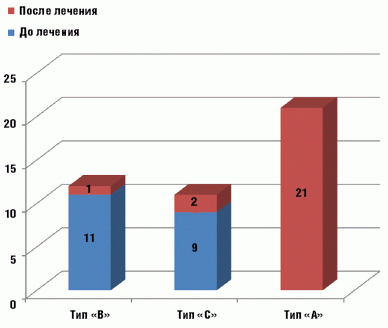
В контрольной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 11, «С» — у 9 больных, 10 детям тимпанометрия не проводилась из-за наличия перфорации. По завершении 6-дневного курса терапии амоксициллина клавуланатом кондуктивная тугоухость сохранялась у 9 пациентов, тимпанограмма типа «А» зафиксирована у 21, «В» — у 1, «С» — у 2 детей, 6 пациентам тимпанометрия не проводилась из-за наличия перфорации (рис. 2).
Нежелательных эффектов, требующих отмены препаратов, ни в одной из групп зафиксировано не было.
Таким образом, подтверждена высокая эффективность и безопасность препарата Супракс при остром среднем отите у детей. Супракс может быть рекомендован для широкого применения в детской оториноларингологической практике.
Литература
О. В. Зайцева, кандидат медицинских наук
ФГУ НКЦ оториноларингологии ФМБА России, Москва
Медикаментозная терапия наружного и среднего отита
Опубликовано в журнале:
Вестник оториноларингологии, 1, 2012
Д.м.н. С.В. Оковитый, к.б.н. Д.Ю. Ивкин, к.м.н. С.В. Малыгин
Кафедра фармакологии (зав — д.м.н. С.В. Оковитый) Санкт-Петербургской государственной химико-фармацевтической академии
Medicamental therapy of otitis externa and otitis media
S.V. Okovity, D.YU. Ivkin, S.V. Malygin
Sankt-Peterburg State Chemico-Pharmaceutical Academy Цель работы — анализ существующих медикаментозных средств для лечения наружного и среднего отита. Рациональное применение представленных фармакологических средств позволяет добиться быстрой элиминации разнообразных этиологических факторов, уменьшения воспаления и повышения качества жизни больного. Одним из способов решения этой задачи является использование при наружном и среднем отитах комбинированных топических препаратов, содержащих комбинацию антибактериального, антимикотического, противовоспалительного и обезболивающего компонентов. В РФ этот принцип реализован в комбинированном четырехкомпонентном препарате кандибиотик, содержащем в своем составе хлорамфеникол, клотримазол, беклометазон и лидокаин. Наряду с высокой клинической эффективностью, обусловленной этиотропной и патогенетической направленностью его действия, препарат отличается большой безопасностью, так как его компоненты не обладают ототоксичностью при местном применении.
Ключевые слова: отит наружный, отит средний, медикаментозная терапия, Кандибиотик.
The objective of the present work was to analyse the available pharmaceutical products used for treatment of otitis media. The rational application of these medications makes it possible to eliminate rapidly a variety of etiological factors, reduce the severity of inflammation, and improve the quality of life of the patients. One of the approaches to the achievement of these goals for the patients with otitis externa and otitis media consists of the use of combined preparations containing antibacterial, antimycotic, anti-inflammatory and analgetic components. Candibiotic is a four-components drug composed of chloramphenicol, clotrimazol, beclomethasone and lidocaine. The advantages of Candibiotic include high therapeutic efficacy due to its ethiotropic and pathogenetic activity and safety as its components do not have ototoxicity in the case of local application).
Key words: otitis externa, otitis media, medicamental therapy, Candibiotic.
Причинами наружного отита могут являться высокая влажность, попадание в ухо воды, загрязненной бактериями, высокая температура окружающей среды, механическое удаление ушной серы, являющейся защитным барьером на пути развития инфекции, попадание инородных объектов; использование слуховых аппаратов, травма кожи наружного слухового прохода, экзема, псориаз, себорейный дерматит [3].
При лечении острого наружного отита нередко бывает достаточным применение местных лекарственных препаратов, при этом нет необходимости в проведении системной антибактериальной терапии. Системные антибиотики и антимикотики необходимы только в случае, если пациент иммуннокомпроментирован или воспаление распространяется за пределы наружного слухового прохода [4, 5]. Лечение наружного отита начинают с того, что © Коллектив авторов, 2012 слуховой проход очищается механически, при наличии выделений проводят промывание раствором фурацилина 1:5000 или стерильным физиологическим раствором с последующим тщательным высушиванием. Быстрый клинический эффект достигается использованием ушных капель, позволяющих создать высокие местные концентрации действующих веществ без системных побочных эффектов. Комбинация капель, содержащих кортикостероид и антибиотик широкого спектра действия — одно из эффективных средств при наружном отите бактериальной этиологии [6]. Тщательный туалет наружного слухового прохода и применение капель кортикостероида/антибиотика почти всегда позволяют уже через несколько дней ликвидировать отек, инфильтрацию и боль в ухе. При выраженном болевом синдроме дополнительно применяют анальгетики [4].
В случае, если воспаление не проходит после первой обработки или приобретает рецидивирующее течение, необходимо идентифицировать бактериального или грибкового возбудителя.
Учитывая полиэтиологичность заболевания (возможность присутствия бактериально-грибковой флоры), лечение должно включать антимикробное, антимикотическое, противовоспалительное и, при необходимости, противоболевое воздействие, что решается благодаря использованию комбинированных многокомпонентных препаратов (табл. 1).
Таблица 1. Состав ушных капель, применяемых для лечения отита в России
Помимо капель, для лечения наружного отита можно применять и другие лекарственные формы, например, мази и кремы. Так, широким антибактериальным спектром обладают мазь и крем мупироцина. Особенно ценным представляется то, что препарат практически не активен против представителей нормальной микрофлоры кожи. Имеются данные об активности препарата в отношении некоторых грибов [7].
Острый средний отит достаточно широко распространен, особенно часто заболевание наблюдается у детей первых лет жизни. В частности, установлено, что к годовалому возрасту 62,4% детей переносят острый средний отит однократно, а у 17,3% отмечаются три и более эпизода этого заболевания. По данным исследований, проведенных в США, за первые 3 года жизни острый средний отит переносят хотя бы один раз до 90% детей. Перенесенный в детском возрасте средний отит в 25,5% случаев является причиной развития тугоухости у взрослых [8—10]. В подавляющем большинстве случаев любые выделения из слухового прохода, боль в одном или обоих ушах и (или) понижение слуха обусловлены именно средним отитом; это заболевание является одной из наиболее частых патологий в отоларингологии, особенно у детей и чаще всего обусловливает назначение антибиотиков детям [11].
Основными возбудителями острого среднего отита являются S. pneumoniae (49%) и H. influenzae (29%). У детей младше 3 лет гемофильная палочка высевается гораздо чаще. M. catarrhalis обнаруживается, по разным данным, у 6—28%. S. pyogenes и S. aureus обусловливают до 30% случаев развития острого среднего отита. Около 12—35% посевов из барабанной полости оказываются стерильными [12—14].
В основе патогенеза острого среднего отита — дисфункция слуховой трубы и нарушение ее проходимости либо функциональные нарушения, связанные с неэффективностью механизма ее активного открытия. Оба механизма приводят к созданию отрицательного давления в барабанной полости и транссудации жидкости, которая изначально является стерильной, но после попадания бактериальной или иной флоры принимает воспалительный характер, направленный на элиминацию возбудителя, регенерацию поврежденных тканей и восстановление функциональных структур. На первом этапе в очаге воспаления усиливается кровоток, повышается проницаемость стенок капилляров, увеличивается миграция клеток белой крови непосредственно в ткани. Затем запускаются защитные механизмы — выделяются медиаторы воспаления, свободные кислородные радикалы, что в остром периоде оказывает положительный эффект на воспалительный процесс. Однако длительное присутствие в очаге высокоактивных клеток и свободных радикалов приводит к серьезным изменениям тканей за счет преобразования коллагена и переокисления клеточных мембран. В этом случае изначально направленная на стимуляцию иммунитета и процессов репарации воспалительная реакция может перейти в неконтролируемую, образуется так называемый «порочный круг» (инфекция и воспаление усиливают друг друга), что способствует хронизации патологического процесса с развитием осложнений и присоединением суперинфекции [15].
Этиологическими факторами острого среднего отита могут служить также иммунодефицит (в частности, низкий уровень IgA, IgG2), ВИЧ-инфекция, генетическая предрасположенность [16].
С точки зрения фармакотерапевтических подходов к лечению острого наружного и среднего отитов целесообразно рассмотреть отдельные компоненты фармакотерапии.
Антибактериальные препараты. Системная антибактериальная терапия требуется, прежде всего, при эмпирическом лечении острого среднего отита у пациентов с болью в ухе и выраженной температурной реакцией (развитие острого гнойного воспаления). В этом случае, если пациент в течение последнего месяца не принимал антибиотики, то препаратом выбора является амоксициллин (0,5—1,0 г 3 раза в сутки), а антибиотиками резерва ко-амоксициллин (0,625 г 3 раза в сутки или 1,0 г 2 раза в сутки) или азитромицин (0,25 г 1 раз в сутки). Как вариант могут быть использованы перорально цефдинир, цефподоксим, цефпрозил или цефуроксим аксетил. Средний курс лечения — 5 сут [17].
В том случае, если пациент в прошлом месяце получал антибактериальные средства, то лечение следует начать с ко-амоксициллина (0,625 г 3 раза в сутки или 1,0 г 2 раза в сутки), а в качестве антибиотика резерва рассмотреть левофлоксацин (Глево) (по 0,5 г 1 раз в сутки) или моксифлоксацин (0,4 г 1 раз в сутки). Средний курс лечения — 7 сут. У пациентов с наличием факторов риска (сахарный диабет, патология печени, почек, сердечная недостаточность), антибактериальная терапия рекомендуется и при остром катаральном воспалении (препараты выбора — левофлоксацин (Глево) или моксифлоксацин) [17].
Если в течение 3 дней антибактериальной терапии улучшение не наступило, существует вероятность инфицирования S. pneumoniae, резистентным к β-лактамам. В этом случае, если пациент не принимал антибиотики в течение последнего месяца, препаратом выбора является ко-амоксициллин или левофлоксацин. Как вариант перорально назначают цефдинир, цефподоксим, цефпрозил, цефуроксим аксетил или цефтриаксон внутримышечно. В том случае, если в последний месяц пациент принимал антибиотики, препаратами выбора являются цефтриаксон (внутримышечно) или респираторные фторхинолоны (левофлоксацин, моксифлоксацин), обладающие высокой активностью в отношении пенициллинрезистентных пневмококков и имеющие оптимальные показатели фармакокинетики (высокая биодоступность и хорошее проникновение в ткани) [18].
В случае, если боль в ухе и температурная реакция отсутствуют, у взрослых проводится местное лечение (ушные капли) с применением анальгетиков по требованию [19].
Местная антибактериальная терапия показана, прежде всего, при наружном отите и остром катаральном или гнойном среднем отите. Выбор препарата в этом случае будет, безусловно, эмпирическим, с учетом потенциальной антимикробной активности противомикробных компонентов (табл. 2).
Таблица 2. Сравнительная оценка минимальной подавляющей концентрации (мг/мл) некоторых антибактериальных компонентов ушных капель [20]
| Возбудитель | Ципрофлоксацин | Норфлоксацин | Гентамицин | Хлорамфеникол | Неомицин | Полимиксин В |
| S. pneumoniae | 1—4 | 8 | 16 | 2 | 128 | 128 |
| H. influenzae | 0,008—0,05 | 0,125 | 2 | 0,5 | 16 | 1 |
| S. epidermidis | 0,5 | 0,5 | 8 | 8 | 4 | 32 |
| P. aeruginosa | 0,12—1 | 2 | 128 | 128 | 128 | 1 |
| S. pyogenes | 2 | 8 | 8 | 2 | 128 | 128 |
| S. aureus | 0,12—1 | 2 | 32 | 4 | 2 | 64 |
В том случае, если сформировалась перфорация барабанной перепонки, возможности местной терапии значительно сужаются, так как в этом случае неприменимы препараты, содержащие в своем составе ототоксические антибиотики (фрамицетин, гентамицин, неомицин, полимиксин В), а также спирты, феназон или холина салицилат.
Особый случай представляет лечение острого диффузного наружного отита («ухо пловца»). Эта патология представляет собой инфекционное поражение кожи наружного слухового прохода, которое чаще всего развивается после плавания или же в других ситуациях, когда уши подвергаются длительному воздействию воды, что провоцирует мацерацию эпителия и бактериальный рост (наиболее часто S. aureus, P. aeruginosa, Enterobacteriaceae).
При этой патологии в легком случае рекомендовано использование ушных капель, содержащих антибактериальные препараты с антипсевдомонадной активностью (ципромед, нормакс), а при тяжелом течении — левофлоксацин (перорально или внутривенно 0,5 г 1—2 раза в сутки) или пенемы (внутривенно 0,5 г 4 раза в сутки).
Важное значение при проведении топической терапии имеет безопасность компонентов ушных капель. В случае частого использования местных антибиотиков при лечении воспалений среднего уха следует обратить внимание на возможность поражения звуковосприятия. Считается, что при местном применении всасывается от 0,5 до 5% аминогликозидов, а воспаление среднего уха может способствовать проникновению антибиотиков к внутреннему уху. Подобным является действие токсинов (продуктов воспаления или распада бактерий), потенцирующих ототоксические эффекты препаратов [21]. Кроме того, некоторые составные части ушных капель (пропиленгликоль, хлоргексидин) могут также представлять опасность для внутреннего уха.
Несмотря на то что ототоксичность не является абсолютным противопоказанием для применения ушных капель, содержащих ототоксические антибиотики [22], в 1996 г. Всемирная организация здравоохранения рекомендовала не использовать аминогликозиды для местноголечения отита из-за их ототоксичности [23]. Наиболее безопасными, с точки зрения ототоксичности, являются хлорамфеникол и фторхинолоны. Некоторые данные по ототоксичности компонентов ушных капель представлены в табл. 3.
Таблица 3. Потенциальная ототоксичность некоторых компонентов ушных капель, применяемых в России [24, 25]
| Препарат | Антибактериальный компонент | Противогрибковый компонент | Местный анестетик | Противовоспалительный компонент | Примечание |
| Унифлокс | Офл (—) | — | — | — | Фторхинолоны считаются одними из наиболее ототоксически безопасных топических антибиотиков |
| Нормакс | Нор (—) | — | — | — | |
| Ципромед | Цпр (—) | — | — | — | |
| Комбинил-Дуо | Цпр (—) | — | — | Дек (—) | |
| Гаразон | Ген (+) | — | — | Бет (—) | Ототоксичность Нео выше таковой Ген |
| Дексона | Нео (+) | — | — | Дек (—) | |
| Софрадекс | Фра (+) Гра (±) | — | — | Дек (—) | Ототоксичность Фра сопоставима с Ген. Топическая ототоксичность Гра мало-изучена |
| Кандибиотик | Хло (—) | Кло (—) | Кси (—) | Бек (—) | Ототоксичность Хло у человека при топическом применении не описана |
| Полидекса | Пол (+) Нео (+) | — | — | Дек (—) | Ототоксичность Пол сопоставима с таковой Ген |
| Анауран | Пол (+) Нео (+) | — | Кси (—) | — | |
| Отипакс | — | — | Кси (—) | Фен (+) | Ототоксичность проявляется в случае попадания в среднее ухо |
| Отинум | — | — | — | Хс (+) |
Примечание. Офл — офлоксацин, Нор — норфлоксацин, Цпр — ципрофлоксацин, Ген — гентамицин, Нео — неомицин, Фра — фрамицетин, Гра — грамицидин, Хло — хлорамфеникол, Пол — полимиксин В, Кло — клотримазол, Кси — ксилокаин, Дек — дексаметазон, Бет — бетаметазон, Бек — беклометазон, Хс — холина салицилат, (—) — топическая ототоксичность отсутствует, (+) — топическая ототоксичность возможна.
В том случае, если требуется системное введение антимикотиков (тяжелое поражение), то препаратами выбора являются амфотерицин В и вориконазол [17].
Противовоспалительные препараты являются наиболее частыми компонентами комбинированных препаратов ушных капель. В этом качестве выступают как стероидные противовоспалительные средства (дексаметазон, бетаметазон, беклометазон), так и нестероидные (феназон, холина салицилат). Их включение в комбинированные рецептуры призвано блокировать каскад медиаторных реакций и уменьшить выраженность воспаления (асептического или септического), сопровождающего развитие патологии уха. Это ведет к купированию таких симптомов воспаления, как боль, отек, расширение сосудов слизистой оболочки, избыточная экссудация. Именно поэтому противовоспалительная терапия является важным компонентом в лечении острого отита.
Глюкокортикоиды (ГК) через ряд внутриклеточных процессов способны увеличивать синтез различных регуляторных белков, в том числе т.н. липокортинов, обладающих высокой биологической активностью, одним из проявлений которой является блокада фермента фосфолипазы А2. Следствием этого является подавление образование простагландинов, тромбоксана А2 и лейкотриенов в начальной стадии (на этапе образования арахидоновой кислоты).
Благодаря подавлению активности ряда транскрипционных факторов (например NF×В), в значительной степени угнетается синтез интерлейкинов (IL-1, IL-3, IL-4, IL-5, IL-6, IL-8), TNF-α, играющих важную роль в развитии воспаления, снижется количество и угнетается активность эозинофилов, тучных клеток, Т-лимфоцитов.
ГК активируют ангиотензинпревращающий фермент и нейтральную эндопептидазу, в результате чего ускоряется разрушение брадикинина, участвующего в регуляции сосудистого тонуса, свертывания крови и процессов воспаления. Кроме того, под влиянием этих препаратов происходит уменьшение проницаемости стенки сосудов за счет повышения синтеза вазокортина и понижения образования или активности лизосомальных ферментов (протеаз, гиалуронидазы и др.), гистамина, брадикинина, простагландинов и лейкотриенов. Дополнительным механизмом противовоспалительного эффекта ГК является нарушение ими синтеза молекул адгезии: ICAM (intercellular adhesion molecules), VCAM (vascular cell adhesion molecule), ELAM-1 (endothelial-leukocyte adhesion molecule 1), принимающих участие в процессах миграции. Наиболее мощное противовоспалительное действие присуще именно ГК.
Нестероидные противовоспалительные агенты (феназон, холина салицилат) реализуют свои эффекты, неселективно блокируя фермент циклооксигеназу, благодаря чему снижается образование простагландинов и уменьшается опосредуемая ими вазодилатация и экссудация, альгезия и воспаление. По выраженности противовоспалительного действия они значительно уступают ГК.
ГК не обладают ототоксичностью в отличие от топических нестероидных противовоспалительных препаратов, которые не следует назначать при перфорации барабанной перепонки.
Местноанестезирующие препараты необходимы, в первую очередь, для уменьшения боли и улучшения качества жизни больного с отитом. Наиболее часто для этой цели используется ксилокаин (лидокаин). Механизм его местноанестезирующего эффекта заключается в блокаде быстрых натриевых каналов нейрональной мембраны, что препятствует возникновению потенциала действия и проведению импульсов. Возможен антагонизм с ионами кальция. Не обладая противовоспалительным действием, он способен оказывать быстрое анальгезирующее действие, развивающееся примерно в течение 1—2 мин.
Таким образом, своевременное распознавание и рациональное лечение острого и хронического воспалительных заболеваний уха позволяет предупредить не только формирование стойкой тугоухости, но и развитие мастоидита, тяжелых, опасных для жизни внутричерепных осложнений, а также распространение патологического процесса на лабиринт, лицевой нерв [20, 27, 28]. Это достигается рациональным применением целого ряда фармакологических средств, позволяющих добиться быстрой элиминации разнообразных этиологических факторов, уменьшения воспаления и повышения качества жизни больного. Одним из способов решения этой задачи является использование при наружном и среднем отитах комбинированных топических препаратов, содержащих комбинацию антибактериального, антимикотического, противовоспалительного и обезболивающего компонентов. В РФ этот принцип реализован в комбинированном четырехкомпонентном препарате Кандибиотик (Гленмарк Фармасьютикалз Лтд, Индия).