какие заболевания относятся к ревматическим
Диагностика и лечение поражений нервной системы при ревматических заболеваниях
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими с
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими свойствами.
Аутоиммунные процессы осуществляют информационный обмен между нейроэндокринной и иммунной системами, при этом главную роль играют аутоантитела к гормонам, медиаторам и их рецепторам. Продемонстрирован синтез нейропептидов в иммунокомпетентных клетках, а в клетках нейроэндокринной системы доказана возможность синтеза лимфокинов и монокинов.
Получены данные о нейрогенной регуляции функций иммунитета и их нарушений, в то же время иммунокомпетентные клетки и их медиаторы могут влиять на функцию центральной нервной системы (ЦНС) по принципу нейроиммуномодуляции. Показано, что свойством нейросекреции обладает вся центральная и периферическая нервная система. Влияние иммунной и нервной систем друг на друга реализуется через рецепторные структуры клеток, взаимодействие которых создает связи «рецептор-рецептор» и таким образом организует молекулярный механизм совместной работы обеих систем.
Функционирование клеток и сигнальная информация обеспечиваются медиаторами и нейротрансмиттерами в обеих системах, между нервной и иммунной системой происходит взаимообмен информацией с помощью цитокинов, стероидов и нейропептидов [1, 2].
Таким образом, доказана общность и взаимосвязь нервной и иммунной систем, сходство между их структурами и функциями и развитие нового направления современной иммунологии — нейроиммунологии [3, 4]. Широкий диапазон неврологических синдромов при аутоиммунных системных заболеваниях позволяет рассматривать их как модельные системы для изучения патогенетической роли иммунных механизмов поражения центральной и периферической нервной системы [5].
Потенциальными мишенями для аутоиммунной агрессии могут быть различные антигены нервной ткани, включая миелин, в том числе ассоциированный с гликопротеином, и его основной белок, ганглиозиды, белок ядер нейрональных клеток и другие [6]. Так, мишеневидные антигены при нейролюпусе представлены антигенами нейрональной ткани, рибосомальным Р-белком, рДНК, малым ядерным рибонуклеопротеидом, а также анионными фосфолипидами при антифосфолипидном синдроме, что обуславливает широкий спектр неврологической симптоматики при данной патологии [7, 8].
По данным различных авторов, частота поражений нервной системы при ревматических заболеваниях (РЗ) колеблется от 40% до 70% и выше, если учитывать психические синдромы и головную боль. Неврологические синдромы включены в классификационные критерии системных васкулитов, опубликованные Американской коллегией ревматологии в 1990 году, в диагностические критерии и критерии активности системной красной волчанки (СКВ), а также в ряд других диагностических критериев, в частности узелкового полиартериита у детей. Неврологические нарушения при РЗ требуют проведения дифференциальной диагностики и назначения адекватного лечения совместно ревматологом и неврологом.
При СКВ в диагностические критерии неврологических поражений включены судороги или психозы. Поражение ЦНС обусловлено в основном сосудистой патологией, к которой относят васкулопатию, тромбозы, истинные васкулиты, инфаркты и геморрагии [7]. В цереброспинальной жидкости обнаруживаются антинейрональные антитела, определяется повышение уровня белка, увеличение клеточного состава. Описаны разные виды судорожных припадков: большие, малые, по типу височной эпилепсии, а также гиперкинезы. При ЦНС-люпусе имеет место головная боль типа мигрени, устойчивая к анальгетикам, но отвечающая на лечение глюкокортикостероидами. Параличи черепных нервов обычно сопровождаются офтальмоплегией, мозжечковыми и пирамидными симптомами и нистагмом. Имеют место зрительные нарушения, преходящие нарушения мозгового кровообращения. Острый поперечный миелит встречается редко и имеет неблагоприятный прогноз. Психические синдромы разнообразны и характеризуются аффективными, органическими мозговыми или шизофреноподобными проявлениями [9, 10].
В рамках СКВ был описан и антифосфолипидный синдром. Этот синдром включает: рецидивирующие артериальные или венозные тромбозы, привычное невынашивание беременности и тромбоцитопению и дополнительные признаки: сетчатое ливедо, неврологические проявления: хорею, эпилепсию, мигренеподобную головную боль, нарушения мозгового кровообращения и деменцию вследствие множественных инфарктов, хронические язвы голеней, Кумбс-положительную гемолитическую анемию, клапанные поражения сердца и серологические маркеры — антифосфолипидные антитела, к которым относятся антикардиолипиновые антитела IgG и IgM и волчаночный антикоагулянт [11].
При системной склеродермии (ССД) неврологический синдром представлен в основном полиневритическими проявлениями, связанными с сосудистыми изменениями и фиброзными процессами в соединительной ткани. Для узелкового полиартериита характерны множественные мононевриты, для гранулематоза Вегенера — асимметричная полинейропатия, для неспецифического аортоартериита — дисциркуляторная энцефалопатия и нарушения мозгового кровообращения.
Собственные данные включали обследование 229 больных различными формами РЗ, среди которых 110 больных страдали системными заболеваниями соединительной ткани: 88 больных СКВ, 22 — ССД и 119 больных — системными васкулитами: облитерирующий тромбангиит (ОТ) — 21, узелковый полиартериит (УП) — 27, неспецифический аортоартериит — (НАА) — 32, геморрагический васкулит (ГВ) — 15 и гранулематоз Вегенера (ГрВ) — 2, другие формы — 22. Проведено детальное неврологическое исследование, ультразвуковая транскраниальная допплерография сосудов мозга, реоэнцефалография, компьютерная (КТ) и магнитно-резонансная томография (МРТ) головного мозга, электроэнцефалография, исследование иммунного статуса.
У большинства больных заболевания дебютировали кожным (50,6%), суставно-мышечным (35,4%) и сосудистым (27,1%) синдромом. Органные поражения в дебюте регистрировались с частотой 7%, синдром артериальной гипертензии — у 5,2%, лихорадка — у 7,0%, гематологические нарушения — 7,9%. Неврологические расстройства в дебюте заболевания отмечены у 12,2% и проявлялись моно- и полиневропатией и синдромом энцефаломиелополирадикулоневрита (ЭМПРН). Поражение периферической нервной системы в дебюте заболевания было особенно характерно для УП и наблюдалось у 30% больных. Основными синдромами дебюта со стороны ЦНС был цефалгический (10,5%) и вестибулярный (6,3%), чаще они наблюдались при НАА. Вовлечение ЦНС имело место у 96 (41,9%) больных, являясь наиболее выраженным при СКВ, НАА, УП.
Цереброваскулярная патология была доминирующей в клинической картине болезни у 34,7% больных, а иногда разнообразные симптомы поражения ЦНС развивались задолго до появления полисиндромной картины заболевания. Основные клинические проявления цереброваскулярной патологии включали: цефалгический (82%), астенический (76%), вестибулярно-атактический (80%), пирамидный (74%) синдромы, синдром вегетативно-сосудистой недостаточности (69%), диссомнический (79%) и базально-оболочечный (37%), гипопоталамической дисфункции (34,7%).
Описанная неврологическая симптоматика часто сочеталась с симптомами сосудистой недостаточности головного мозга, которые объединялись синдромом дисциркуляторной энцефалопатии 1 (11%), 2 (26,4%) или 3 (8%) степени. У 7,8% больных имели место преходящие нарушения мозгового кровообращения.
Гипоталамическая дисфункция у больных РЗ проявлялась полиморфными нейроэндокринными расстройствами, нарушением терморегуляции, преимущественно по типу пароксизмальной центральной гипертермии, инсомнией, патологией психоэмоциональной сферы.
Установлено достоверное преобладание у больных пирамидной недостаточности слева (41%). Преобладание пирамидной недостаточности справа регистрировалось реже (23,7%). Дистонические феномены в форме вестибулярно-мозжечковой установки кисти и диссоциированная мышечная гипотония в ногах также были более выражены слева. Полученные данные свидетельствуют о преобладающем поражении пирамидной и сенсорной систем, а также неспецифических структур правого полушария, которое тесно связано с гипоталамической областью и обеспечивает адаптацию организма к воздействующим факторам внешней среды. Обнаруженная функциональная асимметрия свидетельствует о срыве адаптационных механизмов нервной системы и указывает на роль дисфункции правополушарно-гипоталамической системы.
При использовании методов МРТ и/или КТ было выявлено изменение желудочковой системы в виде ее расширения или деформации и/или расширения субарахноидального пространства, а также очаговые поражения различных структур головного мозга, атрофия вещества мозга и краниовертебральные аномалии. Признаки наружной, внутренней или сочетанной гидроцефалии отмечались при всех нозологических формах. Очаговые изменения вещества мозга включали гиперденситивные зоны, гиподенситивные зоны с отеком или без него, единичные или множественные.
При исследовании сосудистой системы и мозгового кровообращения достоверно наблюдалось повышение тонуса сосудов, гипертонический и дисциркуляторный тип кровообращения по данным реоэнцефалографии (РЭГ) и увеличение линейной скорости кровотока по средней мозговой артерии. Больные с вовлечением ЦНС отличались по электроэнцефалографии: им были свойственны диффузные патологические изменения, наличие дезорганизации альфа-ритма, дизритмий и пароксизмальной активности.
Корреляционный анализ цереброваскулярной патологии и результатов инструментальных исследований сосудов головного мозга показал, что при всех нозологических формах у пациентов имело место нарушение венозной гемоциркуляции. В последующем происходило сужение церебральных артерий, ликвородинамические нарушения с формированием внутричерепной гипертензии, нарушением системы микроциркуляции в головном мозге. Очаговые поражения головного мозга отличались локализацией процесса в зависимости от нозологической формы. В табл. представлены основные неврологические проявления РЗ.
У 39% больных СКВ молодого возраста с поражением ЦНС имели место нарушения мозгового кровообращения, причем у половины из них инсульт развился в начале заболевания. Одновременно с инсультом в дебюте СКВ у больных чаще выявлялась «сосудистая бабочка» и/или вазоспастический синдром, повышение артериального давления, чаще диастолического. У этих больных отмечались умеренные или высокие титры кардиолипинов IgG, антител к нативной ДНК и ревматоидного фактора (РФ) IgM, что могло свидетельствовать о наличии текущего церебрального васкулита. Эти данные подтверждались выявлением гипертонуса резистивных интракраниальных сосудов и патологией микроциркуляторного русла в виде увеличения количества функционирующих капилляров, их выраженной извитостью с замедлением кровотока в артериолах. Изменения в свертывающей системе характеризовались синдромом гиперкоагуляции. Выявлены основные факторы риска развития инсульта у больных РЗ: артериальная гипертензия, поражения сердца, гиперкоагуляция, иммунное воспаление сосудистой стенки, асимметрия мозгового кровотока.
Среди больных РЗ цереброваскулиты (ЦВ) имели место у 28,3% больных. Диагноз ЦВ ставился при обнаружении очаговой неврологической симптоматики, изменений на глазном дне, снижения зрения, наличии признаков нарушения мозгового кровообращения, а также по результатам КТ и ядерно-магнитно-резонансной томографии (ЯМРТ), при которых выявлялись наружная и внутренняя гидроцефалия, очаговые изменения в коре и субкортикальном веществе. При этом с течением времени число очагов любой локализации в головном мозге нарастало. При магнитно-резонансном ангиографическом (МРА) исследовании отмечались множественные сегментарные неровности сосудистой стенки, циркулярные или эксцентричные стенозы и дилятация мелких и средних интракраниальных артерий с формированием аневризм, нарушения кровотока. Выявленное снижение интенсивности МРА-сигнала на фоне повышения активности ревматического процесса свидетельствовало о наличии ЦВ.
Иммунологическими маркерами ЦВ считали антитела к нативной ДНК, IgG-антитела к кардиолипину (аКЛ) и IgM аКЛ, антинейтрофильные цитоплазматические антитела (АНЦА), в меньшей степени — РФ и волчаночный антикоагулянт (ВА). Имели место клинико-иммунологические корреляции с неврологическими проявлениями.
Изолированный (первичный) ЦВ характеризовался обнаружением симптомов вовлечения ЦНС и такими признаками, как головная боль, судороги, менингеальный синдром, острая прогрессирующая энцефалопатия без признаков экстракраниального или системного васкулита, психические синдромы, деменция, прогрессирующее снижение интеллекта, инсульты, нарушения зрения, нистагм. Чаще перивентрикулярные очаги выявлялись в первый год заболевания.
Ряд больных обращались на консультацию к окулисту в связи с ухудшением зрения, вплоть до амавроза, наличием увеита, ишемического неврита. Ангиопатия сетчатки имела место у 41% этих больных, флебопатия — у 14%, ретиноваскулит — у 6%, ангиоспазм — у 13%, ангиосклероз — у 18%.
Полиневритический синдром встречался у подавляющего большинства больных (96,7%) в виде сенсорной, чувствительно-двигательной полиневропатии или в сочетании с поражениями ЦНС, с синдромом ЭПН и ЭМПРН. При ССД, ОТ и ГВ преобладали формы в виде чувствительной или чувствительно-двигательной полиневропатии, а при СКВ и НАА — формы с сочетанным поражением периферической НС (ПНС) и ЦНС — синдромы ЭПН и ЭМПРН. При ОТ и НАА отмечалась отчетливая диссоциация степени выраженности полиневропатии по оси тела, причем при ОТ симптоматика была более отчетливой в ногах, при НАА — в руках. В целом асимметричная полиневропатия имела место у 19,2% больных, достигая максимума при УП (59,3%).
Патология НС при РЗ нередко определяет прогноз, клиническую картину заболевания и качество жизни больных, а также требует обязательного сочетанного применения базисной противовоспалительной терапии, ангио- и нейропротекторов. К группе нейропротекторов относят Актовегин, Инстенон. Используются препараты, улучшающие мозговое кровообращение, — Винпоцетин, Кавинтон, метаболические средства с антигипоксантным действием — Ноотропил, Пирацетам, Церебролизин, по показаниям седативные и противосудорожные средства, антидепрессанты.
При РЗ терапия включает глюкокортикостероиды, иммуносупрессанты, иммуноглобулин, плазмаферез, иммуномодуляторы, дезагреганты, нестероидные противовоспалительные препараты и симптоматические средства.
Лечение состоит из нескольких этапов: быстрое подавление иммунного ответа в дебюте заболевания и при его обострениях (индукция ремиссии); длительная поддерживающая терапия иммуносупрессантами, в дозах, достаточных для достижения клинической и лабораторной ремиссии заболевания; определение степени повреждения органов или систем организма и их коррекция, проведение последующих реабилитационных мероприятий.
Первый этап включает эффективное подавление иммунного воспаления на ранних стадиях болезни и предполагает использование глюкокортикостероидов, иммуносупрессантов цитостатического действия типа Циклофосфана и антиметаболитного действия типа Метотрексата, цитокинсупрессивного препарата Циклоспорина А, внутривенного иммуноглобулина, назначение повторных курсов пульс-терапии метилпреднизолоном и Циклофосфаном, в сочетании с экстракорпоральными методами лечения.
При острых церебральных нарушениях при высокой активности СКВ используется схема пульс-терапии с введением Метипреда 1 г внутривенно 1 раз в день в течение 3 дней и с добавлением 800 мг Циклофосфана во 2-й день. При хроническом течении СКВ суточная доза преднизолона составляла 15–20 мг с последующим постепенным снижением, Циклофосфан применяется внутримышечно в дозе 400 мг в неделю до 1600–2000 мг на курс, затем по 200 мг в неделю в течение года и более. Апробируются препараты мофетила микофенолат и лефлуномид.
При патологии органа зрения назначают нестероидные противовоспалительные препараты в виде инъекций диклофенака, а затем пероральные препараты этой группы, дезагреганты, при наличии признаков воспалительной активности добавляют умеренные дозы глюкокортикостероидов, а при резком снижении зрения и выраженных признаках активности используют пульс-терапию.
Проводится определение наиболее эффективных и менее токсичных схем применения иммуносупрессивных препаратов, путей их введения, и включение в комплексное лечение больных препаратов, улучшающих микроциркуляцию и/или влияющих на реологические свойства крови (Гепарин, Фраксипарин, Трентал, Ралофект, Тиклид).
В ряде случаев назначают препараты типа Реаферона, а при наличии инфицированных язв, некрозов кожи или конечностей применяют антибиотики. Ввиду многообразия нозологических форм на выбор лекарственных средств в дебюте заболевания оказывает влияние распространенность патологического процесса и наличие интеркуррентной инфекции. Показано назначение ангиопротекторов и посиндромная терапия.
Учитывая высокий удельный вес неврологической патологии, больные РЗ должны проходить комплексное клинико-инструментальное неврологическое исследование уже на ранней стадии патологического процесса. Постановка диагноза РЗ и комплексная терапия глюкокортикостероидами и иммуносупрессантами способствуют коррекции нарушений ЦНС и ПНС.
Ревматологический комплекс
Ревматологические заболевания у людей чаще всего ассоциируются с заболеваниями суставов, хотя могут поражаться различные органы и системы. Как можно заподозрить ревматологическое заболевание и какие анализы необходимо сдать?
Ревматологические заболевания представляют большую группу заболеваний, поражающих соединительную ткань организма. Ещё их называют аутоиммунными или системными заболеваниями. Аутоиммунные – потому что иммунная система теряет способность распознавать «своё-чужое» и вырабатывает антитела против собственных клеток и тканей. Системные – так как соединительная ткань содержится во всех органах и сосудах, поэтому затрагиваются все системы организма в той или иной степени. Причина ревматологических заболеваний до конца неясна. Но последствия серьёзные, и раннее распознавание важно для своевременного лечения и предотвращения осложнений.
Как можно заподозрить ревматологическое заболевание?
Вышеперечисленные признаки могут возникать при ряде других заболеваний, хотя зачастую они являются единственными «тревожными сигналами» для начала обследования.
На самом деле, зачастую происходят изменения со стороны сердца, легких, почек, нервной системы и других внутренних органов, но они не имеют ярких проявлений. Иногда обращают внимание признаки поражения кожи – в виде различных высыпаний. Покраснения кожи лица в форме «бабочки» возникают при системной красной волчанке; утолщение кожи пальцев при склеродермии.
Как ставится диагноз?
Для того, чтобы установить ревматологическое заболевание, врач оценивает 2 критерия:
Только на основании совместной оценки клинического и лабораторного критериев возможно установить диагноз ревматологического заболевания и различить, какое именно заболевание из целой группы имеет место. Ни один критерий не используется изолированно!
Для Вашего удобства основные лабораторные тесты объединены в комплекс «Ревматологический, расширенный».
Что входит в состав комплекса?
Что нужно сдать и как подготовиться к исследованию?
Для исследования на ревматологический комплекс сдаётся венозная кровь утром натощак или через 3 часа после необильного приёма пищи. Накануне рекомендуется отказаться от алкоголя.
Ревматологическое заболевание хорошо лечится на ранних стадиях. Обращайте внимание на своё здоровье, будьте внимательны к себе и обследуйтесь своевременно!
Основные сведения о ревматических болезнях
| Сайт: | Образовательный портал МБФ (ВолгГМУ) |
| Курс: | Медицинская биохимия, принципы измерительных технологий в биохимии, патохимия, диагностика, биохимия злокачественного роста. Часть 3 |
| Книга: | Основные сведения о ревматических болезнях |
Оглавление
1. Введение
Современная ревматология оформилась в самостоятельный раздел медицины, чему способствовало выделение большого числа так называемых ревматических болезней, объединенных по принципу преимущественного поражения опорно-двигательного аппарата. В связи с этим термин «ревматический» приобрел неоднозначность и может относиться как к истинному ревматизму—болезни Сокольского — Буйо (ревматический кардит, ревматическая хорея и т.д.), так и к ревматическим заболеваниям вообще. Группа ревматических заболеваний включает болезни, которые, имея ряд общих черт с ревматизмом, в большинстве случаев существенно отличаются по этиологическим факторам, патогенетическим механизмам и клиническим проявлениям.
В настоящей главе основные ревматические заболевания представлены в виде 4 разделов: болезни с преимущественным поражением собственно суставов; васкулиты и диффузные болезни соединительной ткани, в основе которых лежит системное иммуновоспалительное поражение соединительной ткани и ее производных с частым вовлечением в процесс локомоторного аппарата; истинный ревматизм.
2. Классификация и номенклатура
Рабочая классификация и номенклатура ревматических болезней
I. Острая ревматическая лихорадка и хроническая ревматическая болезнь сердца. (Бывший РЕВМАТИЗМ)
II. Системные поражения соединительной ткани
1.0. Системная красная волчанка
1.1. Идиопатическая
1.2. Лекарственный волчаночноподобный синдром
2.0. Системная склеродермия
2.1. Идиопатическая
2.2. Индуцированная (химическая или лекарственная)
3.0. Диффузный фасциит
4.0. Дерматомиозит / полимиозит
4.1. Идиопатический
4.2. Паранеопластический
4.3. Ювенильный
4.4. Миозит «inclusion body»*
5.0. Синдром Шегрена
5.1. Первичный (болезнь Шегрена)
5.2. Вторичный (в сочетании с другими ревматическими заболеваниями)
5.3. «Сухой» синдром при ВИЧ-инфекции*
6.0. Перекрестные (overlap’s) синдромы
6.1. Смешанное заболевание соединительной ткани
6.2. Другие перекрестные синдромы*
7.0. Рецидивирующий полихондрит
8.0. Антифосфолипидный синдром*
III. Системные васкулиты (ангииты, артерииты); васкулопатии*
1.0. Узелковый полиартериит
2.0. Гранулематозные артерииты:
2.1. Гранулематоз Вегенера
2.2. Синдром Черджа—Стросса*
3.0. Гигантоклеточные артерииты
3.1. Височный артериит (болезнь Хортона)
3.2. Ревматическая полимиалгия
3.3. Неспецифический аортоартериит (болезнь Такаясу)
4.0. Гиперегические ангииты
4.1. Геморрагический васкулит (болезнь Шенлейна—Геноха)
4.2. Смешанная криоглобулинемия (криоглобулинемическая пурпура)
5.0. Облитерирующий тромбоангиит (болезнь Бюргера)
6.0. Синдром Гудпасчера
7.0. Болезнь Бехчета
8.0. Болезнь Кавасаки (слизисто-кожно-железистый синдром)
9.0. Тромботическая тромбоцитопениче-ская пурпура (синдром Мошковиц)
10.0 Васкулиты при аутоиммунных, инфекционных заболеваниях и опухолях
IV. Ревматоидный артрит
1.0. Серопозитивный (по ревматоидному фактору)
2.0. Серонегативный (по ревматоидному фактору)
3.0. Без системных проявлений (полиартрит, олигоартрит, моноартрит)
4.0. С системными проявлениями
4.1. Синдром Фелти
4.2. Болезнь Стилла у взрослых*
V. Ювенильный артрит
VI. Анкилозирующий спондилит и другие артриты, сочетающиеся со спондилитом (спондилоартропатии)
1.0. Анкилозирующий спондилит (болезнь Бехтерева)
2.0. Реактивный артрит
3.0. Псориатический артрит
4.0. Артриты при хронических воспалительных заболеваниях кишечника (язвенный колит,болезнь Крона)
VII. Артриты, связанные с инфекцией
1.0. Инфекционные артриты
1.1. Бактериальные
1.1.1. Лаймовская болезнь
1.1.2. Болезнь Уиппла
1.1.3. Бруцеллез
1.2. Вирусные
1.2.1. Карельская лихорадка
1.2.2. Артрит при ВИЧ-инфекции
1.2.3. Артрит при HTLV-1 инфекции*
1.3. Грибковые
1.4. Паразитарные
2.0. Реактивные артриты
2.1. Постэнтероколитические
2.2. Урогенитальные
2.3. После носоглоточной инфекции
2.4. После кишечного шунтирования
2.5. После других инфекций
2.6. Поствакцинальные
VIII. Микрокристаллические артриты
1.0. Подагра первичная
2.0. Подагра вторичная
3.0. Хондрокальциноз («псевдоподагра»)
4.0. Гидроксиапатитовая артропатия
5.0. Другие микрокристаллические артриты
IX. Остеоартроз (остеоартрит) и близкие болезни
1.0. Остеоартроз
1.1. Первичный
1.2. Вторичный
1.3. Спондилез, спондилоартроз
1.4. Эндемический (болезнь Кашина—Бека)
2.0. Остеохондроз межпозвоночный
3.0. Идиопатический диффузный гиперостоз скелета (болезнь Форестье)
X Другие болезни суставов
1.0. Палиндромный ревматизм
2.0. Интермиттирующий гидроартроз
3.0. Множественный ретикулогистиоцитоз
4.0. Синовиома
5.0. Хондроматоз суставов
6.0. Виллезонодулярный синовит
XI. Болезни внесуставных мягких тканей
1.0. Болезни мышц
1.1. Миозиты
1.2. Оссифицирующий миозит
1.3. Идиопатический кальциноз
2.0. Болезни околосуставных тканей
2.1. Энтезопатии
2.2. Тендиниты (включая «щелкающий палец»)
2.3. Тендовагиниты (включая болезнь де Кервена)
2.4. Бурситы (включая кисту Бейкера)
2.5. Периартриты
2.6. Синдром запястного канала и другие лигаментиты
3.0. Болезни фасций и апоневрозов
4.0. Болезни подкожно-жировой клетчатки
4.1. Узловатая эритема
4.2. Болезненный липоматоз Деркума
4.3. Панникулиты (включая болезнь Ве-бера—Крисчена)
5.0. Первичная фибромиалгия
5.1. Психогенный ревматизм
5.2. Синдром хронической усталости*
XII. Болезни костей, хряща и остеохондропатии
1.0. Болезни костей
1.1. Остеопороз генерализованный
1.2. 0стеомаляция
1.3. Гипертрофическая остеоартропатия
1.4. Болезнь Педжета (деформирующий остеит)
1.5. 0стеолиз (неуточненной этиологии)
1.6. Несовершенный остеогенез
2.0. Остеохондропатии
2.1. Асептический некроз головки бедренной кости
2.2. Остеохондропатии тел позвонков
2.3. Остеохондропатии бугристости большеберцовой кости
3.0. Остеохондриты
3.1. Рассекающий остеохондрит Кенига
3.2. Другие остеохондриты
XIII. Артропатии при неревматических заболеваниях
1.0. Аллергические заболевания
1.1. Сывороточная болезнь
1.2. Лекарственная болезнь
1.3. Другие аллергические состояния
2.0. Метаболические нарушения
2.1. Амилоидоз
2.2. Охроноз
2.3. Гиперлипидемия
2.4. Гемохроматоз
2.5. Болезнь Вильсона*
3.0. Врожденные дефекты метаболизма соединительной ткани
3.1. Синдром Марфана
3.2. Синдром Элерса—Данлоса
3.3. Синдром гипермобильности
3.4. Мукополисахаридоз
4.0. Эндокринные заболевания
4.1. Сахарный диабет
4.2. Акромегалия
4.3. Гиперпаратиреоз
4.4. Гипертиреоз
4.5. Гипотиреоз
4.6. Болезнь Аддисона*
5.0. Поражение нервной системы
5.1. Артропатия Шарко
5.2. Альгодистрофия
5.3. Синдром «плечо-кисть»
6.0. Болезни системы крови
6.1. Гемофилия
6.2. Гемоглобинопатии
6.3. Лейкозы
6.4. «Миеломная болезнь»
7.0. Паранеопластический синдром
8.0 Профессиональные болезни
8.0. Вибрационная болезнь
8.1. Силикоз
8.2. Кесонная болезнь
8.3. Другие нарушения
9.0. Другие заболевания
9.1. Саркоидоз
9.2. Периодическая болезнь
9.3. Хронический активный гепатит
9.4. Гиповитаминоз С
9.5. Глютеновая энтеропатия*
9.6. Иммуннодефицитные заболевания
* Заболевания или термины, не вошедшие в официальную классификацию.
3. Острая ревматическая лихорадка (ОРЛ)
3.1. Этиология
Streptococcus pyogenes (β-гемолитический стрептококк группы А) представляет собой грамположительный каталазонегативный кокк. Патогенные штаммы БГСА- М3, М5, М18, М19, М24. Этому способствует обилие факторов патогенности стрептококков:
3.2. Эпидемиология
В 20-30 годах XX века больничная летальность от острой РЛ с вовлечением сердца составляла до 40 %, частота формирования пороков доходила до 50-75 %. Благодаря активной антиревматической работе, организационным мероприятиям и научным достижениям в 60-70-е годы в СССР заболеваемость ревматизмом уже составляла 20-30 случаев на 1000, причём в Москве и Ленинграде этот показатель был на уровне 8-9, в Уфе — 38, в Красноярске — 98 случаев на 1000 населения. Летальность к этому моменту снизилась до 2 %, а частота формирования пороков — до 15-30 %. Мероприятия по внедрению повсеместной бициллинопрофилактики, диспансерного наблюдения, улучшению социального положения населения привели заболеваемость к уровню развитых стран — 0,3-0,8 на 1000 населения [И. М. Воронцов, 2003].
В последнее время наметилась тенденция к увеличению частоты случаев РЛ в различных странах. Так, в Индии заболеваемость составляет в среднем 6 на 1000 населения, в США (штаты Пенсильвания, Огайо, Тенесси, Западная Вирджиния, Калифорния) зарегистрировано 8 вспышек РЛ в средних слоях населения и в воинских коллективах, причём заболеваемость среди детей увеличилась в 5-12 раз в 24 штатах [Н. И. Брико, 2003; E.M. Ayob, 1992 ; A.S.Dajani et al., 1993; L.G.Veasy et al., 1994]. В связи со снижением уровня жизни населения России ревматизм вновь становится актуальной проблемой и в нашей стране. Об этом свидетельствует тот факт, что в 1994 г (разгар войны в Чеченской республике) показатель заболеваемости ревматизмом на Северном Кавказе был почти в 3 раза выше, чем в среднем по России [В. А. Насонова и соавт., 1996]. Именно в этот период шли наиболее активные миграционные процессы, люди жили во временных жилищах, а иногда и под открытым небом, часто малодоступной оказывалась и медицинская помощь. Вполне возможно, что подобного рода ситуации будут повторяться и в дальнейшем, требуя компетентности и настороженности внимания врачей первого контакта [Н. Н. Кузмина, М. Ю. Щербакова, 2004; В. А. Насонова и соавт., 1996]. В последние годы по России в целом и по отдельным её территориям заболеваемость РЛ снизилась.
3.3. Патогенез
В патогенезе ОРЛ также можно говорить о ревматической патогенетической триаде:
1. Прямое повреждение миокарда факторами патогенности БГС-А.
2. Аутоиммунный механизм:
а — оголение аутоантигенов миокарда вследствие прямого повреждения;
б — антигенная мимикрия БГС-А и миокарда (сходство антигенов), то есть антитела на БГС-А способны поражать и миокард);
3. Сосудистый механизм (поражение сосудов миокарда по вышеописанным механизмам ведет к дисциркуляторным изменениям в миокарде — ишемии, ацидозу, — способствуя развитию воспаления, с одной стороны, и реактивному фиброзу, с другой).
Болезнь обычно начинается в возрасте 7— 15 лет. изредка — в 4— 5 лет. В 20 % случаев первая атака ревматизма развивается в юношеском или более старшем возрасте. При этом существенное значение имеет антигенное сходство (мимикрия) между соматическими фрагментами стрептококков и антигенами сарколеммы кардиомиоцитов, а также между М-протеином клеточной стенки бактерии и антигенами стромы миокарда и соединительной ткани клапанов сердца и суставов. Поэтому персистирующая стрептококковая инфекция, вызывающая сенсибилизацию организма, может привести к образованию иммунного ответа не только на антигены стрептококка, но и на антигены собственной соединительной ткани, прежде всего сердца. Это индуцирует аутоиммунизацию с развитием реакций гиперчувствительности немедленного и замедленного типов. В крови появляются перекрестнореагирующие антитела с образованием циркулирующих иммунных комплексов и фиксацией их на базальной мембране сосудов микроциркуляторного русла. Возникает реакция гиперчувствительности немедленного типа (ГНТ), для которой характерна морфология острого иммунного воспаления в виде экссудативнонекротического васкулита. Активируется комплемент, а его хемотаксические компоненты привлекают лейкоциты и макрофаги. Микробные антигены переносятся макрофагами на Т-лимфоциты-хелперы, ответственные за иммунологическую память, и извращают ее. Одновременно макрофаги вырабатывают ряд цитокинов. вызывающих пролиферацию В-лимфоцитов, ответственных за образование антител. Постепенно реакция ГНТ сменяется реакцией гиперчувствительности замедленного типа (ГЗТ), развивается склероз сосудов и периваскулярной соединительной ткани. в том числе сердца и суставов. Таким образом, изменения при ревматизме и его хроническое волнообразное течение oпpeделяются развитием и периодической сменой реакций ГНТ и ГЗТ. В результате участия в процессе иммунных реакций для всех форм ревматизма характерны гиперплазия и плазмоклеточная трансформация лимфоидной ткани, а также полисерозиты.
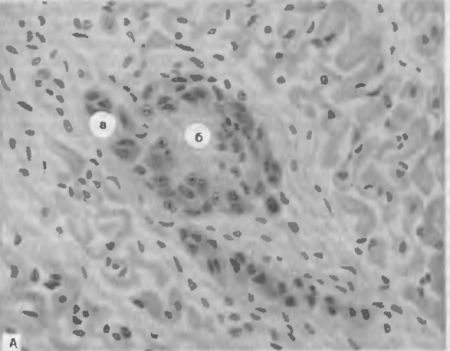
Рис. Ревматическая гранулема Ашоффа— Галалаева в строме миокарда. Гранулема состоит из гистиоцитов с базофильной цитоплазмой (а), в центре гранулемы — очаг фибриноидного некроза соединительной ткани (б).
Морфогенез ревматизма характеризуется прогрессирующей системной дезорганизацией соединительной ткани и изменениями сосудов микроциркуляторного русла, наиболее выраженными в строме и клапанах сердца. Стадия мукоидного набухания и фибриноидных изменений является морфологическим выражением реакций ГНТ. Клеточная воспалительная реакция проявляется в основном образованием специфических гранулем Ашоффа—Талалаева, названных в честь описавших их авторов (рис. 55). Гранулема при ревматизме формируется в ответ на фибриноидный некроз стенки сосуда микроциркуляторного русла и околососудистой соединительной ткани. Назначение ревматической грануле-i мы заключается в фагоцитозе некротических масс, содержащих остатки иммунных комплексов. Гранулема имеет определенную динамику, отражающую реакцию иммунокомпетентной системы. Вокруг очага фибриноидного некроза появляются крупные макрофаги с базофильной цитоплазмой и круглыми или овальными ядрами с центральным расположением хроматина («совиный глаз»), иногда встречаются многоядерные гистиоциты. Ревматическая гранулема при этом называется «цветущей». В дальнейшем реакции ГНТ сменяются на реакции ГЗТ, в гранулеме появляются фибробласты, количество фибриноидного детрита уменьшается («увядающая» гранулема). Затем фибриноид полностью paccaсывается и область гранулемы склерозируется («рубцующаяся гранулема). Ревматические гранулемы появляются также в суставных сумках, апоневрозах, перитонзиллярной соединительной ткани, в строме других органов.
Клинико-морфологические формы ревматизма выделяют на ocновании преимущественного поражения того или иного органа. Различают кардиоваскулярную, полиартритическую, церебральную и нодозную формы. Это деление условно, так как при ревматизме поражение сердца встречается всегда.
Эндокардит — воспаление эндокарда — чаще всего развивается в клапанном аппарате сердца (клапанный эндокардит).
В процесс могут быть вовлечены сухожильные хорды — хордальный эндокардит, а также пристеночный эндокард предсердий или желудочков — пристеночный (париетальный) эндокардит. Наиболее часто поражаются створки митрального клапана (65—70 % ревмокардитов). На 2-м месте по частоте комбинированное поражение створок митрального и аортального клапанов (25 %), на 3-м месте — аортального клапана. Изменения трехстворчатого клапана встречаются значительно реже, и исключительно редко возникают поражения клапана легочного ствола. Выделяют 4 вида связанных между собой морфологических изменений клапанов сердца: диффузный эндокардит (вальвулит), острый бородавчатый, фибропластический и возвратно-бородавчатый эндокардит.
Диффузный эндокардит (вальвулит) характеризуется мукоидным набуханием и умеренными фибриноидными изменениями соединительной ткани створок клапана без повреждения эндотелия, что обусловливает отсутствие на них наложений тромботических масс. Исходом вальвулита является склероз створок клапана, иногда при рано начатом и адекватном лечении процесс обратим. Сходные изменения, заканчивающиеся склерозом, могут развиваться в сухожильных хордах.
Острый бородавчатый эндокардит протекает с более выраженными фибриноидными изменениями, клеточной реакцией и вовлечением в процесс эндотелия клапанов. При этом образуются мелкие (1—2 мм) тромбы, которые располагаются по замыкающему краю створок в виде бородавок серого цвета.
Фибропластический эндокардит развивается из двух предыдущих форм эндокардита и характеризуется усиленными процессами склероза створок клапанов и их деформацией.
Возвратно-бородавчатый эндокардит возникает при повторных атаках ревматизма на фоне склероза, гиалиноза и деформаций створок клапанов. При этом дезорганизация соединительной ткани происходит как в предсуществующей строме, так и в уже склерозированных тромботических бородавках. В результате на уже склерозированные тромботические массы откладываются новые массы фибрина, которые при затихании процесса также склерозируются.
Осложнения.
Острый бородавчатый и возвратно-бородавчатый эндокардиты могут осложняться тромбоэмболией сосудов большого или малого круга кровообращения. Следствием таких тромбоэмболии являются инфаркты селезенки, почек, головного мозга, миокарда, сетчатки глаза, иногда легких, изредка гангрена кишки или нижних конечностей.
В исходе эндокардита развиваются склероз, гиалиноз и деформация створок клапанов. Часто они срастаются друг с другом, нередко развиваются склероз и петрификация фиброзного кольца. Атриовентрикулярное отверстие обычно резко сужено, имеет вид «рыбьего рта» — формируется порок сердца. Сухожильные хорды также утолщены, укорочены и спаяны друг с другом.
3.4. Классификация
Современная классификация ОРЛ включает:
1. Клинический вариант: острая РЛ (ОРЛ), повторная РЛ (ПРЛ).
2. Клинические проявления: кардит, артрит, хорея, кольцевидная эритема, подкожные узелки.
3. Вовлеченность сердца: без поражения сердца, ревматическая болезнь сердца (без порока, с пороком, неактивная фаза).
4. Выраженность хронической сердечной недостаточности: ХСН I, II A, II Б, III ст., ФК I, II, III, IV.
3.5. Клиника и диагностика
Клинико-диагностические критерии ОРЛ Киселя-Джонса:
I. Большие (ревматическая клиническая пентада):
1) ревмокардит (преимущественно эндомиокардит);
2) полиартрит (преимущественно крупных суставов, мигрирующий характер, без остаточных деформаций, рентгенологически негативный);
3) малая хорея (гипотонико-гиперкинетический синдром вследствие поражения полосатого тела подкорки головного мозга);
4) ревматические узелки (периартикулярные подкожные узловатые уплотнения);
5) анулярная эритема (кольцевидные покраснения кожи туловища и проксимальных отделов конечностей).
1) клинические: лихорадка, артралгии;
2) лабораторно-инструментальные: а) лабораторные (СРБ, СК, ДФА, СМ, АСЛО, АСГН); б) инструментальные (увеличение интервала PQ на ЭКГ)
Дифференциальная диагностика
Наиболее часто приходится дифференцировать ОРЛ с:
1) неревматический кардит (на фоне вирусной инфекции, без временного промежутка, без пороков, без поражения суставов, с отрицательными ревмопробами);
2) ревматоидным артритом (поражаются мелкие суставы, стойкий характер поражения, характерна утренняя скованность, узурация на рентгенограммах, деформация, практически не поражается сердце);
3) СКВ (волчаночная бабочка, панцитопения с нейтрофилезом, LE-клетки и АНФ).
4. Ревматоидный артрит
Ревматоидный артрит (англ. rheumatoid arthritis ) — это системное заболевание соединительной ткани с преимущественным поражением мелких суставов по типу эрозивно-деструктивного полиартрита неясной этиологии со сложным аутоиммунным патогенезом.
Название происходит от (др.-греч. ῥεῦμα ) что значит «течение», суффикс -оидный означает «подобный», ἄρθρον переводится как «сустав» и суффикс —ит (гр. —itis) обозначает «состояние воспаления».
Причины заболевания на сей день неизвестны. Косвенные данные: увеличение количества лейкоцитов в крови и скорости оседания эритроцитов (СОЭ) — указывают на инфекционную природу процесса. Полагают, что заболевание развивается в результате инфекции, вызывающей нарушения иммунной системы у наследственно предрасположенных лиц; при этом образуются так называемые иммунные комплексы (из антител, вирусов и проч.), которые откладываются в тканях и приводят к повреждению суставов. Но неэффективность лечения РА антибиотиками скорее всего свидетельствует о неправильности такого предположения.
Заболевание характеризуется высокой инвалидностью (70 %), которая наступает довольно рано. Основными причинами смерти от заболевания являются инфекционные осложнения и почечная недостаточность.
Лечение сосредотачивается в основном на облегчении боли, замедлении развития заболевания и восстановлении повреждений с помощью хирургического вмешательства. Раннее обнаружение заболевания с помощью современных средств может значительно сократить вред, который может быть нанесён суставам и другим тканям.
Впервые может проявиться после тяжёлой физической нагрузки, эмоционального шока, утомления, в период гормональной перестройки, воздействия неблагоприятных факторов или инфекции.
4.1. История
Самые первые следы ревматоидного артрита найдены в 4500 г. до н. э. Их обнаружили на остатках скелетов индейцев в Теннесси, США. Первый документ, описывающий симптомы, очень напоминающие симптомы ревматоидного артрита, датируется 123 г. Симптомы ревматоидного артрита можно отметить и у людей, изображенных на картинах фламандских художников, например, «Три грации» Рубенса.
Первое описание ревматоидного артрита как самостоятельной нозологической формы (под названием первичной астенической подагры — la goutte asthénique primitive) выполнено в 1800 г. О.Ж.Ландре-Бове по результатам наблюдений в госпитале Сальпетриер под руководством Ф.Пинеля. Заболевание получило своё современное имя в опубликованном 1859 г. «Трактате о природе и лечении подагры и ревматической подагры» А.Б.Гарро.