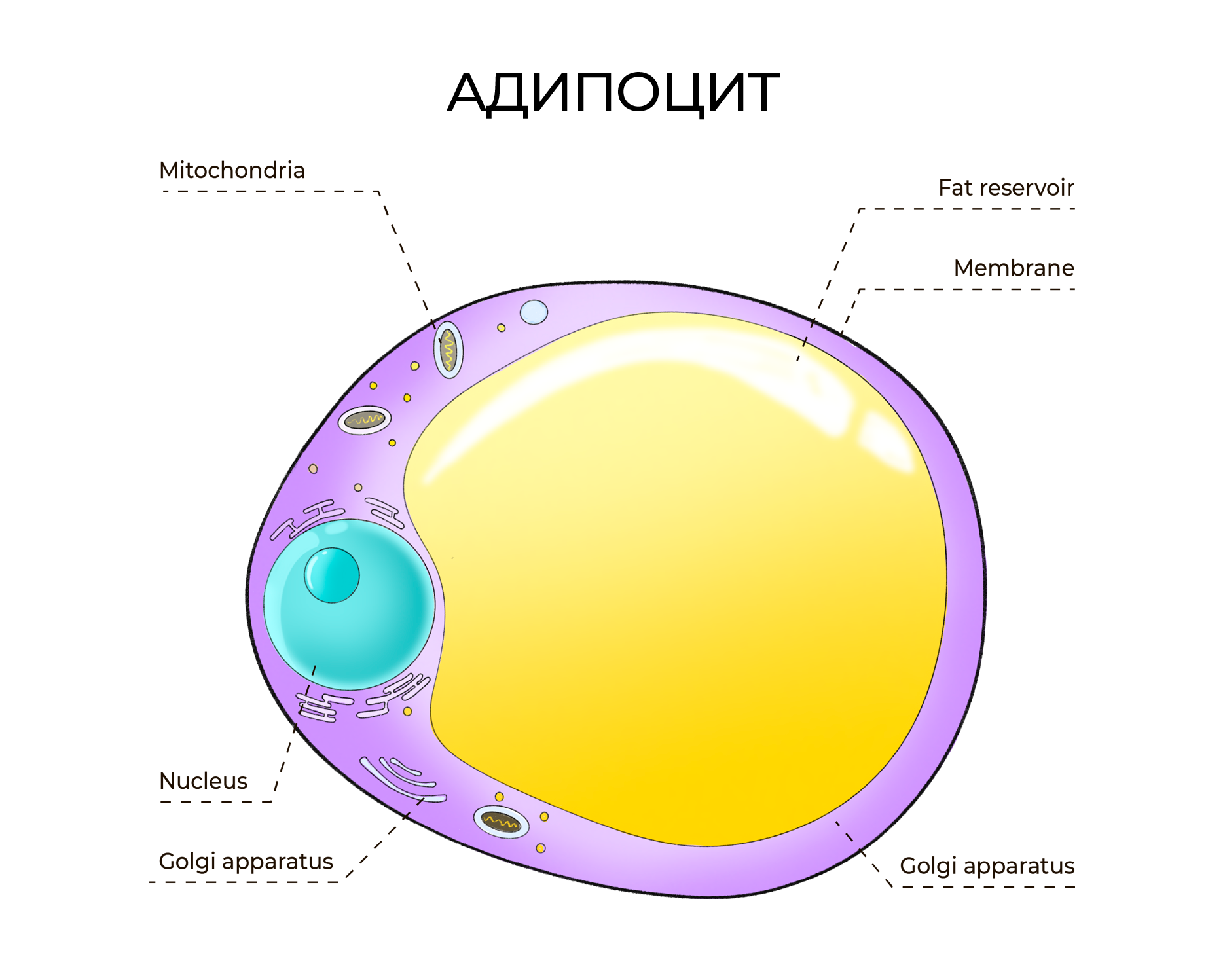
какие жировые клетки составляют основу гиподермы
Кожа под микроскопом: гиподерма
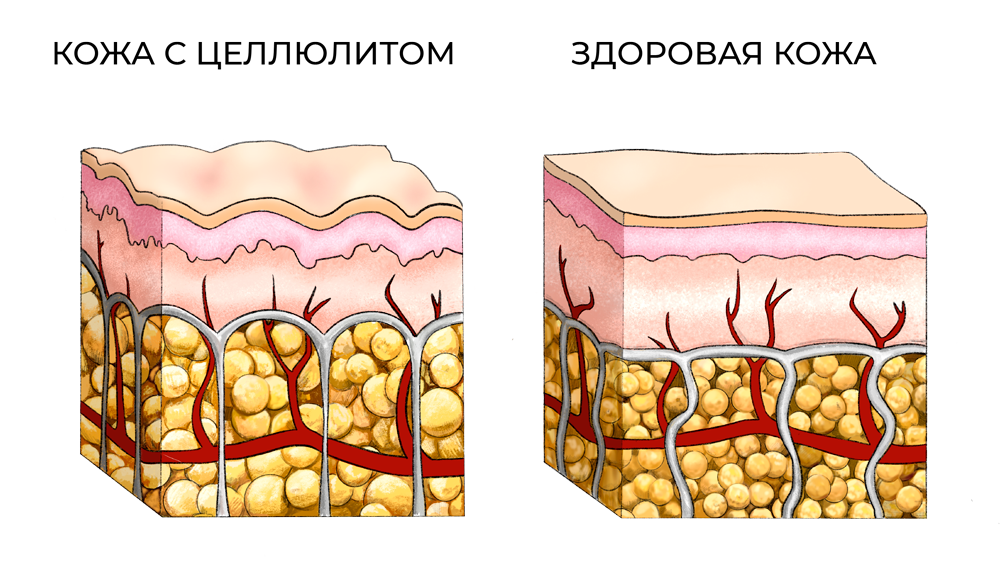
Гиподерма — это наше главное хранилище жировых запасов и именно здесь зарождается целлюлит. Но не спешите проникаться враждебными чувствами к гиподерме.
На самом деле, без подкожно-жировой клетчатки мы бы представляли собой очень жалкое зрелище. Ведь именно жир придает нашим формам аппетитную округлость, а коже – свежесть и гладкость. Дистрофия жировой ткани, и связанные с ней потери объема — одна из основных причин ухудшения внешнего вида.
Кроме того гиподерма делает еще множество других добрых дел для нашего организма.
АНАТОМИЯ И СТРОЕНИЕ
Толщина этого подкожного слоя варьируется по всему телу, а также различаются по полу. Он наиболее толстый в ягодицах, ладонях и подошвах ног. Размер адипоцитов определяется пищевыми привычками человека.
ГИПОДЕРМА И СТАРЕНИЕ
В связи с уменьшением коллагена и локальным изменением жировой ткани приводит к образованию морщин.
Если дерму мы сравнивали с матрасом, то подкожно-жировая клетчатка больше всего похожа на соты, где вместо меда — жировые клетки адипоциты.
Количество этих клеток заложено генетически и у всех людей разное. Ни одна диета на свете, к сожалению, не поможет вам избавиться хотя бы от пары-тройки адипоцитов. Зато увеличить армию жировых клеток вполне в наших силах: от переизбытка калорий они будут пухнуть и пухнуть, пока не достигнуть критической отметки (адипоцит может увеличиться в 27 раз!). И вот тогда на сцену выходят преадипоциты — командиры, которые дают сигнал к размножению жировых клеток.
И процесс этот невозможно повернуть вспять — все новоприбывшие клетки теперь тоже будут жить с вами и при любой возможности (читай: избытке калорий в целом и жира из пищи в частности) увеличиваться в размерах. И даже если вы похудеете, количество и размер самих адипоцитов останется прежним. Вот такая вот печаль и одновременно мотивация всегда следить за питанием!
ОТКУДА БЕРЕТСЯ ЦЕЛЛЮЛИТ
Предполагается, что основным толчком к развитию целлюлита (гиноидной липодистрофии) является наращения метаболизма жиров (химическая трансформация жиров и их введения в систему кровообращения происходит через клетки жировой ткани — адипоциты), сопровождающиеся увеличением количества и размеров жировых клеток. Это приводит к ослаблению механических свойств капилляров, нарушению нормальной циркуляции крови и лимфе в гиподерме и эксудации (выход жидкой части крови через сосудистую стенку в воспаленную ткань). Так же происходит изменение в строение коллагена (нерегулярный переход коллагенового матрикса между дермой и гиподермой с разрывами на границе и протрузиями жировой ткани в дерму).
На оболочке жировых клеток находятся два типа рецепторов:
Для уменьшения выраженности целлюлита необходимо работать с бета-рецепторами
Толщина гиподермы варьируется от 2 мм до доброго десятка сантиметров на бедрах и ягодицах. Совсем отсутствует подкожно-жировая клетчатка на веках, губах и шее. Так что как бы не хотелось потолстеть в губах вместо живота, это не получится
Если у Вас остались или появились вопросы, не стесняйтесь и задавайте их под последним постом в Instagram,
а также подписывайтесь на Telegram-канал.
Кожа под микроскопом. Слои и их строение.
Строение кожи
Основа всех основ для любого косметолога. Знание строения, функций и клеток кожи необходимо для эффективной работы с пациентами.
Кожа является самым большим органом нашего тела, которая выполняет множество важнейших функций:
Сама кожа делится на три слоя: эпидермис, дерму и гиподерму. Каждый слой отличается по строению и функциям. Рассмотрим каждый из них.
Эпидермис
Самый верхний слой кожи, представляющий собой типичную пролиферативную ткань, которая способна к постоянному самообновлению. Эпидермис в свою очередь делится еще на 5 уровней: роговой, блестящий, зернистый, шиповатый, базальный.
Роговой слой
Является внешним слоем эпидермиса. В нем содержится от 15 до 30 слоев клеток, выполняющих защитные функции. Роговой слой – это конечный продукт процесса дифференцировки клеток. Прочность рогового слоя обусловлена качеством кератина и наличием межклеточного диффузионного барьера. Целостность и качество рогового слоя сильно зависит от pH. Воздействие на pH-градиент рогового слоя может привести к изменению активности ферментов, что влечет за собой нарушения во всем эпидермисе.
Блестящий слой
Идет сразу после рогового. Это очень тонкий слой безядерных клеток, которые пропитаны особым веществом – элеидином.
Зернистый слой
Состоит 3-4 слоев клеток, в которых скапливаются нити кератина (строительный материал рогового слоя). Здесь кератиноциты производят липиды и компоненты, составляющие NMF (естественный увлажняющий фактор).
Шиповидный слой
Состоит из 4-8 рядов полигональных клеток, которые соединены прочной связью протоплазматических отростков. Слой получил свое название благодаря шиповатым клеткам, которые имеют в своем составе артефакт, возникающий при гистологической обработке образцов ткани. В клетках шиповидного слоя откладываются продукты синтеза, такие как кератин и липиды. Здесь же располагаются иммунологически активные клетки Лангерганса.
Базальный слой
Состоит из коллагеновых и эластиновых волокон, а также из протоплазматических отростков эпителиальных клеток. В базальном слое расположены меланоциты, несущие в меланосомах запасы пигмента. Каждый меланоцит контактирует приблизительно с 30 кератиноцитами через разветвлённые дендриты и поставляет им пигмент. Таким способом меланоциты защищают кожу от негативного воздействия УФ-излучения. Базальной слой контактирует с дермой и, следовательно, с зоной дермо-эпидермального соединения.
Дерма и гиподерма
Глубже эпидермиса находится дерма, имеющая толщину от 1.5 до 5 мм. Она состоит из двух слоев: сосочкового и сетчатого. Дерма пронизана кровеносными и лимфатическими сосудами, железами.
Сосочковый слой
Представляет собой рыхлую волокнистую соединительную ткань, которая состоит из коллагеновых, эластических и ретикулярных волокон, а также из клеток: фибробластов, тучных клеток, макрофагов и других. Сосочковый слой получил свое название благодаря большому количеству сосочков, вдающихся в эпителий. Размер и количество сосочков по всему тело неодинаково. В дерме лица сосочки совсем плохо развиты и с возрастом имеют тенденцию исчезать.
Также в этом слое находятся гладкие мышечные клетки, которые собираются в пучки, связанные с корнем волоса. Здесь же происходит процесс появления «гусиной кожи», когда сокращаются мышечные клетки. При этом снижается теплоотдача организма, так как мелкие кровеносные сосуды сжимаются, тем самым уменьшая приток крови к коже.
Сетчатый слой
Состоит из плотной соединительной ткани с пучками коллагеновых волокон и сетью эластических волокон. Коллагеновые волокна проходят в двух направлениях: параллельно и косо к поверхности кожи. В сетчатом слое дермы на участках кожи, подверженных сильному растяжению, располагается узкопетлистая коллагеновая сеть. В зонах, где кожа испытывает особое давление, коллагеновая сеть является широкопетлистой. Сеть эластических волокон повторяет расположение коллагеновых пучков. В сетчатом слое фибробласты являются основными клеточными элементами. Кроме этого, в сетчатом слое располагаются кожные железы: потовые и сальные, а также корни волос.
Гиподерма или подкожная жировая клетчатка образуется из соединительнотканных фиброзных тяжей, которые образуют ячейки, наполняющиеся жировой тканью. Жировая ткань состоит из адипоцитов (жировых клеток). В фиброзных тяжах располагаются лимфатические сосуды, нервы, малые артерии, венулы и артериолы. Гиподерма в некоторых областях тела человека отсутствует, например, ее нет в области век, в мошонке и на половом члене. Слой подкожной жировой клетчатки обуславливает подвижность и тургор кожи, принимает участие в жировом обмене организма, является жировым депо и амортизатором внешних механических воздействий. Важно понимать, что ПЖК является сложным органом с важными метаболическими и эндокринными функциями в организме человека.
Источники:
Н.В.Чеботарева. Настольная книга косметолога.
Какие жировые клетки составляют основу гиподермы
Анатомия и физиология кожи
Кожа – наш самый большой орган, составляющий 15% от общей массы тела. Она выполняет множество функций, прежде всего защищает организм от воздействия внешних факторов физической, химической и биологической природы, от потери воды, участвует в терморегуляции. Последние научные данные подтверждают, что кожа не только обладает собственной иммунной системой, но и сама является периферическим иммунном органом.
Структура кожи
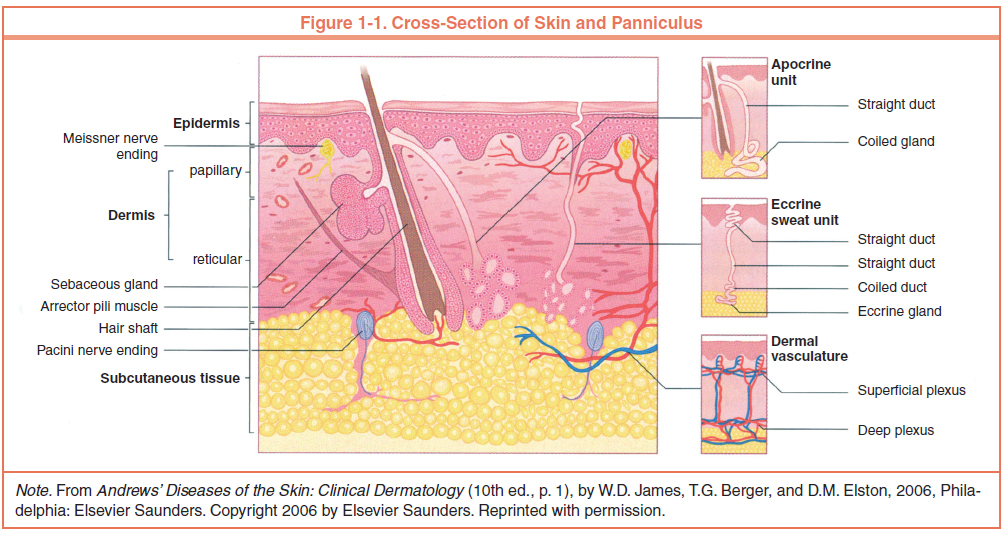
Кожа состоит из 3 слоев: эпидермиса, дермы и подкожной жировой клетчатки (ПЖК) (рис. 1). Эпидермис – самый тонкий из них, представляет собой многослойный ороговевающий эпителий. Дерма – средний слой кожи. Главным образом состоит из фибрилл структурного белка коллагена. ПЖК содержит жировые клетки – адипоциты. Толщина этих слоев может значительно варьировать в зависимости от анатомического места расположения.
Эпидермис
Кератинизация. По мере дифференцировки кератиноцитов и продвижения от базального слоя до рогового происходит их кератинизация (ороговевание) – процесс, начинающийся с фазы синтеза кератина кератиноцитами и заканчивающийся их клеточной деградацией. Кератин служит строительным блоком для промежуточных филаментов. Пучки из этих филаментов, достигая цитоплазматический мембраны, формируют десмосомы, необходимые для образования прочных контактов между соседними клетками. Далее, по мере процесса эпителиальной дифференцировки, клетки эпидермиса вступают в фазу деградации. Ядра и цитоплазматические органеллы разрушаются и исчезают, обмен веществ прекращается, и наступаетапоптозклетки, когда она полностью кератинизируется (превращается в роговую чешуйку).
Базальный слой эпидермиса состоит из одного ряда митотически активных кератиноцитов, которые делятся в среднем каждые 24 часа и дают начало новым клеткам новым клеткам вышележащих эпидермальных слоев. Они активируются только в особых случаях, например при возникновении раны. Далее новая клетка, кератиноцит, выталкивается в шиповатый слой, в котором она проводит до 2 недель, постепенно приближаясь к гранулярному слою. Движение клетки до рогового слоя занимает еще 14 дней. Таким образом, время жизни кератиноцита составляет около 28 дней.
Надо заметить, что не все клетки базального слоя делятся с такой скоростью, как кератиноциты. Эпидермальные стволовые клетки в нормальных условиях образуют долгоживущую популяцию с медленным циклом пролиферации.
Шиповатый слой эпидермиса состоит из 5-10 слоев кератиноцитов, различающихся формой, структурой и внутриклеточным содержимым, что определяется положением клетки. Так, ближе к базальному слою, клетки имеют полиэдрическую форму и круглое ядро, но по мере приближения клеток к гранулярному слою они становятся крупнее, приобретают более плоскую форму, в них появляются ламеллярные гранулы, в избытке содержащие различные гидролитические ферменты. Клетки интенсивно синтезируют кератиновые нити, которые, собираясь в промежуточные филаменты, остаются не связанными со стороны ядра, но участвуют в образовании множественных десмосом со стороны мембраны, формируя связи с соседними клетками. Присутствие большого количества десмосом придает этому слою колючий вид, за что он и получил название «шиповатый».
Зернистый слой эпидермиса составляют еще живые кератиноциты, отличающиеся своей уплощенной формой и большим количеством кератогиалиновых гранул. Последние отвечают за синтез и модификацию белков, участвующих в кератинизации. Гранулярный слой является самым кератогенным слоем эпидермиса. Кроме кератогиалиновых гранул кератиноциты этого слоя содержат в большом количестве лизосомальные гранулы. Их ферменты расщепляют клеточные органеллы в процессе перехода кератиноцита в фазу терминальной дифференцировки и последующего апоптоза. Толщина гранулярного слоя может варьировать, ее величина, пропорциональная толщине вышележащего рогового слоя, максимальна в коже ладоней и подошв стоп.
Блестящий слой эпидермиса (назван так за особый блеск при просмотре препаратов кожи на световом микроскопе) тонкий, состоит из плоских кератиноцитов, в которых полностью разрушены ядра и органеллы. Клетки наполнены элейдином – промежуточной формой кератина. Хорошо развит лишь на некоторых участках тела – на ладонях и подошвах.
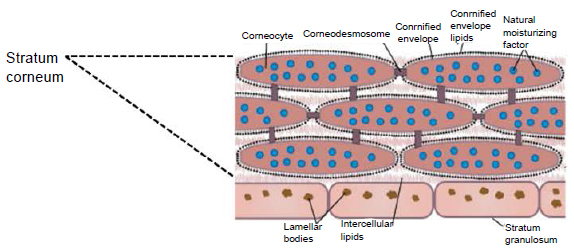
Роговой слой эпидермиса представлен корнеоцитами (мертвыми, терминально-дифференцированными кератиноцитами) с высоким содержанием белка. Клетки окружены водонепроницаемым липидным матриксом, компоненты которого содержат соединения, необходимые для отшелушивания рогового слоя (рис. 3). Физические и биохимические свойства клеток в роговом слое различаются в зависимости от положения клетки внутри слоя, направляя процесс отшелушивания наружу. Например, клетки в средних слоях рогового слоя обладают более сильными водосвязывающими свойствами за счет высокой концентрации свободных аминокислот в их цитоплазме.
Дерма
Дерма представляет собой сложноорганизованную рыхлую соединительную ткань, состоящую из отдельных волокон, клеток, сети сосудов и нервных окончаний, а также эпидермальных выростов, окружающих волосяные фолликулы и сальные железы. Клеточные элементы дермы представлены фибробластами, макрофагами и тучными клетками. Лимфоциты, лейкоциты и другие клетки способны мигрировать в дерму в ответ на различные стимулы.
Дерма, составляя основной объем кожи, выполняет преимущественно трофическую и опорную функции, обеспечивая коже такие механические свойства, как пластичность, эластичность и прочность, необходимые ей для защиты внутренних органов тела от механических повреждений. Также дерма удерживает воду, участвует в терморегуляции и содержит механорецепторы. И, наконец, ее взаимодействие с эпидермисом поддерживает нормальное функционирование этих слоев кожи.
В дерме нет такого направленного и структурированного процесса клеточной дифференцировки, как в эпидермисе, тем не менее в ней также прослеживается четкая структурная организация элементов в зависимости от глубины их залегания. И клетки, и внеклеточный матрикс дермы также подвергаются постоянному обновлению и ремоделированию.
Коллаген – один из главных компонентов ВКМ дермы. Синтезируется фибробластами. Процесс его биосинтеза сложный и многоступенчатый, в результате которого фибробласт секретирует в экстрацеллюлярное пространство проколлаген, состоящий из трех полипептидных α-цепей, свернутых в одну тройную спираль. Затем мономеры проколлагена ферментивным путем собираются в протяженные фибриллярные структуры различного типа. Всего в коже не менее 15 типов коллагена, в дерме больше всего I, III и V типов этого белка: 88, 10 и 2% соответственно. Коллаген IV типа локализуется в зоне базальной мембраны, а коллаген VII типа, секретируемый кератиноцитами, играет роль адаптерного белка для закрепления фибрилл ВКМ на базальной мембране (рис. 4). Волокна структурных коллагенов I, III и V типов служат каркасом, к которому присоединяются другие белки ВКМ, в частности коллагены XII и XIV типов. Считается, что эти минорные коллагены, а также небольшие протеогликаны (декорин, фибромодулин и люмикан) регулируют формирование структурных коллагеновых волокон, их диаметр и плотность образуемой сети. Взаимодействие олигомерных и полимерных комплексов коллагена с другими белками, полисахаридами ВКМ, разнообразными факторами роста и цитокинами приводит к образованию особой сети, обладающей определенной биологической активностью, стабильностью и биофизическими характеристиками, важными для нормального функционирования кожи. В папиллярном слое дермы волокна коллагена располагаются рыхло и более свободно, тогда как ее ретикулярный слой содержит более крупные тяжи коллагеновых волокон.
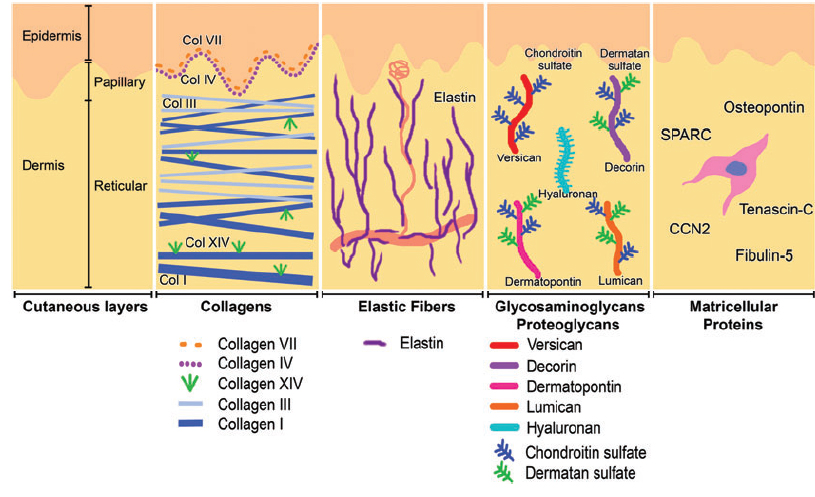
Коллаген постоянно обновляется, деградируя под действием протеолитических ферментов коллагеназ и замещаясь вновь синтезированными волокнами. Этот белок составляет 70% сухого веса кожи. Именно коллагеновые волокна «держат удар» при механическом воздействии на нее.
Эластин формирует еще одну сеть волокон в дерме, наделяя кожу такими качествами, как упругость и эластичность. По сравнению с коллагеном эластиновые волокна менее жесткие, они скручиваются вокруг коллагеновых волокон. Именно с эластиновыми волокнами связываются такие белки, как фибулины и фибриллины, с которыми, в свою очередь, связывается латентный TGF-β-связывающий белок (LTBP). Диссоциация этого комплекса приводит к высвобождению и к активации TGF-β, самого мощного из всех факторов роста. Он контролирует экспрессию, отложение и распределение коллагенов и других матриксных белков кожи. Таким образом, интактная сеть из волокон эластина служит депо для TGF-β.
ГК с легкостью образует вторичные водородные связи и внутри одной молекулы, и между соседними молекулами. В первом случае они обеспечивают формирование относительно жестких спиральных структур. Во втором – происходит ассоциация с другими молекулами ГК и неспецифическое взаимодействие с клеточными мембранами, что приводит к образованию сети из полимеров полисахаридов с включенными в нее фибробластами. На длинную молекулу ГК, как на нить, «усаживаются» более короткие молекулы протеогликанов (версикана, люмикана, декорина и др.), формируя агрегаты огромных размеров. Протяженные во всех направлениях, они создают каркас, внося вклад в стабилизацию белковой сети ВКМ и фиксируя фибробласты в определенном окружении матрикса. В совокупности все эти свойства ГК наделяют матрикс определенными химическими характеристиками – вязкостью, плотностью «ячеек» и стабильностью. Однако сеть ВКМ является динамической структурой, зависящей от состояния организма. Например, в условиях воспаления агрегаты ГК с протеогликанами диссоциируют, а образование новых агрегатов между вновь синтезированными молекулами ГК (обновляющимися каждые 3 дня) и протеогликанами блокируется. Это приводит к изменению пространственной структуры матрикса: увеличивается размер его ячеек, меняется распределение всех волокон, структура становится более рыхлой, клетки меняют свою форму и функциональную активность. Все это сказывается на состоянии кожи, приводя к снижению ее тонуса.
Помимо регуляции водного баланса и стабилизации ВКМ, ГК выполняет важную регуляторную роль в поддержании эпидермального и дермального гомеостаза. ГК активно регулирует динамические процессы в эпидермисе, включая пролиферацию и дифференцировку кератиноцитов, окислительный стресс и воспалительный ответ, поддержание эпидермального барьера и заживление раны. В дерме ГК также регулирует активность фибробластов и синтез коллагена. Ремоделируя матрикс, ГК управляет функционированием клеток в матриксе, влияя на их доступность для различных факторов роста и изменяя их функциональную активности. От действия ГК зависит миграция клеток и иммунный ответ в ткани. Таким образом, изменения в распределении, организации, молекулярном весе и метаболизме ГК имеют значимые физиологические последствия.
Фибробласты представляют собой основной тип клеточных элементов дермы. Именно эти клетки отвечают за продукцию ГК, коллагена, эластина, фибронектина и многих других белков межклеточного матрикса, необходимых для формирования соединительной ткани. Фибробласты в различных слоях дермы различаются и морфологически, и функционально. От глубины их залегания в дерме зависит не только количество синтезируемого ими коллагена, но и соотношение типов этого коллагена, например I и III типов, а также синтез коллагеназы: фибробласты более глубоких слоев дермы производят меньшее ее количество. Вообще, фибробласты – очень пластичные клетки, способные менять свои функции и физиологический ответ и даже дифференцироваться в другой тип клеток в зависимости от полученного стимула. В роли последнего могут выступать и сигнальные молекулы, синтезированные соседними клетками, и перестройка окружающего ВКМ.
Подкожно-жировая клетчатка
Какие жировые клетки составляют основу гиподермы
Челябинский областной клинический онкологический диспансер
Кафедра пластической и эстетической хирургии, косметологии и клеточных технологий ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздравсоцразвития России
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
МАУЗ ОЗП «Городская клиническая больница», Челябинск, Россия
Биологическая характеристика жировой ткани
Журнал: Пластическая хирургия и эстетическая медицина. 2019;(2): 33-42
Васильев В. С., Мантурова Н. Е., Васильев С. А., Терюшкова Ж. И. Биологическая характеристика жировой ткани. Пластическая хирургия и эстетическая медицина. 2019;(2):33-42.
Vasil’ev V S, Manturova N E, Vasil’ev S A, Teryushkova Zh I. Biological features of adipose tissue. Plastic Surgery and Aesthetic Medicine. 2019;(2):33-42.
https://doi.org/10.17116/plast.hirurgia201902133
Челябинский областной клинический онкологический диспансер
Жировая ткань представляет собой биологически активную субстанцию. Помимо депонирования энергетических запасов и участия в формировании контуров тела, определяющих внешний вид человека, жировая ткань является ключевым компонентом системы терморегуляции, оказывает регулирующее влияние на иммунную систему, секретирует большое количество биологически активных веществ. Жировая ткань является динамически функционирующим эндокринным органом, высвобождающим ряд гормонов, напрямую взаимодействующих с гипоталамусом. Стволовые клетки жировой ткани обладают высоким дифференцировочным потенциалом. Они могут дифференцироваться в клетки хрящевой, нервной, костной, мышечной, кардиальной, сосудистой, эндокринной, печеночной, гемопоэтической тканей. Эти свойства стволовых клеток жировой ткани открывают широкие возможности их клинического применения не только по косметическим, но и по реконструктивным показаниям. Доступность жировой ткани для забора из организма человека позволяет рассматривать ее в качестве перспективного субстрата для регенеративной медицины и тканевой инженерии.
Челябинский областной клинический онкологический диспансер
Кафедра пластической и эстетической хирургии, косметологии и клеточных технологий ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздравсоцразвития России
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
МАУЗ ОЗП «Городская клиническая больница», Челябинск, Россия
Введение
Жировая ткань является биологической субстанцией, вызывающей всевозрастающий научный интерес. В течение продолжительного времени функция жировой ткани сводилась к сохранению энергетических запасов организма, получаемых с пищей. Однако оказалось, что жировая ткань секретирует молекулы, напрямую взаимодействующие с головным мозгом, и является компонентом иммунной системы. Эта ткань формирует форму человеческого организма, определяя сексуальную привлекательность, тем самым выполняя еще и социальную функцию. Большинство исследований жировой ткани было проведено на животных, что не позволяет экстраполировать эти данные на человека. Доступность жировой ткани для забора из организма человека открывает широкие возможности ее применения в качестве субстрата для клеточной терапии по различным показаниям.
Различают две разновидности жировой ткани человека: коричневую жировую ткань (brown adipose tissue — BAT) — КЖТ и белую жировую ткань (white adipose tissue — WAT) — БЖТ. Эти две разновидности выполняют различные функции, но по содержанию запасов итрацеллюлярного триглицерида относятся к жировой ткани [1, 2]. КЖТ участвует в механизме выработки энергии для организма, в то время как БЖТ имеет несколько функций: обеспечение термосбережения; определение формы тела, что особенно важно для сексуальной привлекательности женщин; сбережение энергии; амортизация при механических ударах; выполнение эндокринной функции; заполнение свободных пространств организма; облегчение скольжения мышц при их движении. КЖТ и БЖТ обычно не имеют четких границ, а существуют в виде смешанной субстанции [1, 3]. У женщин и мужчин с нормальной комплекцией жировая ткань составляет 22 и 15% от массы тела соответственно. Жировая ткань широко распространена по всему организму, при этом существуют различия в ее распределении у мужчин и женщин. Количество жировой ткани в организме может изменяться в зависимости от особенностей питания и энергозатрат. При поступлении в организм избыточной энергии жировая ткань может образовывать вокруг кровеносных сосудов недифференцированные клетки. На начальной стадии адипогенеза клетки не содержат жировых включений. Затем в стадии жировой пролиферации происходит аккумуляция жира, и преадипоциты дифференцируются в адипоциты с формированием островков жировой ткани. Если адипоцит теряет свою массу (в результате голодания и потери массы тела), клетка становится морфологически неравномерной, с увеличенными митохондриями в цитоплазме. Эти потерявшие жировое наполнение адипоциты (постадипоциты) окружены плотным коллагеновым матриксом, который может вызвать фиброз жировой ткани. Дольки жировой ткани окружаются соединительной тканью с формированием капсулы. Коллагеновая фрагментация продолжается до тех пор, пока каждый адипоцит не будет окружен коллагеновым матриксом (scaffold). Соединительнотканные перегородки внедряются в жировую ткань и разделяют ее на несколько более мелких фрагментов [1, 3].
Жировая ткань имеет два типа нервных волокон: симпатические и чувствительные. Доказано, что симпатическая иннервация подавляет увеличение количества жировых клеток. Это может служить подтверждением связи некоторых синдромов ожирения со сниженной симпатической иннервацией [1, 3]. У мышей и крыс не обнаружено парасимпатической иннервации жировой ткани [4]. Прямая нейронная связь между паравентрикулярными ядрами гипоталамуса и жировой тканью установлена только в придатке яичка [5]. Такая же прямая гипоталамическая связь существует с печенью, что может обеспечивать контроль за метаболическими процессами в организме. Если учесть, что гипоталамус имеет множественные нейронные связи с другими отделами головного мозга, можно понять возможность непредсказуемых биологических взаимодействий. В межлопаточной области хомяков обнаружены прямые нейронные пути между центральной нервной системой и КЖТ. Нейроны средней преоптической области, гипоталамические ядра, вентромедиальные гипоталамические ядра, супрахиазматические и латеральные гипоталамические ядра соединяются с межлопаточной КЖТ через пути спинномозговых волокон, а также со стволом головного мозга, средним и передним мозгом [2].
В зависимости от анатомической локализации жировая ткань демонстрирует различные свойства. Основная масса ткани локализуется в двух отделах: подкожном слое и сальнике. Этот массив ткани легко увеличивается или уменьшается в зависимости от питания. Половые различия также влияют на количество и распределение жировой ткани. В то же время некоторые фрагменты жировой ткани, такие как периокулярные, ладонные, подошвенные, не вовлечены в метаболический процесс организма и их масса не изменяется даже в результате строгого поста. [1, 3]. Самые маленькие адипоциты, которые располагаются в брыжейке, наименее чувствительны к адреналину. Жировая ткань брыжейки имеет более богатые иннервацию и кровоснабжение. Кровоснабжение жировой ткани меняется в зависимости от индекса массы тела (ИМТ). Сердечный выброс в жировую ткань варьирует от 3—7% у худых людей, до 15—30% — при выраженном ожирении. Такое увеличение сердечного выброса может вызывать гемодинамические эффекты с возможным развитием кардиомегалии и выраженной сердечной недостаточности. Процентное содержание макрофагов в ткани также зависит от ИМТ: с увеличением массы тела увеличивается количество макрофагов, которые фагоцитируют жировые фрагменты погибших адипоцитов.
Адипоциты БЖТ содержат одну большую каплю жира в каждой клетке. Эта капля не имеет четкой дифференцировки, но у нее есть однослойная мембрана, отделяющая ее от цитоплазмы. Клетки бывают круглой или полигональной формы, и их размер варьирует от 25 до 200 мкм. Они содержат много органелл, однако трудноразличимы на фоне крупного жирового фрагмента, который выдавливает внутриклеточные структуры вместе с ядром к периферии, где они находятся в тонкой прослойке цитоплазмы под плазмолеммой. В процессе гистологической обработки жировой фрагмент исчезает, оставляя пустое пространство, которое под микроскопом визуализируется как кольцо. Большое скопление пиноцитотических везикул расположено возле плазматической мембраны. Для прокраски адипоцитов используют Sudan III или Scarlet Red staining. БЖТ содержит множество сосудов, обычно каждый адипоцит контактирует с кровеносным сосудом. Жировая ткань представлена зрелыми адипоцитами, преадипоцитами, постадипоцитами, мезенхимальными стволовыми клетками, клетками эндотелия, перицитами, мастовскими клетками, макрофагами, фибробластами, циркулирующими кровяными клетками, ретикулоцитами, нервными клетками. При этом зрелые адипоциты составляют ½ всей клеточной популяции.
КЖТ относят к жировой ткани, поскольку ее клетки содержат в цитоплазме триглицеридные депозиты. Коричневый цвет этой ткани обусловлен высоким содержанием цитохромной оксидазы в митохондриях, которая в избыточном количестве находится в цитоплазме. Различают две разновидности клеток КЖТ. Первая популяция эмбриологически образуется из того же источника, что и мышечные клетки, и составляет основу всех классических депозитов КЖТ. Вторая популяция формируется из клеток БЖТ [6] и распределяется среди белых жировых клеток, поэтому именуется как «коричневая в белом» («beige or brite»). Анатомическое распределение КЖТ и БЖТ различно. В течение первых 10 лет человеческой жизни КЖТ можно обнаружить практически в тех же местах, где находится БЖТ, например в межлопаточной области и на передней брюшной стенке. Однако с течением времени КЖТ исчезает из периферических отделов и концентрируется во внутренних отделах организма: в средостении, вокруг почек, надпочечников, аорты, сохраняясь там вплоть до восьмой декады жизни. Результаты недавних исследований, включающих 3604 пациента и основанных на исследовании 18F-FDG-PET/CT, показали, что объем и активность КЖТ более выражены у женщин. Мужской организм с возрастом теряет объем и активность КЖТ. Предполагается, что это связано с гормональными различиями, а именно — тестостероновой ингибицией экспрессии UCP1 mRNA в дозозависимом порядке. Коричневые адипоциты имеют полигональную или эллипсовидную форму, их диаметр варьирует от 15 до 50 мк. Большое количество жировых капель различных размеров располагается в цитоплазме, что придает адипоцитам мультиокулярый вид [2]. КЖТ продуцирует тепло (термогенезис), которое распространяется по всему организму за счет циркуляции крови. Регуляция термогенеза в основном осуществляется гипоталамусом. Поступающие от гипоталамуса сигналы вызывают высвобождение норэпинефрина, который индуцирует метаболизм жировых кислот в митохондриях коричневых адипоцитов. Выработка тепла происходит за счет функционирования высвобожденного протеина 1 (UCP1) во внутренней мембране митохондрий. Этот протеин в литературе также называют «термогенин». Он присутствует только в клетках КЖТ, являясь их маркером. UCP1 активируется в присутствии свободных жировых кислот, высвобождаемых из триглицеридов в результате воздействия неэпинефрин-активированных β-адренергических рецепторов, и подавляет генерацию АТФ в процессе оксидирования жира. В результате свободная энергия выделяется в виде тепла. Механизм выработки тепла до сих пор изучается. UCP1 скорее всего является переносчиком триглицеридов, а не протонов. Свободные протоны выбрасываются в цитоплазму из митохондрий, где они соединяются с жировыми кислотами, переводя их в растворимое состояние. Эти растворимые жировые кислоты возвращаются в митохондрии. При этом (согласно концепции расщепления) протоны не используются для продукции АТФ, а тепло генерируется за счет высвобождения протонов. Таким образом, жировые кислоты вновь переходят в нерастворимое состояние и транспортируются в цитоплазму с помощью UCP1. Остаточные продукты оксигенированного жира, вероятно, подавляют активность UCP1. КЖТ иннервируется симпатическими нервными волокнами. Выработка тепла зависит от особенностей воздействия секретируемого из нервной ткани норэпинефрина на рецепторы КЖТ. При активации β3-рецепторов происходит активация термогенеза, а при активации β2-рецепторов — его ингибиция. Хотя очевидно, что механизм терморегуляторного баланса существует, однако он нуждается в дальнейшем изучении. Сигналы от кожных терморецепторов по нервным путям поступают в ростральный отдел гипоталамуса, который является предмозговым центром системы КЖТ-терморегуляции [1, 3]. Помимо термогенерирующей функции, коричневые адипоциты секретируют ряд молекулярных элементов, а именно компоненты экстрацеллюлярного матрикса (ЭЦМ) (collagen IV, laminin, heparan sulphate, proteoglycan, fibronectin), аутокринные молекулы (adipsin, FGF-2, IGF-I, prostaglandins E2, prostaglandin Fa, adenosine), паракринные молекулы (NGF, VEGF-A, VEGF-B, VEGF-C, nitric oxide, angiotensinogen), эндокринные молекулы (fatty acids, leptin, adiponectin).
ЭЦМ жировой ткани представлен коллагеновыми, ретикулярными, эластическими волокнами, сосудами, стромальной и лимфатической системой. ЭЦМ ткани очень важен для выживания зрелых адипоцитов, включающих большие жировые капли. Масса этих жировых капель намного превышает массу остальных структур клетки, поэтому механическая поддержка ЭЦМ предохраняет клетки от разрушения [7]. Кроме того, сама архитектура ЭЦМ перераспределяет векторы давления окружающих тканевых структур, что также снижает опасность разрушения [8]. ЭЦМ можно разделить на две части: базальную мембрану и межклеточную субстанцию. Каждый адипоцит имеет свою собственную базальную мембрану, состоящую из сети коллагеновых волокон 4-го типа, пластинки, гепарансульфат полигликана (heparan sulphate proteoglycan), перликана и энтактина. Основным компонентом межклеточной субстанции является коллаген 6-го типа [7]. Детальное рассмотрение этого протеина необходимо для лучшего понимания специфики жировой ткани.
Жировая ткань не только выполняет депонирующую функцию, но также является эндокринным органом [9]. Это ткань состоит из адипоцитов, преадипоцитов, фибробластов, стромально-васкулярных клеток, мастовских клеток, и все эти клетки секретируют биологические молекулы и могут вырабатывать как однотипные, так и дифференцированные вещества. При этом один секретируемый продукт может вырабатываться только строго определенным типом клеток, в то время как другой — тремя или четырьмя типами. Постоянная миграция макрофагов и мастовских клеток приводит к изменению общего количества клеток, что затрудняет оценку секретирующей функции жировой ткани. На существующий в БЖТ клеточный трафик влияет целый ряд параметров. Секретируемые жировой тканью продукты могут быть классифицированы в зависимости от их специфики следующим образом: компоненты ЭЦМ (collagen I, III, VI, V, laminin, heparan sulphate, proteoglycan, perlecan, entactin), аутокринные (glycerol, NEFA, monoglyceride, eicosanoids, oleoyl-esttrone, prostagalandin E2, I2, lipoprotein lipase, acylation-stimulating protein, fasting-induced adipose factor, cholestery1 ester transfer protein, tumor necrosis factor a, interleukin-6, complement components, angiotensinogen, VEGF, metalloproteinase inhibitors, matrix metalloproteinases, secreted protein acidic), паракринные (NEFA, monoglyceride, eicosanoids, oleoy1-estrone, prostaglandin E2,12, acylation-stimulating protein, fasting-induced adipose factor, cholesteryl ester transfer protein, tumor necrosis factor α, interleukin-6, IL-1β, IL-8, IL-10, IL-18, IL-17D, transforming growth factor-β, monocyte chemoattractant protein 1, macrophage migration inhibiting factor, complement components, haptoglobin, serum amyloid A3, plasmogen activator inhibitor-1, angeotensinigen, pigment epithelian-derived factor, adrenomedullin, VEGF, apelin, NGF, fibroblast growth factors, metalloproteinase inhibitors, matrix metalloproteniases, secreted protein acid), эндокринные (NEFA, leptin, resistin, omentin, estrogen, oleoy1-oestrogen, androgens, cortisol, cortisone, adiponectin, vistafin, vaspin, fasting-induced adipose factor, retinol binding protein, interleukin-6, IL-1β, IL-8, IL-10, IL-18, IL-17D, transforming growth factor-β, monocyte chemoattractant protein 1, macrophage migration inhibiting factor, complement components, haptoglobine, serum amyloid A3, plasminogen activator inhibitor-1, pigment epithelian-derived factor, adrenomedullin, VEGF, apelin