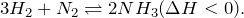при каких параметрах скорость реакции азота с водородом уменьшается ответ
Скорость реакции азота с водородом уменьшится при
Помогите ответить на вопрос теста. Скорость реакции азота с водородом уменьшится при: уменьшении температуры, увеличении концентрации азота, использовании катализатора, увеличении давления? Расскажите о принципе Ле-Шателье.
Влияние различных факторов на состояние химического равновесия качественно описывается принципом равновесия Ле Шателье (1884). Согласно этому принципу, при всяком внешнем воздействии на систему, находящуюся в состоянии химического равновесия, в ней протекают процессы, приводящие к уменьшению этого воздействия. Действительно, повышение температуры увеличивает выход продуктов эндотермических реакций, в ходе которых подводимая теплота поглощается. Практическое использование принципа смещения равновесия можно показать на примере синтеза аммиака. Эта реакция экзотермична и протекает с уменьшением объема:
Синтез аммиака идет тем полнее, чем ниже температура (
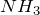
Принцип смещения равновесия применим только к системам, находящимся в состоянии истинного химического равновесия. Поэтому в конденсированных (особенно твердофазных) системах, процессы в которых часто заторможены, применение этого принципа ограничено.
При каких параметрах скорость реакции азота с водородом уменьшается ответ
С наименьшей скоростью происходит реакция между водородом и
Скорость реакции зависит от природы реагирующих веществ. Активность галогенов падает от фтора к иоду, поэтому с наименьшей скоростью происходит реакция между водородом и иодом.
С наибольшей скоростью водород реагирует с
Скорость реакции зависит от природы реагирующих веществ. Наиболее активный элемент, входящий в простые вещества неметаллы, это фтор, значит, реакция с водородом пойдет с большей скоростью
При комнатной температуре водород наиболее активно реагирует с
Скорость реакции зависит от природы реагирующих веществ. Самым сильным окислителем из представленных веществ является молекулярный хлор.
Наиболее активный элемент, входящий в простые вещества неметаллы, это азот, но молекула азота очень инертна из-за наличия тройной связи между атомами азота.
С наибольшей скоростью при обычных условиях происходит взаимодействие воды с
3) оксидом кремния (IV)
С алюминием и оксидом кремния (IV) вода не реагирует.С железом реагирует при нагревании. Остается ответ№1
«С алюминием и оксидом кремния (IV) вода не реагирует.»
Методическая ошибка. Не объяснена причина, почему алюминий не реагирует с водой. Алюминий металл активней железа и без пояснения, что на поверхности алюминия образуется оксидная пленка, у учащихся может сформироваться ошибочное знание.
Да и по поводу диоксида кремния, тоже не мешало бы пояснить.
Для этого и существуют учебники (бумажные, электронные. ). А этот сайт учебником не является, это, скорее, задачник.
С наименьшей скоростью при комнатной температуре протекает взаимодействие между
1)
2)
3)
4)
С наименьшей скоростью при комнатной температуре протекает реакция между и
. Данный процесс активно протекает только при высоких температурах.
Задания 20. Скорость реакции и ее зависимость от различных факторов.
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к уменьшению скорости реакции этилена с водородом.
1) понижение температуры
2) увеличение концентрации этилена
3) использование катализатора
4) уменьшение концентрации водорода
5) повышение давления в системе
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 14
1) понижение температуры
Понижение температуры снижает скорость любой реакции, как экзотермической, так и эндотермической.
2) увеличение концентрации этилена
Увеличение концентрации реагентов всегда увеличивает скорость реакции
3) использование катализатора
Все реакции гидрирования органических соединений являются каталитическими, т.е. существенно ускоряются в присутствии катализаторов.
4) уменьшение концентрации водорода
Уменьшение концентрации исходных реагентов всегда снижает скорость реакции
5) повышение давления в системе
Повышение давления, когда хотя бы один из реагентов является газом, увеличивает скорость реакции, т.к. фактически это то же самое, что увеличение концентрации этого реагента.
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции метанола с пропионовой кислотой.
1) повышение температуры
2) понижение давления
3) понижение температуры
4) использование сильной неорганической кислоты в качестве катализатора
5) облучение ультрафиолетовым светом
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 14
1) повышение температуры
При повышении температуры скорость любой реакции увеличивается (как экзотермической, так и эндотермической)
2) понижение давления
3) понижение температуры
Понижение температуры снижает скорость любой реакции (как экзотермической, так и эндотермической).
4) использование сильной неорганической кислоты в качестве катализатора
Взаимодействие спиртов с карбоновыми кислотами (реакция этерификации) ускоряется в присутствии сильных минеральных (неорганических) кислот
5) облучение ультрафиолетовым светом
Реакция этерификации протекает по ионному механизму, а ультрафиолетовый свет влияет лишь на некоторые реакции, протекающие по свободнорадикальному механизму, например, хлорирование метана.
Скорость прямой реакции
1) увеличении концентрации азота
2) уменьшении концентрации азота
3) увеличении концентрации аммиака
4) уменьшении концентрации аммиака
5) повышении температуры
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 15
Из предложенного перечня внешних воздействий выберите два воздействия, от которых не зависит скорость реакции
1) степень измельчения угля
5) концентрация CO2
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 34
Из предложенного перечня внешних воздействий выберите два воздействия, при которых скорость реакции
1) повышение концентрации CO2
2) понижение температуры
3) повышение давления
4) повышение температуры
5) степень измельчения CaO
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 45
Из предложенного перечня внешних воздействий выберите два воздействия, которые не оказывают влияния на скорость реакции
1) изменение концентрации HCOOCH3
2) использование катализатора
3) повышение давления
4) повышение температуры
5) изменение концентрации HCOOH
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 35
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции
1) увеличение концентрации сернистого газа
2) повышение температуры
3) уменьшение концентрации кислорода
4) понижение температуры
5) увеличение концентрации кислорода
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 25
Из предложенного перечня внешних воздействий выберите два воздействия, которые не влияют на скорость реакции
1) изменение концентрации соляной кислоты
2) изменение давления
3) изменение температуры
4) изменение концентрации сульфита натрия
5) изменение концентрации хлорида натрия
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 25
Из предложенного перечня веществ выберите по две пары, реакция между которыми протекает с наибольшей скоростью при комнатной температуре.
2) растворы карбоната натрия и хлорида калия
3) калий и разбавленная серная кислота
4) магний и соляная кислота
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 34
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции
1) увеличение концентрации кислорода
2) понижение температуры
3) увеличение концентрации углекислого газа
4) увеличение концентрации метана
5) понижение давления
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 14
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции
1) понижение давления в системе
2) повышение давления в системе
3) повышение температуры
4) степень измельчения серебра
5) степень измельчения нитрата серебра
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 35
Из предложенного перечня веществ выберите по две пары, реакция между которыми протекает с наименьшей скоростью при комнатной температуре.
1) сульфат меди (р-р) и гидроксид натрия (р-р)
5) серная кислота (р-р) и карбонат калия (р-р)
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 34
Из предложенного перечня веществ выберите по две пары, скорость реакции между которыми повышается при увеличении давления.
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 13
Из предложенного перечня реакции выберите две реакции, скорость которых увеличивается при увеличении концентрации азота.
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 15
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции
1) увеличение концентрации ионов железа
2) измельчение металлического железа
3) добавление нескольких кусочков железа
4) увеличение концентрации кислоты
5) уменьшение температуры
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 24
Из предложенного перечня веществ выберите по две пары, скорость реакции между которыми не зависит от увеличения площади поверхности соприкосновения реагентов.
2) кремний и кислород
3) водород и кислород
4) диоксид серы и кислород
5) цинк и соляная кислота
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 34
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к увеличению скорости реакции азота с водородом.
1) увеличение температуры
2) использование ингибитора
3) использование катализатора
4) уменьшение концентрации аммиака
5) уменьшение концентрации водорода
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 13
Из предложенного перечня внешних воздействий выберите два воздействия, которые не приводят к изменению скорости реакции
1) изменение температуры
2) изменение концентрации спирта
3) изменение концентрации щелочи
4) изменение концентрации соли
5) изменение концентрации эфира
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 24
Из предложенного перечня внешних воздействий выберите два воздействия, при которых скорость реакции гидролиза сложного эфира значительно увеличится.
1) увеличение температуры
2) добавление щелочи
3) уменьшение концентрации спирта
4) уменьшение концентрации эфира
5) увеличение давления
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 12
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к изменению скорости реакции между медью и азотной кислотой.
1) увеличение массы меди
2) увеличение концентрации кислоты
3) уменьшение температуры
4) уменьшение объема кислоты
5) увеличение объема колбы
Запишите в Поле «ОТВЕТ» номера выбранных типов реакций.
Ответ: 23
Из предложенного перечня выберите два внешних воздействия, которые приводят к увеличению скорости реакции железа с серой.
1) понижение давления в системе
2) понижение температуры
3) добавление сульфида железа(II)
4) увеличение степени измельчения железа
5) повышение температуры
Запишите в поле ответа номера выбранных внешних воздействий.
Ответ: 45
Из предложенного перечня выберите два внешних воздействия, которые приводят к увеличению скорости реакции между растворами медного купороса и гидроксида натрия.
1) понижение давления в системе
2) увеличение концентрации щёлочи
3) повышение давления в системе
4) увеличение концентрации купороса
5) понижение температуры
Запишите в поле ответа номера выбранных внешних воздействий.
Ответ: 24
Из предложенного перечня выберите два внешних воздействия, которые приводят к увеличению скорости реакции между растворами медного купороса и сульфида натрия.
1) использование ингибитора
2) повышение давления в системе
3) увеличение концентрации сульфида натрия
4) увеличение концентрации сульфата меди(II)
5) понижение температуры
Запишите в поле ответа номера выбранных внешних воздействий.
Ответ: 34
Из предложенного перечня выберите два внешних воздействия, которые приводят к увеличению скорости реакции пропена с водородом.
1) понижение температуры
2) увеличение концентрации водорода
3) использование ингибитора
4) уменьшение концентрации водорода
5) повышение давления в системе
Запишите в поле ответа номера выбранных внешних воздействий.
Ответ: 25
Из предложенного перечня выберите два внешних воздействия, которые приводят к увеличению скорости реакции азота с водородом.
1) понижение температуры
2) увеличение концентрации азота
3) использование ингибитора
4) уменьшение концентрации водорода
5) повышение давления в системе
Запишите в поле ответа номера выбранных внешних воздействий.
Ответ: 25
Из предложенного перечня выберите две реакции, для которых увеличение давления приводит к увеличению скорости реакции.
Запишите в поле ответа номера выбранных реакций.
Ответ: 23
Из предложенного перечня выберите две реакции, для которых уменьшение концентрации кислоты приводит к уменьшению скорости реакции.
Запишите в поле ответа номера выбранных реакций.
При каких параметрах скорость реакции азота с водородом уменьшается ответ
Скорость реакции углерода с кислородом не зависит от
3) степени измельчённости углерода
4) количества продукта реакции
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Скорость гетерогенной реакции рассчитывается на единицу площади твердого вещества, поэтому не может зависеть от степени измельчения. Эта величина влияет не на скорость, а на интенсивность реакции
Скорость реакции азота с водородом определяется как
1)
2)
3)
4)
Вопрос не корректен, так как реагент и продукт не указаны в вопросе. И второе в уравнение скорости необходимо учитывать в знаменателе коэффициенты в уравнении реакции, поэтому с этой сточки зрения правильнее ответ 4. А дельта с может быть как меньше 0 так и больше. минус у вас не стоит ни в одном уравнении
Реагенты в вопросе указаны.
4 вариант противоречит понятию «скорость»
При реакции азота и водорода, только изменение концентрации аммиака величина положительная.
Извините, но есть же формула для определения скорости: V=К*С(N2)*C(H2), поэтому подходит 3 ответ.
там еще степени должны быть
Скорость реакции угарного газа с кислородом определяется как
1)
2)
3)
4)
С наибольшей скоростью при комнатной температуре взаимодействуют
1) цинк (гранулы) и кислород
2) цинк (гранулы) и соляная кислота
3) цинк (порошок) и кислород
4) цинк (порошок) и соляная кислота
Скорость гетерогенной реакции рассчитывается на единицу площади поверхности, поэтому не зависит от степени измельченности реагента
С наибольшей скоростью при комнатной температуре взаимодействуют
2) соляная кислота и раствор карбоната натрия
3) натриевая щелочь и алюминий
4) оксид кальция и вода
Взаимодействие двух растворимых веществ в воде будет протекать быстрее чем приведенные гетерогенные реакции.
При каких параметрах скорость реакции азота с водородом уменьшается ответ
Скорость химической реакции
(20%-ый раствор)
при обычных условиях больше, чем скорость реакции
1) (96%-ый раствор)
2) (20%-ый раствор)
3) (20%-ый раствор)
4) (5%-ый раствор)
5) (5%-ый раствор)
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
1) (96%-ый раствор)
— железо пассивируется концентрированной серной кислотой, поэтому скорость данной реакции будет крайне мала
5) (5%-ый раствор)
— скорость данной реакции будет ниже реакции в условии, так как в данном случае ниже концентрация кислоты.
Из предложенного перечня выберите все способы увеличения скорости реакции между твёрдым хлоридом натрия и серной кислотой.
1) увеличение общего давления
2) нагревание реакционного сосуда
4) увеличение концентрации кислоты
5) измельчение хлорида натрия
Запишите номера выбранных ответов в порядке возрастания.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— давление (при наличии газообразных реагентов — повышение давления повышает концентрацию газообразных веществ);
— катализатор (увеличивает скорость реакции).
1. Нет, поскольку реагенты не газообразны;
2. Скорость увеличится;
3. Добавление воды замедлит реакцию, поскольку концентрация реагентов уменьшится;
4. Скорость увеличится;
5. Скорость увеличится, поскольку увеличится площадь соприкосновения реагентов.
Скорость реакции углерода с кислородом не зависит от
3) степени измельчённости углерода
4) количества продукта реакции
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Скорость гетерогенной реакции рассчитывается на единицу площади твердого вещества, поэтому не может зависеть от степени измельчения. Эта величина влияет не на скорость, а на интенсивность реакции
Из предложенного перечня внешних воздействий выберите все воздействия, которые приводят к уменьшению скорости реакции этилена с водородом.
1) понижение температуры
2) увеличение концентрации этилена
3) использование катализатора
4) уменьшение концентрации водорода
5) повышение давления в системе
Запишите в поле ответа номера выбранных внешних воздействий.
1) Понижение температуры — уменьшит скорость реакции, как и для большинства реакций.
2) Увеличение концентрации этилена — увеличит скорость реакции.
3) Использование катализатора — увеличит скорость реакции.
4) Уменьшение концентрации водорода — уменьшит скорость реакции.
5) Повышение давления в системе — увеличит скорость реакции.
Скорость реакции уменьшится при
1) внесении катализатора
2) уменьшении концентрации
3) увеличении концентрации
4) уменьшении давления в системе
5) уменьшении концентрации кислорода
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Поэтому скорость реакции уменьшится при:
4) уменьшении давления в системе
5) уменьшении концентрации кислорода
Скорость реакции увеличится при
1) внесении катализатора
3) уменьшении концентрации кислорода
4) уменьшении давления в системе
5) увеличении концентрации
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Скорость этой реакции увеличится при
1) внесении катализатора
Реакция экзотермическая, при повышении температуры равновесие сместится в сторону обратной реакции
В вопросе нет ни слова о равновесии
Скорость реакции
1) внесении катализатора
3) уменьшении концентрации аммиака
4) уменьшении давления в системе
5) уменьшении концентрации
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Поэтому скорость реакции уменьшится при:
4) уменьшении давления в системе
5) уменьшении концентрации
Если стоит +Q, то при увеличении температуры скорость реакции будет уменьшаться, нет?
Не путайте скорость и смещение равновесия. Классическая ошибка. Здесь не идёт речь о равновесии.
Скорость реакции
1) добавлении ингибитора
3) увеличении концентрации FeCl2
4) увеличении давления в системе
5) увеличении концентрации кислоты
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Поэтому скорость реакции увеличится при:
5) увеличении концентрации кислоты
Скорость реакции уменьшится при
1) добавлении ингибитора
2) уменьшении концентрации
3) увеличении температуры
4) уменьшении давления в системе
5) добавлении катализатора
Запишите номера выбранных ответов.
Факторы влияющие на скорость реакции
— температура (с увеличением температуры увеличивается скорость реакции);
— концентрация реагентов (с увеличением концентрации реагентов увеличивается скорость реакции);
— площадь соприкосновения реагентов (для гетерогенных реакций);
— катализатор (увеличивает скорость реакции).
Скорость этой реакции уменьшится при
1) добавлении ингибитора
4) уменьшении давления в системе
Из предложенного перечня выберите все воздействия, которые приводят к уменьшению скорости реакции между цинком и соляной кислотой.
1) измельчение цинка
3) добавление
5) уменьшение количества реагентов с течением времени
Запишите в поле ответа номера выбранных воздействий.
Скорость химической реакции зависит от природы реагирующих веществ.
Скорость реакции увеличивается при увеличении температуры, увеличении концентрации исходных веществ (для газообразных и растворенных реагентов), увеличении площади соприкосновения реагентов (для гетерогенных реагентов — тех, которые находятся в разных фазах, например: жидкие и твердые, твердые и газообразные), при увеличении давления (для газообразных реагентов). Также скорость реакции увеличивается под влиянием катализаторов — веществ, ускоряющих реакцию, но не входящих в состав продуктов реакции.
Для указанных агрегатных состояний реагентов уменьшение температуры способствует снижению скорости реакции. По мере расходования реагентов скорость реакции уменьшается.
Из предложенного перечня выберите все пары веществ, у каждой из которых скорость реакции не зависит от изменения давления.
1) и
2) и
3) и
4) и
5) и
Запишите в поле ответа номера выбранных пар веществ.
Скорость химической реакции зависит от природы реагирующих веществ.
Скорость реакции увеличивается при увеличении температуры, увеличении концентрации исходных веществ (для газообразных и растворенных реагентов), увеличении площади соприкосновения реагентов (для гетерогенных реагентов — тех, которые находятся в разных фазах, например: жидкие и твердые, твердые и газообразные), при увеличении давления (для газообразных реагентов). Также скорость реакции увеличивается под влиянием катализаторов — веществ, ускоряющих реакцию, но не входящих в состав продуктов реакции.
Для указанных агрегатных состояний реагентов при увеличении температуры и концентрации реагентов скорость реакции увеличивается. Давление не будет влиять на скорость реакции между жидкими и твердыми веществами.