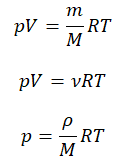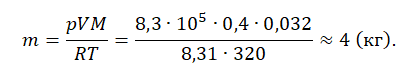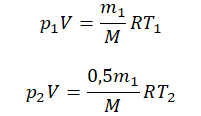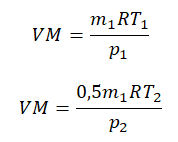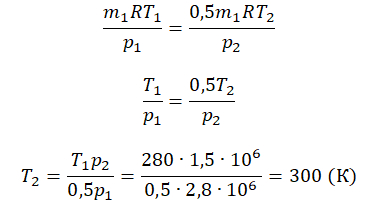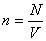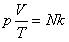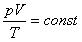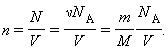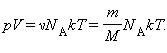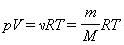состояние идеального газа определяется значениями параметров tpv где
Состояние идеального газа определяется значениями параметров tpv где
Файл: Тест.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлена: 31.01.2019
Просмотров: 8693
Скачиваний: 83
На рисунке изображен цикл Карно в координатах (T,S), где S-энтропия. Адиабатное сжатие происходит на этапе …
Процессы 2-3 и 4-1 являются адиабатными. Адиабатное сжатие происходит на этапе возрастания температуры, т.е. на участке 4 – 1.
Процесс, изображенный на рисунке в координатах (T,S), где S-энтропия, является…
1: адиабатным сжатием*
2: изохорным нагреванием
3: изобарным расширением
4: изотермическим расширением
Поскольку в процессе 1-2 не происходит изменения энтропии, то процесс является адиабатным. Т.к. температура Т увеличивается, то происходит процесс адиабатного сжатия.
Процесс, изображенный на рисунке в координатах (T,S), где S-энтропия, является…
1: адиабатным расширением*
2: изохорным охлаждением
3: изобарным сжатием
4: изотермическим сжатием
Поскольку в процессе 1-2 не происходит изменения энтропии, то процесс является адиабатным. Т.к. температура Т уменьшается, то происходит процесс адиабатного расширения.
Молярные теплоемкости гелия в процессах 1-2 и 1-3 равны С 1 и С 2 соответственно.
Молярные теплоемкости гелия в процессах 1-2 и 1-3 равны С 1 и С 2 соответственно.
Среди приведённых формул к изотермическому процессу имеют отношение
– адиабатный процесс; – изобарный процесс; – адиабатный процесс.
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для адиабатного расширения газа справедливы соотношения…
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для адиабатного сжатия газа справедливы соотношения…
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для адиабатного сжатия газа справедливы соотношения…
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для изохорного охлаждения газа справедливы соотношения…
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для изобарного охлаждения газа справедливы соотношения…
Внутренняя энергия уменьшается за счёт того, что над газом совершается работа и газ отдаёт тепло окружающей среде.
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для изотермического сжатия газа справедливы соотношения…
При совершении работы внешними силами газ отдаёт тепло окружающей среде.
Если – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для изобарного нагревания газа справедливы соотношения…
Уравнение состояния идеального газа
теория по физике 🧲 молекулярная физика, МКТ, газовые законы
Уравнение состояния идеального газа было открыто экспериментально. Оно носит название уравнения Клапейрона — Менделеева. Это уравнение устанавливает математическую зависимость между параметрами идеального газа, находящегося в одном состоянии. Математически его можно записать следующими способами:
Уравнение состояния идеального газа
Внимание! При решении задач важно все единицы измерения переводить в СИ.
Пример №1. Кислород находится в сосуде вместимостью 0,4 м 3 под давлением 8,3∙10 5 Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода равна 0,032 кг/моль.
Из основного уравнения состояния идеального газа выразим массу:
Уравнение состояния идеального газа следует использовать, если газ переходит из одного состояния в другое и при этом изменяется его масса (количество вещества, число молекул) или молярная масса. В этом случае необходимо составить уравнение Клапейрона — Менделеева отдельно для каждого состояния. Решая систему уравнений, легко найти недостающий параметр.
Подсказки к задачам
| Давление возросло на 15% | p2 = 1,15p1 |
| Объем увеличился на 2% | V2 = 1,02V1 |
| Масса увеличилась в 3 раза | m2 = 3m1 |
| Газ нагрелся до 25 о С | T2 = 25 + 273 = 298 (К) |
| Температура уменьшилась на 15 К (15 о С) | T2 = T1 – 15 |
| Температура уменьшилась в 2 раза | 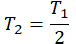 |
| Масса уменьшилась на 20% | m2 = 0,8m1 |
| Выпущено 0,7 начальной массы | |
| Какую массу следует удалить из баллона? | Нужно найти разность начальной и конечной массы: |
| Газ потерял половину молекул | 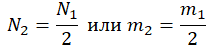 |
| Молекулы двухатомного газа (например, водорода), диссоциируют на атомы | 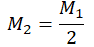 |
| Озон (трехатомный кислород) при нагревании превращается в кислород (двухатомный газ) | M (O3) = 3Ar (O)∙10 –3 кг/моль M (O2) = 2Ar (O)∙10 –3 кг/моль |
| Открытый сосуд | Объем V и атмосферное давление pатм остаются постоянными |
| Закрытый сосуд | Масса m, молярная масса M, количество вещества ν, объем V, число N и концентрация n частиц, плотность ρ— постоянные величины |
| Нормальные условия | Температура T0 = 273 К Давление p0 = 10 5 Па |
| Единицы измерения давления | 1 атм = 10 5 Па |
Пример №2. В баллоне содержится газ под давлением 2,8 МПа при температуре 280 К. Удалив половину молекул, баллон перенесли в помещение с другой температурой. Определите конечную температуру газа, если давление уменьшилось до 1,5 МПа.
Так как половина молекул была выпущена, m2 = 0,5m1. Объем остается постоянным, как и молярная масса. Учитывая это, запишем уравнение состояния идеального газа для начального и конечного случая:
Преобразим уравнения и получим:
Приравняем правые части и выразим искомую величину:

Алгоритм решения
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
pазбирался: Алиса Никитина | обсудить разбор | оценить
На высоте 200 км давление воздуха составляет примерно 10 –9 от нормального атмосферного давления, а температура воздуха Т – примерно 1200 К. Оцените плотность воздуха на этой высоте.
Уравнение состояния идеального газа. Состояние заданной массы газа определяется значениями трех параметров: давления p, объема V и температуры T
Состояние заданной массы газа определяется значениями трех параметров: давления p, объема V и температуры T. Эти параметры закономерно связаны друг с другом, так что изменение одного из них влечет за собой изменение других. Указанная связь может быть задана аналитически или в виде функции
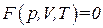
Соотношение, определяющее связь между параметрами какого-либо тела, называется уравнением состояния этого тела. Следовательно, (1.15) представляет собой уравнение состояния данной массы газа.
Простейшими свойствами обладает воображаемый газ, взаимодействие между молекулами которого пренебрежимо мало. Такой газ называется идеальным. Взаимодействие между молекулами всякого газа становится пренебрежимо слабым при большом разрежении, т. е. при малых плотностях газа. Всякий реальный газ при достаточном разрежении близок по своим свойствам к идеальному. Некоторые газы, такие как воздух, азот, кислород, даже при обычных условиях, т. е. при комнатной температуре и атмосферном давлении, мало отличаются от идеального газа. Особенно близки по своим свойствам к идеальному газу гелий и водород.
При небольших плотностях газы с хорошей точностью подчиняются уравнению
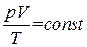
Следовательно, это уравнение есть уравнение состояния идеального газа.
В соответствии с законом, установленным Авогадро, моли всех газов занимают при одинаковых условиях (т. е. при одинаковых температуре и давлении) одинаковый объем. В частности, при так называемых нормальных условиях, т. е. при 0°C и при давлении в 1 атм (1,01·10 5 Па), объем моля любого газа равен 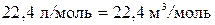
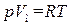
Мы поставили при V индекс «м», чтобы показать, что речь идет об объеме, занимаемом при данных p и T молем газа. Уравнение (1.17) есть уравнение состояния идеального газа, написанное для одного моля.
Величина R называется газовой постоянной. Согласно соотношению (1.17) и закону Авогадро
(произносится: джоуль на моль-кельвин)[7].
От уравнения (1.17) для одного моля легко перейти к уравнению для любой массы m, приняв во внимание, что при одинаковых давлениях и температуре ν молей газа будут занимать в ν раз больший объем, чем один моль: 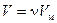
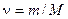
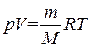
Это уравнение представляет собой уравнение состояния идеального газа, написанное для массы газа m.
Уравнению (1.18) можно придать другой вид. Для этого введем величину
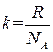
(R – газовая постоянная, NA – число Авогадро). Эта величина называется постоянной Больцмана. Она имеет более глубокий физический смысл, чем постоянная R. Далее будет показано, что k представляет собой коэффициент пропорциональности между средней энергией теплового движения молекулы и абсолютной температурой. Подстановка в (1.19) числовых значений R и NA дает
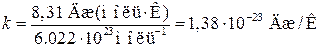
Умножим и разделим правую часть уравнения (1.18) на NA. Тогда уравнение можно написать в виде
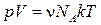
Произведение νNA равно числу молекул N, содержащихся в массе газа m. С учетом этого получаем, что
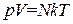
Теперь разделим обе части уравнения (1.20) на V. Приняв во внимание, что 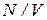
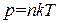
Уравнения (1.18), (1.20) и (1.21) представляют собой различные формы записи уравнения состояния идеального газа.
Отношение массы газа к занимаемому им объему дает плотность газа: 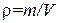
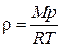
Таким образом, плотность идеального газа пропорциональна давлению и обратно пропорциональна температуре.
Простая связь между температурой и остальными параметрами идеального газа делает заманчивым использование его в качестве виртуального термометрического вещества. Обеспечив постоянство объема и используя в качестве температурного признака давление газа, можно получить воображаемый термометр с идеально линейной температурной шкалой. В дальнейшем эту шкалу мы будем называть идеальной газовой шкалой температур.
Практически, по международному соглашению, в качестве термометрического тела берется водород. Установленная по водороду с использованием уравнения (1.18) шкала называется эмпирической шкалой температур.
Как сказал.
Вопросы к экзамену
Для всех групп технического профиля

Урок 15. Лекция 15. Идеальный газ
Как известно, многие вещества в природе могут находиться в трех агрегатных состояниях: твердом, жидком и газообразном.
Учение о свойствах вещества в различных агрегатных состояниях основывается на представлениях об атомно-молекулярном строении материального мира. В основе молекулярно-кинетической теории строения вещества (МКТ) лежат три основных положения:
Значит, агрегатное состояние вещества зависит от взаимного расположения молекул, расстояния между ними, сил взаимодействия между ними и характера их движения.
Сильнее всего проявляется взаимодействие частиц вещества в твердом состоянии. Расстояние между молекулами примерно равно их собственным размерам. Это приводит к достаточно сильному взаимодействию, что практически лишает частицы возможности двигаться: они колеблются около некоторого положения равновесия. Они сохраняют форму и объем.
Свойства жидкостей также объясняются их строением. Частицы вещества в жидкостях взаимодействуют менее интенсивно, чем в твердых телах, и поэтому могут скачками менять свое местоположение – жидкости не сохраняют свою форму – они текучи. Жидкости сохраняют объем.
Газ представляет собой собрание молекул, беспорядочно движущихся по всем направлениям независимо друг от друга. Газы не имеют собственной формы, занимают весь предоставляемый им объем и легко сжимаются.
Модель идеального газа. Связь между давлением и средней кинетической энергией.
Для выяснения закономерностей, которым подчиняется поведение вещества в газообразном состоянии, рассматривается идеализированная модель реальных газов – идеальный газ. Это такой газ, молекулы которого рассматриваются как материальные точки, не взаимодействующие друг с другом на расстоянии, но взаимодействующие друг с другом и со стенками сосуда при столкновениях.
Идеальный газ – это газ, взаимодействие между молекулами которого пренебрежимо мало. (Ек>>Ер)
Идеальный газ – это модель, придуманная учеными для познания газов, которые мы наблюдаем в природе реально. Она может описывать не любой газ. Не применима, когда газ сильно сжат, когда газ переходит в жидкое состояние. Реальные газы ведут себя как идеальный, когда среднее расстояние между молекулами во много раз больше их размеров, т.е. при достаточно больших разрежениях.
Свойства идеального газа:
Состояние некоторой массы газообразного вещества характеризуют зависимыми друг от друга физическими величинами, называемыми параметрами состояния. К ним относятся объем V, давление p и температура T.
Давление – физическая величина, равная отношению силы F, действующей на элемент поверхности перпендикулярно к ней, к площади S этого элемента.
До настоящего времени употребляются внесистемные единицы давления:
техническая атмосфера 1 ат = 9,81-104 Па;
физическая атмосфера 1 атм = 1,013-105 Па;
миллиметры ртутного столба 1 мм рт. ст.= 133 Па;
1 атм = = 760 мм рт. ст. = 1013 гПа.
Как возникает давление газа? Каждая молекула газа, ударяясь о стенку сосуда, в котором она находится, в течение малого промежутка времени действует на стенку с определенной силой. В результате беспорядочных ударов о стенку сила со стороны всех молекул на единицу площади стенки быстро меняется со временем относительно некоторой (средней) величины.
Давление газа возникает в результате беспорядочных ударов молекул о стенки сосуда, в котором находится газ.
Используя модель идеального газа, можно вычислить давление газа на стенку сосуда.
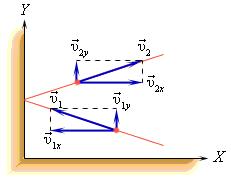
В процессе взаимодействия молекулы со стенкой сосуда между ними возникают силы, подчиняющиеся третьему закону Ньютона. В результате проекция υx скорости молекулы, перпендикулярная стенке, изменяет свой знак на противоположный, а проекция υy скорости, параллельная стенке, остается неизменной.
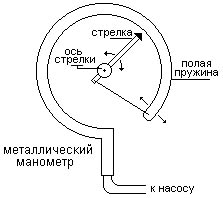
Приборы, измеряющие давление, называют манометрами. Манометры фиксируют среднюю по времени силу давления, приходящуюся на единицу площади его чувствительного элемента (мембраны) или другого приемника давления.

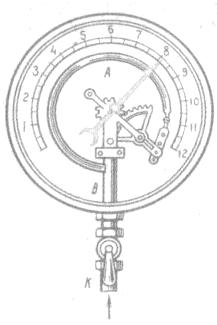
Металлический манометр – для измерения больших давлений.
Основной его частью является изогнутая трубка А, открытый конец которой припаян к трубке В, через которую поступает газ, а закрытый – соединен со стрелкой. Газ поступает через кран и трубку В в трубку А и разгибает её. Свободный конец трубки, перемещаясь, приводит в движение передающий механизм и стрелку. Шкала градуирована в единицах давления.
Основное уравнение молекулярно-кинетической теории идеального газа.
Основное уравнение МКТ: давление идеального газа пропорционально произведению массы молекулы, концентрации молекул и среднему квадрату скорости движения молекул
n = N/V – число молекул в единице объема, или концентрация молекул;
Так как средняя кинетическая энергия поступательного движения молекул E = m0*v 2 /2, то домножив основное уравнение МКТ на 2, получим p = 2/3· n·(m0· v 2 )/2 = 2/3·E·n
Давление газа равно 2/3 от средней кинетической энергии поступательного движения молекул, которые содержатся в единичном объеме газа.
Так как m0·n = m0·N/V = m/V = ρ, где ρ – плотность газа, то имеем p = 1/3· ρ· v 2
Объединенный газовый закон.
Макроскопические величины, однозначно характеризующие состояние газа, называют термодинамическими параметрами газа.
Важнейшими термодинамическими параметрами газа являются его объем V, давление р и температура Т.
Всякое изменение состояния газа называется термодинамическим процессом.
В любом термодинамическом процессе изменяются параметры газа, определяющие его состояние.
Соотношение между значениями тех или иных параметров в начале и конце процесса называется газовым законом.
Газовый закон, выражающий связь между всеми тремя параметрами газа называется объединенным газовым законом.
Соотношение p = nkT связывающее давление газа с его температурой и концентрацией молекул, получено для модели идеального газа, молекулы которого взаимодействуют между собой и со стенками сосуда только во время упругих столкновений. Это соотношение может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν. Для этого нужно использовать равенства
где n – концентрация молекул, N – общее число молекул, V – объем газа
Тогда получим 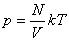
Так как при постоянной массе газа N остается неизменным, то Nk – постоянное число, значит
При постоянной массе газа произведение объема на давление, деленное на абсолютную температуру газа, есть величина одинаковая для всех состояний этой массы газа.
Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Б. Клапейроном и часто его называют уравнением Клайперона.
Уравнение Клайперона можно записать в другой форме.
Здесь N – число молекул в сосуде, ν – количество вещества, NА – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим:
Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной (молярной) газовой постоянной и обозначается буквой R.
Ее численное значение в СИ R = 8,31 Дж/моль·К
называется уравнением состояния идеального газа.
В полученной нами форме оно было впервые записано Д. И. Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева.`
Для одного моля любого газа это соотношение принимает вид: pV=RT
Установим физический смысл молярной газовой постоянной. Предположим, что в некотором цилиндре под поршнем при температуре Е находится 1 моль газа, объем которого V. Если нагреть газ изобарно (при постоянном давлении) на 1 К, то поршень поднимется на высоту Δh, а обьем газа увеличится на ΔV.
Запишем уравнение pV=RT для нагретого газа: p ( V + ΔV ) = R (T + 1)
ΔV = SΔh, где S – площадь основания цилиндра. Подставим в полученное уравнение:
pS = F – сила давления.
Получим FΔh = R, а произведение силы на перемещение поршня FΔh = А – работа по перемещению поршня, совершаемая этой силой против внешних сил при расширении газа.
Универсальная (молярная) газовая постоянная численно равна работе, которую совершает 1 моль газа при изобарном нагревании его на 1 К.