вторичный иммунодефицит код мкб
Тяжелый комбинированный иммунодефицит
Общая информация
Краткое описание
Тяжелый комбинированный иммунодефицит (тяжелая комбинированная иммунная недостаточность-ТКИН) – генетически обусловленный иммунодефицит, характеризующийся практически полным отсутствием зрелых Т-лимфоцитов при наличии или отсутствии В- и НК-лимфоцитов, что ведет к ранним, крайне тяжелым инфекциям вирусной, бактериальной и оппортунистической природы и в отсутствие патогенетической терапии смерти в первые два года жизни.
Общая частота ТКИН 1:50000 новорожденных. Среди больных преобладают лица мужского пола.
Соотношение кодов МКБ-10 и МКБ-9
| МКБ-10 | МКБ-9 | ||
| Код | Название | Код | Название |
| D81.0 | Тяжелый комбинированный иммунодефицит с ретикулярным дисгенезом | 86.10 | Диагностические процедуры на коже и подкожных тканях |
| D81.1 | Тяжелый комбинированный иммунодефицит с низким содержанием Т и В- клеток | 86.11 | Биопсия кожи и подкожных тканей |
| D81.2 | Тяжелый комбинированный иммунодефицит с низким и нормальным содержанием В-клеток | 40.11 | Биопсия лимфатической структуры |
| D81.3 | Дефицит аденозиндезаминазы | ||
| D81.4 | Синдром Незелофа | ||
| D81.5 | Дефицит пуриннуклеозидфосфорилазы | ||
| D81.6 | Дефицит молекул класса I главного комплекса гистосовместимости | ||
| D81.7 | Дефицит молекул класса IIглавного комплекса гистосовместимости | ||
| D81.8 | Другие комбинированный иммунодефициты | ||
| D81.9 | Комбинированный иммунодефицит неуточненный | ||
Дата разработки/пересмотра протокола: 2016 год.
Пользователи протокола: врачи общей практики, педиатры, неонатологи, детские онкологи/гематологи, иммунологи, аллергологи.
Категории пациентов: дети 0-2 года.
Шкала уровня доказательности:
| A | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| B | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| C | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
В зависимости от измененного гена выделяют аутосомно-рецессивный и Х-сцепленный тип наследования [2].
Диагностика (амбулатория)
ДИАГНОСТИКА НА АМБУЛАТОРНОМ УРОВНЕ [1-3,5,7]
Диагностические критерии
Жалобы и анамнез: разнообразие жалоб связано с многообразием клинических проявлений осложнений тяжелого комбинированного иммунодефицита и уровнем дефекта. Преимущественные жалобы на затяжные пневмонии, отставание массы тела, частый жидкий стул, длительный кашель, затяжные лихорадки, появление частых гнойных выделений из различных локусов, упорный афтозный стоматит, снижение аппетита, рвота, длительный кашель [3,5].
При сборе семейного анамнеза надо обращать внимание на случаи повторных тяжелых инфекций и смертей детей в раннем возрасте с клиникой инфекционных заболеваний. Смерти мальчиков в нескольких поколениях в семье позволяет предполагать Х-сцепленный характер заболевания. Близкородственный брак у родителей увеличивает вероятность аутосомно-рецессивной патологии [2, 5-7].
Клиническая симптоматика:
· отставание ребенка в возрасте до 1 года в весе и росте;
· поствакцинальные осложнения (БЦЖит диссеминированный, полиомиелит паралитический и др.);
· перенесенные не менее 2 раз тяжелые инфекции, такие как: менингит, остеомиелит, целлюлит, сепсис;
· частые гнойные отиты — не менее 3-4 раз в течение одного года;
· упорная молочница и грибковые поражения кожи;
· гнойное воспаление придаточных пазух носа 2 и более раз в течение года;
· рецидивирующие гнойные поражения кожи;
· рецидивирующие типичные бактериальные инфекции, протекающие в тяжелой форме, с необходимостью использования множественных курсов антибиотиков (до 2 месяцев и дольше);
· оппортунистические инфекции (например: Pneumocystic carini), вирусами герпес группы, грибками, проявляются в очень тяжелой, хронической форме или не поддаются стандартному лечению, (необходимо внутривенное введение антибиотиков);
· рецидивирующие (повторные) диареи; мальабсорбция;
· отсутствие/увеличение лимфатических узлов;
· увеличение печени и селезенки;
· наличие в семье больных ПИД;
· наличие в семейном анамнезе смерти ребенка раннего возраста с клиникой инфекционного заболевания;
· изменения в анализе крови: очень часто анемия, в лейкоформуле снижение количества лимфоцитов, эритроцитов, реже тромбоцитов;
· абсцессы внутреннего органа;
· рецидивирующие абсцессы подкожной клетчатки;
· тяжелое или длительное проявление бородавок, контагиозный моллюск.
Физикальное обследование
· рост и вес ребенка. У детей с ТКИН часто отмечается задержка развития;
· лимфатическая система: периферические лимфатические узлы уменьшены или отсутствуют, реже лимфаденопатия (чрезмерная);
· увеличение печени и селезенки;
· кожные покровы и слизистые: кандидоз кожи и слизистых при отсутствии предрасполагающих факторов (лечения антибиотиками или кортикостероидами, инфицирование при кормлении грудью). Изъязвления языка, слизистой рта и перианальной области. Гнойные инфекции кожи и подкожной клетчатки. Возможна сыпь по типу себорейного дерматита. Конъюнктивит, вызванный Haemophilus influenzae;
· заболевания ЛОР органов: хронические гнойные отиты, сопровождающиеся рубцовыми имениями барабанной перепонки;
· неврологические нарушения: энцефалопатии;
· позднее отпадение пуповины, омфалиты.
Инструментальные исследования:
· УЗИ органов брюшной полости, щитовидной железы и других органов (по показаниям);
· УЗИ вилочковой железы;
· Рентгенография органов грудной клетки (по показаниям);
· Рентгенография грудной клетки в двух проекциях (дополнительно размер вилочковой железы).
Диагностический алгоритм: (схема) 
Диагностика (стационар)
ДИАГНОСТИКА НА СТАЦИОНАРНОМ УРОВНЕ [2,4] (УД – В)
Диагностические критерии: см. амбулаторный уровень.
Лабораторные исследования:
· общий анализ крови + лейкоформула ручным методом;
· биохимический анализ крови: ферритин сыворотки, железо сыворотки, трансферрин, АЛТ, АСТ, билирубин общий/фракции, щелочная фосфатаза, гамма‐глутамилтранспептидаза, общий белок, определение белковых фракций, уровень иммуноглобулинов A,M,G,E, креатинин, мочевина, электролиты;
· развернутая иммунограмма : подсчет субпопуляционного состава Т-, В-лимфоцитов, NK-клеток, HLA DR+CD3+, HLADR+CD3-, CD25+, CD95+;
· CD4+8+, уровень сывороточных иммуноглобулинов (с подтипами G1,2,3,4, sIgA), кислородзависимый и кислороднезависимый фагоцитоз, определение активности компонентов комплемента, тесты функциональной активности Т-лимфоцитов, цитокиновый статус, интерфероновый статус, экспрессия рецепторов цитокинов;
· определение TREG [2];
· исследование крови на ВИЧ;
· HLA-типирование ребенка и его ближайших родственников (сибсов и родителей) [2];
· микробиологические исследования – посевы биоматериала (на флору и грибы) с определением антибиотикочувствительности со слизистых, из очагов инфекции (включая кровь, мочу, кал, бронхоальвеолярный лаваж, ликвор и биопсийный материал) [2];
· при наличии вакцинации БЦЖ микроскопия материала на кислотоустойчивые бактерии, а также выявление M.bovii методом ПЦР;
· молекулярно- генетический анализ с помощью ПЦР и последующего секвенирования;
· ИФА и ПЦР на цитомегаловирусную, Эпштейн-Барр вирусную, герпес-инфекцию, токсоплазмоз;
· при подозрении на Т-В- ТКИН – АДА недостаточность необходимо цитохимическое исследование: определение АДА в эритроцитах и лимфоцитах;
· морфологическое исследование пунктата костного мозга с целью дифференциальной диагностики;
· гистологическое исследование кожи, лимфоузлов и ткани тимуса при подозрении на синдром Омен [4].
Инструментальные исследования [2]:
· УЗИ брюшной полости и забрюшинного пространства для оценки вовлеченности внутренних органов;
· УЗИ вилочковой железы;
· компьютерная томография грудной клетки с контрастированием сосудов даже при отсутствии указаний на подтвержденные пневмонии в анамнезе;
· рентгенография грудной клетки;
· рентгенография придаточных пазух носа в динамике.
Диагностический алгоритм: (схема)
Перечень основных диагностических мероприятий:
· общий анализ крови + лейкоформула ручным методом;
· пунктат костного мозга (миелограмма);
· биохимический анализ крови;
· определение белковых фракций;
· развернутая иммунограмма : подсчет субпопуляционного состава Т-,В-лимфоцитов, NK-клеток, HLA DR+CD3+, HLADR+CD3-, CD25+, CD95+, CD4+8+, уровень сывороточных иммуноглобулинов (с подтипами G1,2,3,4, sIgA), кислородзависимый и кислороднезависимый фагоцитоз, определение активности компонентов комплемента, тесты функциональной активности Т-лимфоцитов, цитокиновый статус, интерфероновый статус, экспрессия рецепторов цитокинов;
· общий анализ мочи;
· исследование крови, других сред на стерильность, грибы;
· бак посев из зева на стерильность, грибы;
· ИФА на цитомегаловирус, вирусы простого герпеса;
· ПЦР (кровь, моча, слюна) на цитомегаловирус, ВПГ, ВЭБ, вирус Зостер;
· ИФА на грибковые инфекции;
· ПЦР (кровь, отделяемого из различных локусов) на грибковую инфекцию;
· копрология, исследование кала на яйца глист и простейших;
· УЗИ органов брюшной полости и забрюшинного пространства;
· УЗИ вилочковой железы;
· рентгенография грудной клетки в 2-х проекциях;
· компьютерная томография грудной клетки с контрастированием сосудов;
· молекулярно-генетическое исследование с целью выявления причинной генетической мутации;
· исследование крови на ВИЧ;
· HLA типирование пациента (в качестве реципиента ТГСК) и его сиблингов ( в качестве потенциальных доноров).
Что такое вторичный иммунодефицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бычковой Е.Ю., остеопата со стажем в 22 года.
Определение болезни. Причины заболевания
Вторичный иммунодефицит формируется у людей старше 6 лет с исходно нормальным иммунитетом. До этого возраста происходит созревание иммунной системы, особенно полноценных механизмов противоинфекционной защиты, поэтому частое развитие инфекционных заболеваний у детей младше 6 лет не является признаком патологии.
Появление вторичного иммунодефицита обычно связано с воздействием окружающей среды или каких-либо других факторов, но у многих из пациентов можно выявить генетическую предрасположенность к нарушению иммунитета.
Иммунологически здоровый организм способен контролировать и предотвращать развитие инфекций и опухолевых процессов, то есть осуществлять иммунологический контроль внутренней среды.
Когда можно заподозрить вторичный иммунодефицит
Причины развития вторичных иммунодефицитных состояний:
Иммунодефицитные состояния у детей
Развитию иммунодефицита у детей, как и у взрослых, способствуют:
Дисбактериоз у матери является причиной дисбактериоза у ребёнка с последующим замедлением и неполноценным созреванием иммунной системы. Каждый курс антибиотикотерапии может усугубить это состояние.
Проявления иммунодефицита зависят от степени его выраженности, они сопровождаются частыми ОРВИ с инфекционными осложнениями, эпизодами лихорадки, болезненностью, увеличением лимфоузлов, болью в животе, рвотой и нарушением стула.
Симптомы вторичного иммунодефицита
Как проявляется вторичный иммунодефицит
Клинические проявления вторичного иммунодефицита разнообразны. Очень часто на первый план выходят симптомы основного заболевания, которое привело к развитию иммунодефицита. Но основные проявления проблем с иммунитетом, которые указывают на необходимость иммунологического обследования, всё же присутствуют. К ним относятся:
Все хронические инфекции и воспаления протекают на фоне ослабленной иммунной защиты. Поэтому любая хронизация инфекции будет указывать на несостоятельность иммунитета, который не может справиться с болезнью в ходе острого воспалительного процесса.
Патогенез вторичного иммунодефицита
В течение жизни организм подвергается воздействию различных повреждающих факторов, вызывающих вторичный иммунодефицит. Они приводят к угнетению реакций клеточного иммунитета, снижению лейкоцитов и интерферонов — белков иммунной системы, которые вырабатываются лейкоцитами и иммунными клетками и блокируют распространение вируса. Вследствие этого появляются хронические инфекционно-воспалительные процессы, часто рецидивирующие.
Опухоли, возникающие в организме с ослабленной иммунной защитой, истощают иммунитет по мере своего роста, а проводимое лечение (операция, лучевая и химиотерапия) усугубляют возникший иммунодефицит. В этом случае страдает клеточное звено иммунитета:
Классификация и стадии развития вторичного иммунодефицита
По причине возникновения выделяют:
По форме вторичный иммунодефицит может быть:
По продолжительности выделяют два типа вторичного иммунодефицита:
По локализации основного дефекта различают:
Установить локализацию повреждения иммунной системы, основываясь только на симптомах, без лабораторного исследования иммунного статуса, практически невозможно: сходная клиническая картина может наблюдаться при разных типах вторичного дефицита. Например, склонность к вирусным инфекциям может встречаться как при Т-клеточном дефиците, так и при дефиците системы интерферонов.
Осложнения вторичного иммунодефицита
Вторичный иммунодефицит, развивающийся на фоне инфекции и/или воспаления, становится причиной тяжёлых жизнеугрожающих состояний. Без своевременной коррекции иммунитета патологический круг замыкается: течение основной болезни ухудшается.
Наиболее частыми осложнениями вторичного иммунодефицита являются тяжёлые инфекционные заболевания: пневмония, сепсис, абсцесс и флегмона. Их основные проявления: высокая температура и признаки воспаления. При пневмонии наблюдается одышка, кашель и боль в грудной клетке. Сепсис является жизнеугрожающим состоянием, он развивается при попадании в кровь инфекции, сопровождается системной воспалительной реакцией и полиорганной недостаточностью. При абсцессах и флегмоне в организме присутствует очаг гнойного воспаления с выраженной болью, отёком и гиперемией (покраснением).
Диагностика вторичного иммунодефицита
Диагноз «вторичный иммунодефицит» ставится на основании истории болезни, физикального обследования и оценки статуса иммунной системы.
Чтобы назначить эффективных мер по коррекции иммунитета, важно выявить факторы, которые поспособствовали развитию иммунодефицита. Поэтому на консультацию к врачу-иммунологу стоит принести все имеющиеся обследования, а врач будет очень подробно расспрашивать о перенесённых заболеваниях, проведённом лечении, операциях и образе жизни пациента.
Как распознать вторичный иммунодефицит
При подозрении на вторичный иммунодефицит врач назначает анализ крови и иммунограмму — иммунологические тесты, которые оценивают компоненты иммунной системы с точки зрения количества и качества.
Схема обследования различных звеньев иммунной системы (иммунограмма):
На вторичный иммунодефицит могут указывать как пониженные, так и повышенные показатели иммунограммы.
При подозрении на дисбаланс ключевых нутриентов (витаминов, микроэлементов и т. д.) врач-иммунолог может назначить исследования:
В своём заключении врач-иммунолог может указать «вторичный иммунодефицит» как основной или сопутствующий диагноз. Всё зависит от клинической картины.
Лечение вторичного иммунодефицита
Лечение пациента с вторичным иммунодефицитом проводится совместно с врачом, который курирует пациента по поводу основного заболевания. Задача врача-иммунолога заключается в подборе иммунокорригирующей терапии.
«Коррекция иммунитета» в данном случае подразумевает восстановление ослабленной иммунной защиты, исправление дисбаланса её компонентов и иммунных реакций, ослабление патологических иммунных процессов и подавление аутоиммунных реакций.
Лечение вторичного иммунодефицита начинают с определения и устранения его причины. Например, при нарушении иммунитета, вызванном инфекционно-воспалительным процессом, устраняются очаги хронического воспаления.
Если вторичный иммунодефицит возник в результате витаминно-минеральной недостаточности, то назначаются комплексы, содержащие дефицитные компоненты. Например, при истощении лимфоузлов и старении вилочковой железы назначают витамины В6. При обострении или начале аутоиммунных и лимфопролиферативных заболеваний показаны витамины Е.
Важными минералами для иммунной системы являются цинк, йод, литий, медь, кобальт, хром, молибден, селен, марганец и железо. Эти микроэлементы помогают активировать ферменты, которые участвуют в иммунных реакциях. К примеру, цинк предотвращает гибель клеток иммунной системы.
Заместительное лечение вторичного иммунодефицита
Заместительная терапия помогает предотвратить инфекции. Для этого применяют:
Иммунотропное лечение вторичного иммунодефицита
При остром инфекционном воспалении иммуностимуляторы позволяют:
При хроническом инфекционном воспалении иммуномодуляторы:
На степень эффективности иммунокоррекции влияет кратность приёма и стадия заболевания. Срок действия иммуномодуляторов зависит от характера препарата, показателей иммунного статуса и вида заболевания, вызвавшего вторичный иммунодефицит.
Устранение дефицита одного звена иммунитета может привести к компенсации другого звена, так как иммунная система работает по принципу взаимосвязанных модулей.
Может быть назначен как один иммуномодулятор, так и несколько, то есть их комбинация. При комбинированной иммунокоррекцией последовательно или одновременно принимают несколько модуляторов, обладающих разными механизмами действия. Таких иммуномодулирующих препаратов сейчас довольно много.
Показаниями для комбинированной иммунотерапии являются:
ВАЖНО: Самостоятельно назначать себе иммунокорректоры нельзя, так как их бесконтрольное применение может спровоцировать развитие вторичного иммунодефицита.
Прогноз. Профилактика
При вторичном иммунодефиците работа иммунной системы нарушена слабее, чем при первичном. В большинстве случаев выявляется несколько факторов, подавляющих иммунный ответ.
Прогноз определяется тяжестью основного заболевания. Например, если иммунодефицит возник из-за нехватки витаминов или нарушения режима труда и отдыха, он намного легче компенсируется, чем иммунодефицит, спровоцированный опухолевым процессом, сахарным диабетом или ВИЧ-инфекцией.
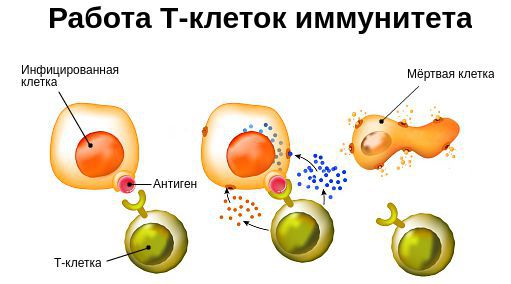
У детского организма отдельные звенья иммунной системы ещё незрелы: Т-лимфоциты только начинают «знакомиться» с различными инфекциями, поэтому ребёнок часто болеет ОРВИ. Со временем нарабатываются «клетки памяти». По мере взросления формируется широкий «репертуар» Т-лимфоцитов, способных распознавать и быстро запустить иммунный ответ, в связи с чем заболеваемость снижается.
С возрастом иммунная система стареет: в ответ на новые антигены участвует меньше Т-клеток, ухудшается кооперация между клетками иммунной системы, фагоциты хуже поглощают вирусы и мёртвые клетки. Поэтому многие инфекционно-воспалительные заболевания у пожилых людей протекают значительно тяжелее и чаще дают осложнения.
Первичная профилактика вторичного иммунодефицита заключается в ведении здорового образа жизни, сбалансированном питании, отказе от курения. Всё это позволяет предупредить развитие различных заболеваний.
Вторичная профилактика направлена на своевременное лечение инфекционных и общесоматических заболеваний.
Людям с вторичным иммунодефицитом нужны «особые условия», которые не позволят усугубить нарушение иммунитета. Пациентам следует:
Вакцинотерапия
Вакцинация проводится в соответствии с национальным календарем прививок. Перед введением вакцины нужно скомпенсировать иммунодефицит: пропить курс витаминов, минералов и иммуномодуляторов по назначению врача. Это позволит сформировать иммунный ответ на прививку и снизить риск осложнений.
Публикации в СМИ
Иммунодефициты вторичные
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ ПРИ НАРУШЕНИЯХ БИОХИМИЧЕСКОГО ГОМЕОСТАЗА
Состояния, приводящие к хроническому дисбалансу гормонов, питательных веществ и токсичных продуктов метаболизма, могут оказывать выраженные эффекты на один или несколько компонентов иммунной системы. В настоящей статье рассмотрены некоторые заболевания и состояния, при которых часто возникает клинически значимая дисфункция иммунной системы.
Сахарный диабет • Дисфункция нейтрофилов у больных СД предрасполагает к грибковым инфекциям • Существует прямая зависимость между степенью гипергликемии и подавлением функций нейтрофилов • Недостаточность микроциркуляции приводит к изъязвлению кожных покровов и ограничению хемотаксиса нейтрофилов к месту внедрения микроорганизмов • Типичные инфекционные осложнения СД — диссеминированный кандидоз, зигомикозы (Absidia, Mortierella, Mucor, Rhizopus) носовой полости и лёгких, а также отит, вызванный Pseudomonas aeruginosa.
Диализ/почечная недостаточность • Пациенты, находящиеся на хроническом гемодиализе, характеризуются подавлением функций Т-лимфоцитов in vitro и in vivo (кожная анергия), угнетением синтеза АТ и активности нейтрофилов, снижением экспрессии и/или функции рецепторов к Fc-фрагменту IgG • Механизм иммунодепрессии при гемодиализе полностью не изучен. Некоторые из иммунных дефектов частично объясняют высоким уровнем эндогенных ГК и применением бионесовместимых диализных мембран, повреждающих клеточную адгезию и ослабляющих фагоцитарный ответ • У больных, длительно находящихся на перитонеальном диализе, в результате потери с диализатом опсонинов (иммуноглобулинов и компонентов комплемента) и прямого супрессивного действия диализата возникает недостаточность функций нейтрофилов брюшины. В совокупности указанные факторы объясняют повышенную частоту бактериальных перитонитов в этой группе больных.
Нефротический синдром. Снижение концентрации многих сывороточных факторов приводит к депрессии иммунной системы у больных с нефротическим синдромом.
• Потеря иммуноглобулинов и белков комплемента увеличивает частоту бактериальных инфекций. Потеря витамина D и сывороточных факторов роста и дифференцировки может вызывать депрессию клеточного иммунитета.
• Иммунодепрессанты, назначаемые по поводу основного заболевания, усугубляют дефицит антиинфекционной резистентности.
• Нарушение питания повышает заболеваемость и смертность от инфекций, вызываемых превалирующими для данного региона возбудителями. Например, смертность от пневмонии и гастроэнтерита увеличивается в 10 и 30 раз, соответственно. В Латинской Америке алиментарная недостаточность выступает в качестве кофактора для 60% летальных исходов вследствие инфекционных заболеваний.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ ПРИ АУТОИММУННЫХ ЗАБОЛЕВАНИЯХ
Аутоиммунное заболевание и иммунодефицит часто сопутствуют друг другу. Как и при микробных инфекциях, умеренные изменения функции иммунной системы обнаруживают практически при всех аутоиммунных заболеваниях. Однако связь между ними и снижением иммунной защиты не так очевидна. Тем не менее при СКВ значение вторичных инфекций, связанных с иммунной дисфункцией, весьма существенно.
СКВ. Инфекции — основной фактор заболеваемости и смертности, а также главная причина летальных исходов 33% больных СКВ. Часто встречающиеся возбудители включают Staphylococcus aureus, E. coli, P. aeruginosa, Salmonella enteritidis, Streptococcus pneumoniae, Neisseria meningitidis, Listeria monocytogenes, Mycobacterium tuberculosis, Herpes zoster, Candida albicans, Cryptococcus neoformans, Pneumocystis carinii, Toxoplasma gondii. Регистрируемые иммунные дефекты зависят не только от применяемых иммунодепрессантов и отличаются межиндивидуальной гетерогенностью. При СКВ обнаружены дефекты практически в каждом звене иммунной системы.
• Т-клеточная (особенно CD4 + ) лимфопения.
• Подавление реакций ГЗТ, снижение ответа Т-лимфоцитов на Аг и митогены in vitro.
• Характерно увеличение количества периферических Т-лимфоцитов с фенотипом TCR a / b + CD4 – CD8 – (TCR — рецептор T-лимфоцитов, от англ. T cell receptor).
• Поликлональная активация В-лимфоцитов и гипергаммаглобулинемия (наблюдают также гипогаммаглобулинемию и дефицит субклассов IgA и/или IgG).
• Снижение содержания и активности NK-клеток.
• Подавление клеточно-опосредованного иммунного ответа in vitro и in vivo. Интенсивность гуморального ответа варьирует и зависит от Аг.
• Дисфункция макрофагов (снижение иммунного клиренса, Аг-представляющей функции, продукции цитокинов), возможно, вследствие образования аутоантител против рецепторов к Fc-фрагменту IgG.
• Нейтропения и подавление фагоцитарной активности нейтрофилов обусловлены, вероятно, аутоантителами к молекулам адгезии (увеличение клиренса клеток, хроническая аберрантная активация клеток с последующим сниженным ответом на физиологические стимулы).
• При СКВ аутоантитела класса IgM, реагирующие против Т-лимфоцитов, в значительной степени ответственны за депрессию Т-клеточной функции. Имеются сообщения о функциональной асплении в сочетании с сепсисом у больных СКВ.
Ревматоидный артрит. Стойкие изменения функций периферических Т-лимфоцитов при ревматоидном артрите отсутствуют. Имеются отдельные сообщения о незначительных дефектах иммунной защиты, например уменьшении количества цитотоксических Т-лимфоцитов, специфичных к вирусу Эпстайна–Барр, однако системного дефекта цитотоксической функции нет. Гуморальный ответ (на противогриппозную вакцину) и реакция ГЗТ при ревматоидном артрите не изменены.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ, ОБУСЛОВЛЕННЫЕ СРЕДОВЫМИ ВОЗДЕЙСТВИЯМИ
Ультрафиолетовое облучение. УФ-лучи В спектра (УФ-В) — главный фактор риска рака кожи. Существует мнение, что рак кожи развивается не только вследствие прямого мутагенного действия УФ-лучей, но и в результате УФ-опосредованной супрессии иммунных функций кожи. При базально-клеточной карциноме или меланоме УФ-В подавляют индукцию контактной ГЗТ. Лабораторные животные после УФ-облучения характеризуются повышенной чувствительностью к инфекциям.
Токсические химические соединения. Появление новой дисциплины — иммунотоксикологии — свидетельствует об актуальности проблемы иммуноповреждающих эффектов ксенобиотиков. Некоторые из ксенобиотиков с доказанным или вероятным иммунотоксичным действием в отношении людей и животных перечислены ниже. Многие из этих соединений в той или иной степени угнетают костный мозг, подавляют функции Т-лимфоцитов in vivo (атрофия вилочковой железы, ГЗТ) и in vitro (ответ на митогены, Аг, смешанная культура лимфоцитов), вызывают поликлональную активацию В-лимфоцитов (проаутоиммунный эффект), увеличивают частоту инфекций (преимущественно респираторных), повышают риск злокачественных заболеваний (прямое мутагенное действие и/или угнетение функции иммунного надзора).
Химические соединения, приводящие к дисфункциям иммунной системы (По Faist E et al., World J Surg 1966, 20:454)
• Полициклические ароматические углеводороды •• Бензпирены: уменьшают образование АТ •• Бензантрацены: уменьшают активность цитотоксических T-лимфоцитов; канцерогены •• Бензол: вызывает лимфопению; канцероген.
• Полигалогенированные ароматические углеводороды •• Полихлорированные бифенилы: уменьшают активность T-лимфоцитов •• Полибромированные бифенилы: способствуют инфекциям дыхательных путей и лёгких •• полихлорированные дибензофураны, полихлорированные бензодиоксины: подавляют клеточный иммунитет.
• Ароматические амины •• Бензидин: подавляет клеточный иммунитет, канцероген (рак мочевого пузыря).
• Ксенобиотики с эффектами эстрогенов •• ДДТ (дихлордифенилтрихлорэтан): вызывает атрофию вилочковой железы •• Зеараленол: миелотоксикант •• Тетрагидроканнабинол: подавляет клеточный иммунитет •• Диэтилстильбэстрол: подавляет активность NK-клеток и образование АТ.
• Пестициды •• Хлорорганические соединения (в т.ч. ДДТ): вызывают лимфопению •• Фосфорорганические соединения: вызывают атрофию вилочковой железы, уменьшают активность T-лимфоцитов, подавляют образование АТ •• Метил изоцианат: увеличивает количество T-лимфоцитов, но подавляет их активность.
• Содержащие металлы органические соединения •• Органотины: вызывают атрофию вилочковой железы, уменьшают пролиферацию цитотоксических T-лимфоцитов •• Метилированная ртуть: угнетает систему комплемента •• диметилнитрозамин: подавляет образование АТ; канцероген.
• Тяжёлые металлы •• Мышьяк, кадмий, медь, золото, железо, свинец, цинк: подавляют костномозговые ростки, вызывают лимфопению; канцерогены •• Асбест: подавляет все виды иммунитета.
• Поллютанты воздуха •• Озон, диоксид серы: уменьшают сопротивляемость к респираторным инфекциям •• Диоксид азота: подавляет активность альвеолярных макрофагов.
• Токсины грибов •• Охратоксин: подавляет образование АТ •• Трихотецены: подавляют клеточный и гуморальный иммунитет.
• Разные •• Этанол: подавляет все виды и реакции иммунитета.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ, СВЯЗАННЫЕ С ДРУГИМИ СОСТОЯНИЯМИ И ЗАБОЛЕВАНИЯМИ
Кишечная лимфангиэктазия — патологическое расширение лимфатических сосудов слизистой оболочки кишечника, приводящее к потере лимфы, иммуноглобулинов и лимфоцитов через просвет кишечника. Это врождённое заболевание или вторичное состояние, возникающее при обструкции дренирующих лимфатических протоков или повышении ЦВД.
• У больных с рецидивирующими инфекциями и низким содержанием в сыворотке крови IgG могут быть эффективны иммуноглобулины для внутривенного введения. Необходимы высокие дозы ввиду постоянных потерь иммуноглобулинов через кишечник.
Аспления/гипоспленизм. В селезёнке сосредоточено приблизительно 25% фагоцитарного потенциала организма. Она осуществляет иммунный клиренс слабо опсонизированных Аг (т.е. связавших недостаточные количества АТ или комплемента). Поэтому селезёнка приобретает важное значение при первичном и ранних этапах вторичного иммунного ответа на инфекционные Аг, когда высокоаффинные АТ в больших количествах ещё отсутствуют. В селезёнке происходит взаимодействие Т-лимфоцитов, Аг-представляющих клеток и В-лимфоцитов. Селезёнка — главное место активации В-лимфоцитов и важный источник сывороточного IgM.
• Аспления или гипоспленизм увеличивают риск генерализованных инфекций, возбудители которых имеют полисахаридную капсулу: S. pneumoniae, H. influenzae, N. meningitidis. Эти микроорганизмы резистентны к фагоцитозу, если не связаны с достаточным количеством IgG и комплемента.
• При асплении гуморальный ответ к этим и другим возбудителям снижен. Содержание в сыворотке крови IgM ниже нормы, уровень IgG варьирует, содержание IgA может быть повышено. Абсолютное содержание периферических В-лимфоцитов увеличено, в основном вследствие нарушения рециркуляции (кровоток–ткани) и хоминга. Аспления не повреждает клеточный иммунитет.
• При спленэктомии риск инфекции максимален в раннем послеоперационном периоде. Частота сепсиса у взрослых и детей (до 16 лет) без селезёнки составляет 0,9% и 4,2%, соответственно •• Пациентам старше 2 лет за 2 нед до спленэктомии назначают пневмококковую и менингококковую вакцины. Ревакцинацию пневмококковой вакциной проводят через 3–6 лет •• Всем больным показана антибиотикопрофилактика в течение как минимум 3 лет: феноксиметилпенициллин или амоксициллин по 125 мг 2 р/сут для детей младше 5 лет или по 250 мг 2 р/сут для лиц старше 5 лет. Альтернативный режим химиопрофилактики — ко-тримоксазол в суточной дозе 4–5 мг/кг однократно •• Для эмпирической терапии лихорадочных состояний применяют комбинированный препарат амоксициллин + клавулановая кислота.
Аллогенное переливание крови
• Трансфузия крови от донора, несовместимого по Аг главного комплекса гистосовместимости, увеличивает частоту послеоперационных инфекций на 30% и более. Объём перелитой аллогенной крови достоверно коррелирует с риском послеоперационной инфекции.
• При трансфузии лейкоредуцированной крови (истощение лейкоцитов) лабораторным животным проинфекционный эффект отсутствует. В экспериментальных моделях переливание крови вызывает ускорение опухолевого роста и увеличивает смертность.
• Всё большое распространение получает мнение о необходимости трансфузий лейкоредуцированной крови хирургическим и онкологическим пациентам, т.к. аллогенные лейкоциты сенсибилизируют реципиента (фебрильные негемолитические посттрансфузионные реакции), вызывают реакции «трансплантат против хозяина», иммунодепрессию и реактивацию вирусных инфекций.
Беременность. У беременных повышена частота инфекционных заболеваний, контролируемых клеточным иммунным ответом: гепатиты А, В, грипп, герпес, хламидиоз, кампилобактериоз, туберкулёз, грибковые, протозойные инфекции и гельминтозы. Депрессия клеточного иммунитета у беременных, очевидно, имеет физиологический смысл, т.к. позволяет уменьшить вероятность отторжения плода, экспрессирующего отцовские Аг. Имеют значение следующие этиологические факторы:
• Прогестерон подавляет пролиферацию лимфоцитов in vitro, может быть основным иммунодепрессором при беременности.
• Уромодулин — сывороточный фактор, специфичный для беременных, — ингибирует активность В-лимфоцитов, хотя гуморальный ответ при беременности в целом сохранён.
• Сниженный ответ Т-лимфоцитов на митогены наблюдают только в присутствии аутологичной сыворотки, что указывает на значение циркулирующих факторов супрессии.
• При неосложнённой беременности антибиотикопрофилактика банальных инфекций не рекомендована.
Старение. Иммунодефицит в старческом возрасте выражен умеренно, и тяжёлые оппортунистические инфекции (пневмоцистная пневмония, генерализованные грибковые инфекции) нетипичны. С наибольшей частотой возникают реактивация туберкулёза и инфекции, обусловленные вирусом varicella-zoster.
• Снижение секреторной активности слизистых оболочек, потеря эластичности тканей, вегетативная дисфункция способствуют увеличению частоты инфекций дыхательной и мочеполовой систем.
• Фагоцитарная активность (хемотаксис, фагоцитоз, внутриклеточный киллинг) может быть подавлена. Это объясняет меньшее повышение содержания в крови лейкоцитов при инфекциях у пожилых и приводит к незавершённому фагоцитозу.
• Снижение продукции провоспалительных цитокинов ограничивает температурную реакцию у пожилых.
• С возрастом увеличивается количество циркулирующих незрелых Т-лимфоцитов, что отражает нарушение тимус-зависимой дифференцировки вследствие инволюции вилочковой железы. У пожилых также снижен Т-клеточный ответ на митогены, аллоантигены и специфические Аг. Кожная реакция ГЗТ обычно подавлена или отсутствует. При инфицировании M. tuberculosis в возрасте до 55 лет анергию наблюдают в 10% случаев, в возрасте старше 55 лет — в 30%. Содержание Аг-представляющих клеток Лангерханса в коже пожилых снижено вдвое.
• По мере старения нарастает титр аутоантител, снижается титр специфических АТ; количество В-лимфоцитов существенно не меняется. По-видимому, снижение ответа на чужеродные Аг — результат недостаточной активности Т-хелперов, потому что ответ В-лимфоцитов на поликлональные активаторы (митогены, анти-Ig АТ) сохранён в достаточной степени. Вакцинация пожилых менее эффективна по сравнению с молодыми. Нет убедительных доказательств того, что аутореактивные элементы ответственны за развитие широкого круга патологических состояний у пожилых.
• Увеличение частоты злокачественных заболеваний при старении приписывают, по крайней мере отчасти, снижению иммунного надзора. Однако отчётливые доказательства этой связи отсутствуют.
Сокращение. TCR — рецептор T-лимфоцитов (от англ. T cell receptor).
МКБ-10 • D80 Иммунодефициты с преимущественной недостаточностью АТ • D81 Комбинированные иммунодефициты • D83 Обычный вариабельный иммунодефицит • D84 Другие иммунодефициты
Код вставки на сайт
Иммунодефициты вторичные
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ ПРИ НАРУШЕНИЯХ БИОХИМИЧЕСКОГО ГОМЕОСТАЗА
Состояния, приводящие к хроническому дисбалансу гормонов, питательных веществ и токсичных продуктов метаболизма, могут оказывать выраженные эффекты на один или несколько компонентов иммунной системы. В настоящей статье рассмотрены некоторые заболевания и состояния, при которых часто возникает клинически значимая дисфункция иммунной системы.
Сахарный диабет • Дисфункция нейтрофилов у больных СД предрасполагает к грибковым инфекциям • Существует прямая зависимость между степенью гипергликемии и подавлением функций нейтрофилов • Недостаточность микроциркуляции приводит к изъязвлению кожных покровов и ограничению хемотаксиса нейтрофилов к месту внедрения микроорганизмов • Типичные инфекционные осложнения СД — диссеминированный кандидоз, зигомикозы (Absidia, Mortierella, Mucor, Rhizopus) носовой полости и лёгких, а также отит, вызванный Pseudomonas aeruginosa.
Диализ/почечная недостаточность • Пациенты, находящиеся на хроническом гемодиализе, характеризуются подавлением функций Т-лимфоцитов in vitro и in vivo (кожная анергия), угнетением синтеза АТ и активности нейтрофилов, снижением экспрессии и/или функции рецепторов к Fc-фрагменту IgG • Механизм иммунодепрессии при гемодиализе полностью не изучен. Некоторые из иммунных дефектов частично объясняют высоким уровнем эндогенных ГК и применением бионесовместимых диализных мембран, повреждающих клеточную адгезию и ослабляющих фагоцитарный ответ • У больных, длительно находящихся на перитонеальном диализе, в результате потери с диализатом опсонинов (иммуноглобулинов и компонентов комплемента) и прямого супрессивного действия диализата возникает недостаточность функций нейтрофилов брюшины. В совокупности указанные факторы объясняют повышенную частоту бактериальных перитонитов в этой группе больных.
Нефротический синдром. Снижение концентрации многих сывороточных факторов приводит к депрессии иммунной системы у больных с нефротическим синдромом.
• Потеря иммуноглобулинов и белков комплемента увеличивает частоту бактериальных инфекций. Потеря витамина D и сывороточных факторов роста и дифференцировки может вызывать депрессию клеточного иммунитета.
• Иммунодепрессанты, назначаемые по поводу основного заболевания, усугубляют дефицит антиинфекционной резистентности.
• Нарушение питания повышает заболеваемость и смертность от инфекций, вызываемых превалирующими для данного региона возбудителями. Например, смертность от пневмонии и гастроэнтерита увеличивается в 10 и 30 раз, соответственно. В Латинской Америке алиментарная недостаточность выступает в качестве кофактора для 60% летальных исходов вследствие инфекционных заболеваний.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ ПРИ АУТОИММУННЫХ ЗАБОЛЕВАНИЯХ
Аутоиммунное заболевание и иммунодефицит часто сопутствуют друг другу. Как и при микробных инфекциях, умеренные изменения функции иммунной системы обнаруживают практически при всех аутоиммунных заболеваниях. Однако связь между ними и снижением иммунной защиты не так очевидна. Тем не менее при СКВ значение вторичных инфекций, связанных с иммунной дисфункцией, весьма существенно.
СКВ. Инфекции — основной фактор заболеваемости и смертности, а также главная причина летальных исходов 33% больных СКВ. Часто встречающиеся возбудители включают Staphylococcus aureus, E. coli, P. aeruginosa, Salmonella enteritidis, Streptococcus pneumoniae, Neisseria meningitidis, Listeria monocytogenes, Mycobacterium tuberculosis, Herpes zoster, Candida albicans, Cryptococcus neoformans, Pneumocystis carinii, Toxoplasma gondii. Регистрируемые иммунные дефекты зависят не только от применяемых иммунодепрессантов и отличаются межиндивидуальной гетерогенностью. При СКВ обнаружены дефекты практически в каждом звене иммунной системы.
• Т-клеточная (особенно CD4 + ) лимфопения.
• Подавление реакций ГЗТ, снижение ответа Т-лимфоцитов на Аг и митогены in vitro.
• Характерно увеличение количества периферических Т-лимфоцитов с фенотипом TCR a / b + CD4 – CD8 – (TCR — рецептор T-лимфоцитов, от англ. T cell receptor).
• Поликлональная активация В-лимфоцитов и гипергаммаглобулинемия (наблюдают также гипогаммаглобулинемию и дефицит субклассов IgA и/или IgG).
• Снижение содержания и активности NK-клеток.
• Подавление клеточно-опосредованного иммунного ответа in vitro и in vivo. Интенсивность гуморального ответа варьирует и зависит от Аг.
• Дисфункция макрофагов (снижение иммунного клиренса, Аг-представляющей функции, продукции цитокинов), возможно, вследствие образования аутоантител против рецепторов к Fc-фрагменту IgG.
• Нейтропения и подавление фагоцитарной активности нейтрофилов обусловлены, вероятно, аутоантителами к молекулам адгезии (увеличение клиренса клеток, хроническая аберрантная активация клеток с последующим сниженным ответом на физиологические стимулы).
• При СКВ аутоантитела класса IgM, реагирующие против Т-лимфоцитов, в значительной степени ответственны за депрессию Т-клеточной функции. Имеются сообщения о функциональной асплении в сочетании с сепсисом у больных СКВ.
Ревматоидный артрит. Стойкие изменения функций периферических Т-лимфоцитов при ревматоидном артрите отсутствуют. Имеются отдельные сообщения о незначительных дефектах иммунной защиты, например уменьшении количества цитотоксических Т-лимфоцитов, специфичных к вирусу Эпстайна–Барр, однако системного дефекта цитотоксической функции нет. Гуморальный ответ (на противогриппозную вакцину) и реакция ГЗТ при ревматоидном артрите не изменены.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ, ОБУСЛОВЛЕННЫЕ СРЕДОВЫМИ ВОЗДЕЙСТВИЯМИ
Ультрафиолетовое облучение. УФ-лучи В спектра (УФ-В) — главный фактор риска рака кожи. Существует мнение, что рак кожи развивается не только вследствие прямого мутагенного действия УФ-лучей, но и в результате УФ-опосредованной супрессии иммунных функций кожи. При базально-клеточной карциноме или меланоме УФ-В подавляют индукцию контактной ГЗТ. Лабораторные животные после УФ-облучения характеризуются повышенной чувствительностью к инфекциям.
Токсические химические соединения. Появление новой дисциплины — иммунотоксикологии — свидетельствует об актуальности проблемы иммуноповреждающих эффектов ксенобиотиков. Некоторые из ксенобиотиков с доказанным или вероятным иммунотоксичным действием в отношении людей и животных перечислены ниже. Многие из этих соединений в той или иной степени угнетают костный мозг, подавляют функции Т-лимфоцитов in vivo (атрофия вилочковой железы, ГЗТ) и in vitro (ответ на митогены, Аг, смешанная культура лимфоцитов), вызывают поликлональную активацию В-лимфоцитов (проаутоиммунный эффект), увеличивают частоту инфекций (преимущественно респираторных), повышают риск злокачественных заболеваний (прямое мутагенное действие и/или угнетение функции иммунного надзора).
Химические соединения, приводящие к дисфункциям иммунной системы (По Faist E et al., World J Surg 1966, 20:454)
• Полициклические ароматические углеводороды •• Бензпирены: уменьшают образование АТ •• Бензантрацены: уменьшают активность цитотоксических T-лимфоцитов; канцерогены •• Бензол: вызывает лимфопению; канцероген.
• Полигалогенированные ароматические углеводороды •• Полихлорированные бифенилы: уменьшают активность T-лимфоцитов •• Полибромированные бифенилы: способствуют инфекциям дыхательных путей и лёгких •• полихлорированные дибензофураны, полихлорированные бензодиоксины: подавляют клеточный иммунитет.
• Ароматические амины •• Бензидин: подавляет клеточный иммунитет, канцероген (рак мочевого пузыря).
• Ксенобиотики с эффектами эстрогенов •• ДДТ (дихлордифенилтрихлорэтан): вызывает атрофию вилочковой железы •• Зеараленол: миелотоксикант •• Тетрагидроканнабинол: подавляет клеточный иммунитет •• Диэтилстильбэстрол: подавляет активность NK-клеток и образование АТ.
• Пестициды •• Хлорорганические соединения (в т.ч. ДДТ): вызывают лимфопению •• Фосфорорганические соединения: вызывают атрофию вилочковой железы, уменьшают активность T-лимфоцитов, подавляют образование АТ •• Метил изоцианат: увеличивает количество T-лимфоцитов, но подавляет их активность.
• Содержащие металлы органические соединения •• Органотины: вызывают атрофию вилочковой железы, уменьшают пролиферацию цитотоксических T-лимфоцитов •• Метилированная ртуть: угнетает систему комплемента •• диметилнитрозамин: подавляет образование АТ; канцероген.
• Тяжёлые металлы •• Мышьяк, кадмий, медь, золото, железо, свинец, цинк: подавляют костномозговые ростки, вызывают лимфопению; канцерогены •• Асбест: подавляет все виды иммунитета.
• Поллютанты воздуха •• Озон, диоксид серы: уменьшают сопротивляемость к респираторным инфекциям •• Диоксид азота: подавляет активность альвеолярных макрофагов.
• Токсины грибов •• Охратоксин: подавляет образование АТ •• Трихотецены: подавляют клеточный и гуморальный иммунитет.
• Разные •• Этанол: подавляет все виды и реакции иммунитета.
ВТОРИЧНЫЕ ИММУНОДЕФИЦИТЫ, СВЯЗАННЫЕ С ДРУГИМИ СОСТОЯНИЯМИ И ЗАБОЛЕВАНИЯМИ
Кишечная лимфангиэктазия — патологическое расширение лимфатических сосудов слизистой оболочки кишечника, приводящее к потере лимфы, иммуноглобулинов и лимфоцитов через просвет кишечника. Это врождённое заболевание или вторичное состояние, возникающее при обструкции дренирующих лимфатических протоков или повышении ЦВД.
• У больных с рецидивирующими инфекциями и низким содержанием в сыворотке крови IgG могут быть эффективны иммуноглобулины для внутривенного введения. Необходимы высокие дозы ввиду постоянных потерь иммуноглобулинов через кишечник.
Аспления/гипоспленизм. В селезёнке сосредоточено приблизительно 25% фагоцитарного потенциала организма. Она осуществляет иммунный клиренс слабо опсонизированных Аг (т.е. связавших недостаточные количества АТ или комплемента). Поэтому селезёнка приобретает важное значение при первичном и ранних этапах вторичного иммунного ответа на инфекционные Аг, когда высокоаффинные АТ в больших количествах ещё отсутствуют. В селезёнке происходит взаимодействие Т-лимфоцитов, Аг-представляющих клеток и В-лимфоцитов. Селезёнка — главное место активации В-лимфоцитов и важный источник сывороточного IgM.
• Аспления или гипоспленизм увеличивают риск генерализованных инфекций, возбудители которых имеют полисахаридную капсулу: S. pneumoniae, H. influenzae, N. meningitidis. Эти микроорганизмы резистентны к фагоцитозу, если не связаны с достаточным количеством IgG и комплемента.
• При асплении гуморальный ответ к этим и другим возбудителям снижен. Содержание в сыворотке крови IgM ниже нормы, уровень IgG варьирует, содержание IgA может быть повышено. Абсолютное содержание периферических В-лимфоцитов увеличено, в основном вследствие нарушения рециркуляции (кровоток–ткани) и хоминга. Аспления не повреждает клеточный иммунитет.
• При спленэктомии риск инфекции максимален в раннем послеоперационном периоде. Частота сепсиса у взрослых и детей (до 16 лет) без селезёнки составляет 0,9% и 4,2%, соответственно •• Пациентам старше 2 лет за 2 нед до спленэктомии назначают пневмококковую и менингококковую вакцины. Ревакцинацию пневмококковой вакциной проводят через 3–6 лет •• Всем больным показана антибиотикопрофилактика в течение как минимум 3 лет: феноксиметилпенициллин или амоксициллин по 125 мг 2 р/сут для детей младше 5 лет или по 250 мг 2 р/сут для лиц старше 5 лет. Альтернативный режим химиопрофилактики — ко-тримоксазол в суточной дозе 4–5 мг/кг однократно •• Для эмпирической терапии лихорадочных состояний применяют комбинированный препарат амоксициллин + клавулановая кислота.
Аллогенное переливание крови
• Трансфузия крови от донора, несовместимого по Аг главного комплекса гистосовместимости, увеличивает частоту послеоперационных инфекций на 30% и более. Объём перелитой аллогенной крови достоверно коррелирует с риском послеоперационной инфекции.
• При трансфузии лейкоредуцированной крови (истощение лейкоцитов) лабораторным животным проинфекционный эффект отсутствует. В экспериментальных моделях переливание крови вызывает ускорение опухолевого роста и увеличивает смертность.
• Всё большое распространение получает мнение о необходимости трансфузий лейкоредуцированной крови хирургическим и онкологическим пациентам, т.к. аллогенные лейкоциты сенсибилизируют реципиента (фебрильные негемолитические посттрансфузионные реакции), вызывают реакции «трансплантат против хозяина», иммунодепрессию и реактивацию вирусных инфекций.
Беременность. У беременных повышена частота инфекционных заболеваний, контролируемых клеточным иммунным ответом: гепатиты А, В, грипп, герпес, хламидиоз, кампилобактериоз, туберкулёз, грибковые, протозойные инфекции и гельминтозы. Депрессия клеточного иммунитета у беременных, очевидно, имеет физиологический смысл, т.к. позволяет уменьшить вероятность отторжения плода, экспрессирующего отцовские Аг. Имеют значение следующие этиологические факторы:
• Прогестерон подавляет пролиферацию лимфоцитов in vitro, может быть основным иммунодепрессором при беременности.
• Уромодулин — сывороточный фактор, специфичный для беременных, — ингибирует активность В-лимфоцитов, хотя гуморальный ответ при беременности в целом сохранён.
• Сниженный ответ Т-лимфоцитов на митогены наблюдают только в присутствии аутологичной сыворотки, что указывает на значение циркулирующих факторов супрессии.
• При неосложнённой беременности антибиотикопрофилактика банальных инфекций не рекомендована.
Старение. Иммунодефицит в старческом возрасте выражен умеренно, и тяжёлые оппортунистические инфекции (пневмоцистная пневмония, генерализованные грибковые инфекции) нетипичны. С наибольшей частотой возникают реактивация туберкулёза и инфекции, обусловленные вирусом varicella-zoster.
• Снижение секреторной активности слизистых оболочек, потеря эластичности тканей, вегетативная дисфункция способствуют увеличению частоты инфекций дыхательной и мочеполовой систем.
• Фагоцитарная активность (хемотаксис, фагоцитоз, внутриклеточный киллинг) может быть подавлена. Это объясняет меньшее повышение содержания в крови лейкоцитов при инфекциях у пожилых и приводит к незавершённому фагоцитозу.
• Снижение продукции провоспалительных цитокинов ограничивает температурную реакцию у пожилых.
• С возрастом увеличивается количество циркулирующих незрелых Т-лимфоцитов, что отражает нарушение тимус-зависимой дифференцировки вследствие инволюции вилочковой железы. У пожилых также снижен Т-клеточный ответ на митогены, аллоантигены и специфические Аг. Кожная реакция ГЗТ обычно подавлена или отсутствует. При инфицировании M. tuberculosis в возрасте до 55 лет анергию наблюдают в 10% случаев, в возрасте старше 55 лет — в 30%. Содержание Аг-представляющих клеток Лангерханса в коже пожилых снижено вдвое.
• По мере старения нарастает титр аутоантител, снижается титр специфических АТ; количество В-лимфоцитов существенно не меняется. По-видимому, снижение ответа на чужеродные Аг — результат недостаточной активности Т-хелперов, потому что ответ В-лимфоцитов на поликлональные активаторы (митогены, анти-Ig АТ) сохранён в достаточной степени. Вакцинация пожилых менее эффективна по сравнению с молодыми. Нет убедительных доказательств того, что аутореактивные элементы ответственны за развитие широкого круга патологических состояний у пожилых.
• Увеличение частоты злокачественных заболеваний при старении приписывают, по крайней мере отчасти, снижению иммунного надзора. Однако отчётливые доказательства этой связи отсутствуют.
Сокращение. TCR — рецептор T-лимфоцитов (от англ. T cell receptor).
МКБ-10 • D80 Иммунодефициты с преимущественной недостаточностью АТ • D81 Комбинированные иммунодефициты • D83 Обычный вариабельный иммунодефицит • D84 Другие иммунодефициты