что значит когда перекись водорода пенится на ране
Лечение пяточной шпоры
Что же такое пяточные шпоры и откуда они берутся?
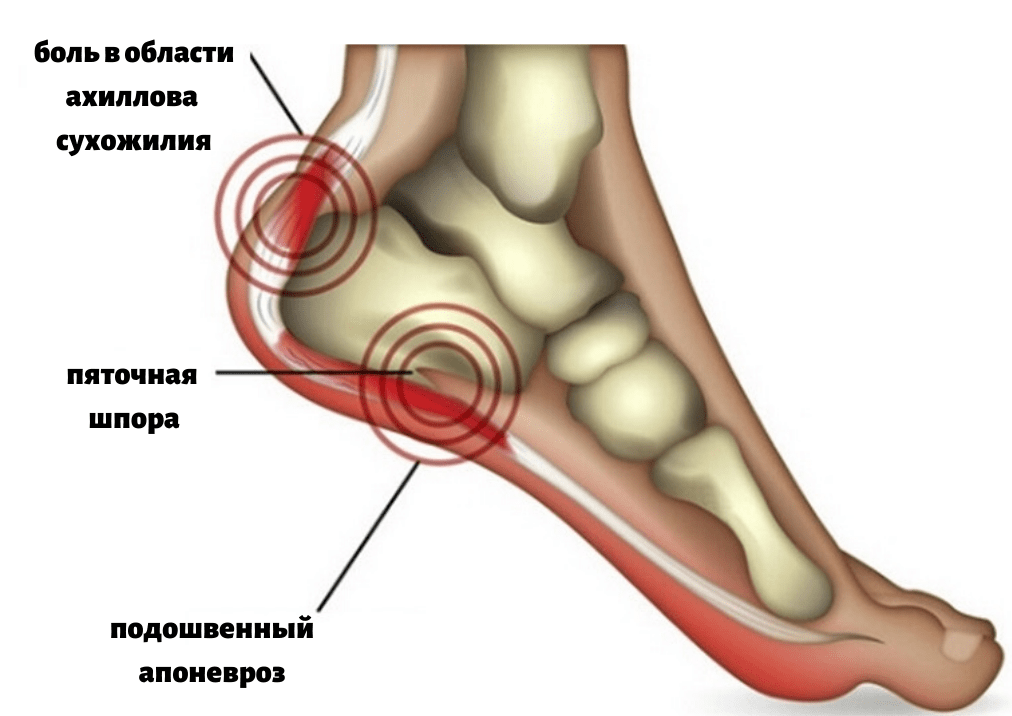
В результате различных процессов (избыточный вес, травма и др.) в данной области возникает хроническая травматизация сухожилия с образованием микронадрывов и постепенное развитие воспалительного процесса. Как компенсаторная реакция на травму и воспалительный процесс начинает образовываться костный вырост, он принимает форму шипа и, передавливая мягкие ткани подошвы стопы, вызывает характерные сильные боли в пяточной области. Самым значимым симптомом пяточной шпоры является сильная боль при ходьбе, особенно в самом начале ходьбы (так называемая, стартовая боль), при вставании со стула, с постели.
Основные причины образования пяточных шпор:
Проявления заболевания
Боли, возникающие при опоре на больную пятку, развиваются постепенно с ростом самой шпоры, характеризуются как жгучие или острые, с ощущением «гвоздя в пятке». Они могут локализоваться на внутренней поверхности больной пятки и переходить на всю стопу. При осмотре пяточной области нет никаких видимых изменений, редко отмечается отечность, болезненность определяется при надавливании на пятку. Интересно, что интенсивность боли не зависит от размера шпоры, что обусловлено, прежде всего, не наличием самой шпоры, а воспалительными изменениями в мягких тканях пятки. Диагноз пяточной шпоры подтверждается рентгенографией.
Основные принципы лечения пяточных шпор
1. Вначале необходимо выяснить причину развития воспалительного процесса в области подошвы и постараться максимально устранить ее. Т.е. выяснить, какой патологический процесс мог привести к избыточной травматизации фасции и возникновению воспаления. С этой же целью следует нормализовать вес, если он избыточный, дозировать физические нагрузки и ношение тяжестей, подобрать удобную, правильную обувь для занятий спортом и для повседневной носки. Снять и отложить в сторону неудобную обувь. На время экспресс-лечения следует ограничить нагрузку на ноги — сократить ходьбу и тем более бег или переноску тяжести насколько это возможно. Лучше носить удобные легкие кроссовки с хорошим супинатором.
2. Необходимо максимально возможное обеспечение физической разгрузки болезненной области, для чего рекомендуется подбор индивидуальных ортопедических стелек с выкладкой внутреннего и наружного продольного сводов, углублением и мягкой прокладкой под пяткой, а также временное ношение подпяточника с углублением или отверстием в центре. Как временную меру при лечении пяточной шпоры можно рекомендовать ношение обуви без задника;
3. Консервативное лечение направленно на ликвидацию воспалительного процесса и включает местное применение нестероидных противовоспалительных препаратов (гели и мази), обладающих противовоспалительным и рассасывающим эффектом. Но эти методы, как правило, приносят лишь только временный эффект, их обязательно нужно сочетать в комплексе с другими методами.
4. Наружное применение мазей при пяточной шпоре лучше сочетать с массажем стоп. Массаж при пяточной шпоре удобно делать самостоятельно.
5. В комплекс лечения пяточной шпоры включают теплые ванны с морской солью, содой. Ванночки необходимо делать перед применением мазей и массажа.
6. Определенные упражнения лечебной гимнастики с проведением массажа мышц стопы и голени — рекомендуются для улучшения кровоснабжения тканей стопы, с этой же целью можно проводить тепловые процедуры парафино- или озокеритотерапии.
7. В некоторых случаях (если развитие пяточной шпоры происходит на фоне артроза) в комплексной терапии рекомендуют прием хондропротекторов с анальгетическим и противовоспалительным эффектом, что останавливает прогрессивный воспалительный процесс, но эффект от внутреннего применения препаратов развивается только через 6 недель от начала лечения и сохраняется в течение 2–3 мес. после его отмены.
8. Методы медикаментозного лечения пяточной шпоры.
Официальная медицина на сегодняшний день разработала большое количество схем фармакологической терапии данного заболевания. Среди препаратов, применяемых для лечения пяточной шпоры: нестероидные противовоспалительные средства, гели, мази, кремы и пластыри для лечения пяточной шпоры местного применения, обладающие рассасывающим и противовоспалительным эффектом.
При малой эффективности консервативного лечения выполняются лекарственная блокада пяточной шпоры — обкалывание болезненного места шприцом с лекарственным веществом. Например, стойким эффектом обладает однократное местное введение дипроспана.
Препараты, применяемые с этой целью, оказывают выраженный местный противовоспалительный эффект, что быстро подавляет воспалительный процесс и снижает болевой синдром.
Данная процедура требует знаний и большого опыта, поэтому проводить ее может только квалифицированный специалист. Однако при частом использовании метода возможно разрушение связки или фасции.
9. К хирургическому лечению прибегают крайне редко, так как встречается много недостатков при данной методике. При проведении операции удаляют пяточную шпору. После чего конечность фиксируют гипсовой повязкой примерно на один месяц.
После снятия гипса назначают ортопедические стельки и проводят курсы восстановительного лечения. Помните, что в большинстве случаев пяточные шпоры вполне поддаются терапии и без операций.
10. Любой метод лечения необходимо сочетать с физиотерапевтическими воздействиями.
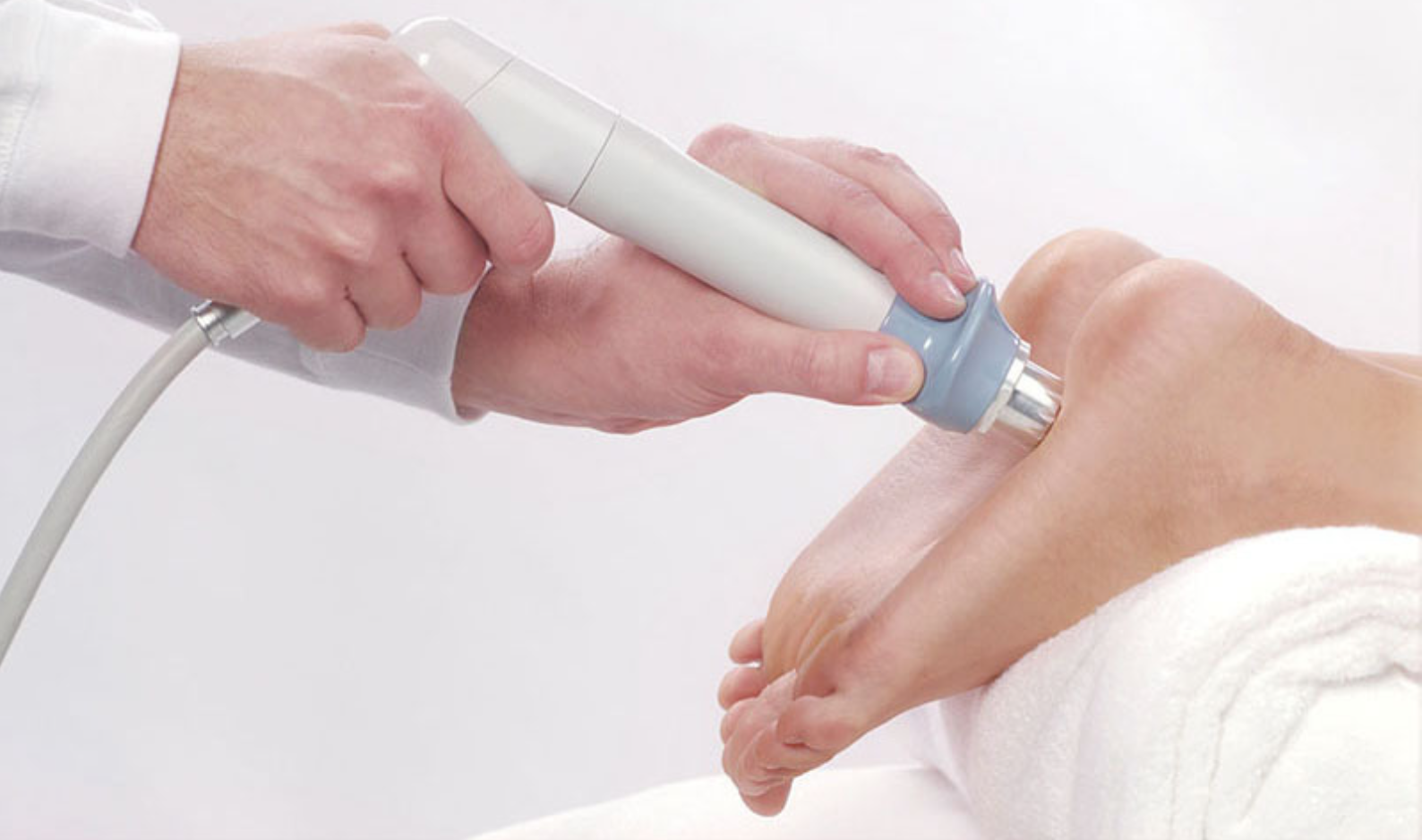
Ударно-волновая терапия пяточной шпоры
Является наиболее эффективным методом: терапия воздействует непосредственно на костные разрастания и способствует их уменьшению или даже рассасыванию. Ударно-волновая терапия — относительно новый метод лечения.
В нашей стране данная процедура начала практиковаться не очень давно, но первые результаты уже обнадеживают.
Имеющийся опыт позволяет утверждать, что при использовании данного метода лечения эффективность лечения пяточной шпоры очень высока. Метод основан на воздействии импульсов ударных волн определенной частоты. Эффект ударной волны разрыхляет отложения кальция в пяточной шпоре.
Это позволяет в дальнейшем вымывать разрыхленные отложения из организма с кровотоком. Пораженная связка избавляется таким образом от накопленных солей кальция.
Кроме того, при этом активизируются процессы регенерации тканей, уменьшаются отечность и воспалительные явления. С каждой проведенной процедурой болевой синдром становится все меньше и, как правило, значительно уменьшается или исчезает к концу лечения.
Пораженный участок во многом восстанавливает свою естественную структуру и возвращает себе способность переносить каждодневные нагрузки, не вызывая болезненных ощущений.
На начальных стадиях заболевания лечение требует небольшого количества процедур от 3 до 5 на курс, а при большой длительности процесса длительность лечения до 5-10 процедур на курс. Между сеансами обязателен перерыв 5-7 дней.
Продолжительность одного сеанса составляет 15-20 минут на одно поле. На кожу пятки наносят специальный гель, воздействие осуществляется с помощью излучателя.
Существуют противопоказаниями к лечению пяточной шпоры: нарушения свертываемости крови и тромбофлебит, злокачественные новообразования, беременность.
Нежелательно проведение процедур ударно-волновой терапии в течение месяца после введения в область пятки гормональных противовоспалительных препаратов.
Лучевая терапия (рентгенотерапия) пяточной шпоры
Использование рентгеновского излучения в лечении пяточной шпоры показывает весьма эффективные результаты. Метод заключается в том, что на область пятки направляются четко сфокусированные рентгеновские лучи, несущие пониженную дозу радиации.
Они вызывают блокирование нервных окончаний, и пациент перестает испытывать болевые ощущения.
Курс лечения чаще всего состоит из десяти сеансов, каждый из которых имеет продолжительность в 10 минут.
Рентгенотерапия в лечении пяточной шпоры обладает следующими преимуществами: полная безболезненность процедуры, высокая эффективность, минимум противопоказаний, воздействие излучения только на пяточную шпору, противоаллергическое и противовоспалительное действие, возможность амбулаторного лечения.
Противопоказанием к использованию данного метода является только беременность.
При применении рентгенотерапии сама шпора не исчезает, блокируются только болевые ощущения, исходящие от нее. Поэтому после проведения курса рентгенотерапии необходимо обязательной позаботиться о разгрузке стопы.
Лазерное лечение пяточной шпоры
В настоящее время низкоинтенсивная лазерная терапия — популярный и достаточно широко используемый метод лечения данного заболевания. Лазерная терапия воздействует на мягкие ткани, находящиеся вокруг шпоры.
Сфокусированное излучение вызывает увеличение кровообращения в области воспаления, что способствует уменьшению болей.
Среди пациентов бытует мнение о том, что лазерная терапия способна устранять саму пяточную шпору. Однако это является заблуждением. Проникая в ткани стопы, низкоинтенсивный лазерный луч на сам костный нарост не оказывает практически никакого действия.
Его эффект проявляется только на мягких тканях. А значит, после проведения курсов лазерной терапии также необходимо применять все методы, направленные на профилактику данного заболевания.
УВЧ-СВЧ-терапия
Этот метод заключается в применении переменного электромагнитного поля ультравысокой и сверхвысокой частоты. Влияние этих токов приводит к расширению капилляров в мягких тканях и к значительному усилению кровообращения. При этом уменьшается болевой синдром и воспаление.
Длительность одного сеанса составляет 10-15 минут. Для лечения пяточной шпоры требуется около 10-12 сеансов терапии.
Чаще врачи назначают пациентам переменное магнитное поле. Образуются слабые токи в крови и лимфе, которые влияют на метаболизм, а также на структуру воды и белков. Повышается сосудистая и кожная проницаемость, рассасываются отеки, уменьшается воспаление.
Данная методика позволяет достичь те же результаты, что и УВЧ-терапия.
Лечить шпоры на пятке можно и с помощью электрофореза или СМТ-ДДТ-фореза
Электрический ток повышает ионную активность в проводящих тканях, при этом увеличивается синтез многих биологически активных веществ. Лечебное действие обусловлено поступлением ионов лекарственных веществ (именно в ионной форме вещества наиболее активны), а также формированием кожного депо, из которого ионы постепенно поступают в ткани в последующие дни.
При электрофорезе используют специальные прокладки, пропитанные лекарством. Прокладки располагают между кожей пятки и пластинами электродов. Для лечения пяточной шпоры используют йодистый калий, гидрокортизон, новокаин и прочие препараты.
Эффективность таких методов физиолечения, как ультразвука и фонофореза (сочетанное применение ультразвука и лекарственного препарата) при пяточных шпорах составляет более 30%.
Основной эффект физиотерапии ультразвуком при лечении пяточной шпоры заключается в устранении воспалительного процесса, учитывая, что лучше всего ультразвук поглощается костной тканью.
При этом не следует бояться, что ультразвуковое лечение будет влиять на здоровую костную ткань пятки. Проведенные исследования низкочастотным ультразвуком показали, что разрушений костных тканей не вызывалось, но локальное применение ультразвуковых волн на область шпоры способствовало снижению содержания в ней кальция с замещением волокнистой соединительной тканью.
Также ультразвук оказывает рассасывающее и спазмолитическое действие, улучшая процессы локальной микроциркуляции.
Эффект от ультразвукового лечения усиливается сочетанным применением противовоспалительных мазевых препаратов. Озвучивание низкочастотным ультразвуком повышает проницаемость клеточных мембран, улучшает проницаемость и введение лекарственных веществ.
Наиболее часто применяют гидрокортизоновую мазь. Фонофорез способствует более глубокому проникновению лекарственного вещества в пораженную область, нежели применять мазь как самостоятельное средство лечения.
Метод фонофореза основан на свойстве ультразвука изменять проницаемость кожных покровов, в связи с чем лекарства, нанесенные на кожу, всасываются более активно.
Продолжительность самой процедуры — до 10 минут. На курс лечения может понадобится 5-10 процедур, с возможными повторными курсами.
Профилактика пяточной шпоры
Профилактические меры должны быть направлены, в первую очередь, на предупреждение преждевременного износа, старения и травм костно-суставного аппарата:
Водорода перекись (раствор) : инструкция по применению
Лекарственная форма
Раствор для наружного применения 3 %
Состав
100 мл препарата содержат
(в зависимости от фактического содержания водорода пероксида в исходном препарате);
вспомогательные вещества: натрия бензоат, вода очищенная.
Описание
Бесцветная, прозрачная жидкость без запаха
Фармакотерапевтическая группа
Антисептики и дезинфицирующие препараты прочие
Фармакологическое действие
Данные по фармакокинетике водорода перекиси для наружного применения не представлены.
Антисептическое средство из группы оксидантов. Обладает также гемостатическим эффектом. При контакте перекиси водорода с поврежденной кожей и слизиcтыми оболочками высвобождается активный кислород, при этом происходит механическое очищение раны и инактивация органических веществ (протеины, кровь, гной). Антисептическое действие перекиси водорода не является стерилизующим, при его применении просходит лишь временное уменьшение количества микроорганизмов. Обильное пенообразование способствуют тромбообразованию и остановке кровотечений из мелких сосудов.
Показания к применению
— первичная обработка поверхностных загрязненных ран, очищение раны от гноя
— для обработки слизистых оболочек при стоматитах, ангинах, гинекологи-ческих заболеваниях
— остановка капиллярных кровотечений из поверхностных ран, носовых кровотечений.
Способ применения и дозы
Для обработки ран раствор наносят на поврежденный участок кожи.
Для полоскания растворяют одну столовую ложку водорода перекиси в стакане воды.
Пораженный участок обрабатывают марлевым или ватным тампоном, смоченным раствором водорода перекиси.
Продолжительность лечения зависит от достигнутого эффекта.
Что значит когда перекись водорода пенится на ране
Кровоподтеки кожи давно являются привычными исходами травм и некоторых медицинских процедур [6, 8, 9, 14]. Несмотря на то, что кожа в местах кровоподтеков и синяков воспаляется, теряет нормальную структуру и функцию, официальная медицина до сих пор не признает эту патологию самостоятельным заболеванием [11]. Поэтому отсутствует стандарт его лечения и не разработаны специальные отбеливающие лекарственные средства [12].
Однако в 2013 году ситуация кардинально изменилась, поскольку впервые было предложено выделить кровоподтеки кожи пациентов в местах инъекций в самостоятельное заболевание, которое получило название «Инъекционная болезнь кожи» [9, 11]. При этом специальные средства профилактики и лечения кровоподтеков до сих пор отсутствуют.
Тем не менее, в последние годы достигнуты значительные успехи в разработке чистящих, моющих и отбеливающих средств, которые находят широкое применение в быту в борьбе с загрязнениями унитазов, ванн, раковин и медицинских халатов различными биологическими тканями, включая пятна крови. Но данные гигиенические средства не пригодны для инъекций и аппликаций с целью отбеливания кожи в местах кровоподтеков, поскольку имеют чрезмерно высокую физико-химическую агрессивность, поскольку они способны вызвать газовую эмболию, некроз тканей и острое отравление, характерное для поверхностно активных веществ (ПАВ). Тем не менее, их состав может быть учтен для создания новой фармакологической группы лекарств – отбеливателей кровоподтеков. Дело в том, что аналогичный научный подход (обеспечение фармакологической активности за счет определенных физико-химических свойств растворов лекарственных средств) был успешно использован нами ранее при разработке новой фармакологической группы лекарств – пиолитических средств, которые способны эффективно разжижать не только густой гной, но и сгустки крови [1, 2, 3, 4, 5, 7, 13].
Цель исследования – разработать отбеливатель кровоподтеков кожи и подкожно-жировой клетчатки.
Материалы и методы исследования
Проведены лабораторные исследования с использованием стандартных ватно-марлевых тампонов и консервированной донорской крови. В опытах использовалась просроченная на 5 дней консервированная донорская кровь, которая перед опытами дополнительно разводилась водой для инъекций с целью гемолиза. Для этого за 10 минут до применения определенная порция крови разводилась дистиллированной водой в соотношении 1/5 при температуре + 25 °С. Сухие ватно-марлевые тампоны опускались на сухое дно чашек Петри так, чтобы плоскость тампонов располагалась горизонтально, после этого в центр каждого тампона вводилось по 3 капли гемолизированной крови. Затем тампоны инкубировались 10 минут при температуре + 25 °С.
После этого кровавые тампоны пропитывались исследуемыми растворами при температуре + 25 °С с помощью медицинского шприца, соединенного с инъекционной иглой, предназначенной для подкожных инъекций. Исследуемые растворы вводились в объеме 20 мл в центр каждого кровавого пятна в течение 60 секунд. Динамика изменения цвета тампонов регистрировалась с помощью цветной киносъемки, после чего полученные результаты воспроизводились на экране компьютера и анализировались с помощью специальной программы. При этом исследовалось газообразование, определялась площадь зоны полного обесцвечивания тампона и длительность времени, необходимого для обесцвечивания тампона.
Статистическая обработка результатов проведена с помощью программы BIOSTAT по общепринятой методике.
Результаты исследования
и их обсуждение
В качестве прототипов и аналогов нового фармакологического средства нами были использованы распространенные бытовые отбеливатели и средство, указанное в «Способе экспресс удаления пятен крови с одежды» [2]. Проведенный нами анализ состава указанных средств показал, что фармакологическое средство, претендующее на роль нового медицинского отбеливателя, вероятнее всего, должно включать следующие ингредиенты:
– натрия гидрокарбонат (то есть «съедобную» щелочь, а именно – питьевую соду);
– динатриевую соль ЭДТУ (то есть клещевидное соединение, комплексон);
– перекись водорода (химический аккумулятор кислорода).
При этом натрия гидрокарбонат – это самый безопасный естественный щелочной буфер, который обеспечивает щелочность плазмы крови. Натриевая соль ЭДТА (этилендиаминтетраацетат натрия) – это безопасный комплексон, который обеспечивает инактивацию ионов железа, освобождающихся после гемолиза эритроцитов и азрушения гемоглобина за счет его клещевидного «связывания». Перекись водорода – это самая безопасная неорганическая кислота, способная выделять молекулярный кислород под действием каталазы крови.
Перед проведением лабораторных исследований нами были проведены теоретические расчеты, направленные на обоснование состава и концентрации ингредиентов разрабатываемого отбеливателя. Анализ литературных данных показал, что разрабатываемый отбеливатель должен содержать натрия гидрокарбонат в концентрации 1,8 % и динатриевую соль ЭДТУ – в концентрации 0,25 %, поскольку именно такое их содержание обеспечивает осмотическую активность в пределах 285–295 мОсмоль/л воды, щелочность в пределах рН 8,4, а также умеренную буферную и комплексообразующую активность раствора при отсутствии токсичности и местного раздражающего действия.
Более трудной задачей оказалось выяснение требуемой концентрации перекиси водорода. Опираясь на наш прежний опыт разработки лекарственных средств, включающих перекись водорода, мы исходили из того, что концентрация перекиси водорода, обеспечивающая обесцвечивание крови без выделения газа, находится в диапазоне ниже 0,05 %. В связи с этим нами были проведены лабораторные исследования, направленные на конкретизацию искомого диапазона концентраций перекиси водорода. Для этого все испытуемые растворы содержали перекись водорода в диапазоне от 0,05 до 0,008 %.
Проведено 9 серий опытов с растворами, включающими 1,8 % натрия гидрокарбоната и 0,25 % динатриевой соли этилендиаминтетрауксусной кислоты, которые дополнительно содержали перекись водорода в концентрации (соответственно) 0,05 %, 0,04 %, 0,035 %, 0,03 %, 0,02 %, 0,015 %, 0,01 %, 0,0095 %, 0,009 или 0,008 %.
Растворы вводились в кровавые ватно-марлевые тампоны по единой схеме. При этом было установлено следующее.
В первой серии опытов центры кровавых пятен в тампонах красного цвета после введения в них раствора (содержащего 0,05 % Н2О2) начинали моментально светлеть с образованием пузырьков газа и пены. Образовавшиеся пузыри сохранялись в кровавой пене 10,3 ± 0,3 минут (Р ≤ 0,05, n = 5). При этом центр кровавого пятна практически полностью обесцвечивался, а площадь обесцвеченного участка составляла 64 ± 2,5 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови при этом приобретала светло-желтый цвет.
Во второй серии опытов центры кровавых пятен в тампонах красного цвета после введения в них раствора (содержащего 0,04 % Н2О2) начинали светлеть моментально с образованием пузырьков газа и пены. Образовавшиеся пузыри сохранялись в кровавой пене 7 ± 0,1 минут (Р ≤ 0,05, n = 5), после чего образование пузырьков газа прекращалось. Центр кровавых пятен практически полностью был обесцвечен, а площадь обесцвеченного участка составляла в среднем 49 ± 2,0 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала светло-желтый цвет.
В третьей серии опытов центры кровавых пятен в тампонах красного цвета после введения в него раствора (содержащего 0,035 % Н2О2) начинали моментально светлеть со слабым образованием пузырьков газа без пены. Образовавшиеся пузыри лопались и через 1,5 ± 0,08 минут (Р ≤ 0,05, n = 5) образование пузырьков газа прекращалось. При этом центры кровавых пятен оказывались бесцветными, а их площадь составляла в среднем 36 ± 0,9 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятен крови приобретала желтый цвет.
В четвертой серии опытов центр кровавых пятен в тампонах после введения в него раствора (содержащего 0,03 % Н2О2) начинал светлеть без образования пузырьков газа и пены практически моментально. Через 2 ± 0,1 секунд (Р ≤ 0,05, n = 5) центр кровавого пятна во всех тампонах был лишен красной окраски и оказался почти бесцветным (площадь его составила 29 ± 0,6 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала желто-желто-оранжевый цвет.
В пятой серии опытов центры кровавых пятен в тампонах начинали быстро светлеть после введения испытуемого раствора (содержащего 0,02 % Н2О2) без образования пузырьков газа и пены. Уже через 4 ± 0,15 секунд (Р ≤ 0,05, n = 5) центр кровавых пятен был лишен красной окраски, стал бесцветным, а площадь его составила в среднем 19 ± 0,7 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови в тампонах приобретала оранжево-желтый цвет.
В шестой серии опытов центры кровавых пятен в тампонах начинали светлеть после введения испытуемого раствора (содержащего 0,01 % Н2О2) без образования пузырьков газа и пены. Через 5 ± 0,19 секунд (Р ≤ 0,05, n = 5) центр кровавых пятен терял красный цвет и становился бесцветным, а площадь его составляла в среднем 14 ± 0,6 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала оранжево-желтый цвет.
В седьмой серии опытов центры кровавых пятен в тампонах начинали светлеть после введения испытуемого раствора (содержащего 0,0095 % Н2О2) без образования пузырьков газа и пены. Через 6 ± 0,17 секунд (Р ≤ 0,05, n = 5) центр кровавых пятен терял красный цвет и становился бесцветным, а площадь его составляла 11 ± 0,5 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала оранжевый цвет.
В восьмой серии опытов центры кровавых пятен в тампонах начинали светлеть после введения испытуемого раствора (содержащего 0,009 % Н2О2) без образования пузырьков газа и пены. Через 10 ± 0,3 секунд (Р ≤ 0,05, n = 5) центр кровавых пятен терял красный цвет и становился бесцветным, а площадь его составляла в среднем 9 ± 0,35 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала красно-оранжевый цвет.
В девятой серии опытов центры кровавых пятен (имевшие красный цвет) после введения в них раствора (содержащего 0,008 % Н2О2) начинали светлеть без образования пузырьков газа и пены. Через 15 ± 0,8 секунд (Р ≤ 0,05, n = 5) они теряли цвет и становились бесцветными, а их площадь составляла в среднем 6 ± 0,15 мм2 (Р ≤ 0,05, n = 5). Периферическая зона пятна крови приобретала красно-оранжевый цвет.
Следовательно, водные растворы 1,8 % натрия гидрокарбоната и 0,25 % динатриевой соли этилендиаминтетрауксусной кислоты при внесении к ним перекиси водорода в диапазоне концентраций 0,05–0,03 % обесцвечивают кровавые тампоны, но с бурным и длительным образованием газа. Поэтому они не годятся для подкожных и внутрикожных инъекций.
Водные растворы 1,8 % натрия гидрокарбоната, 0,25 % динатриевой соли этилендиаминтетрауксусной кислоты и 0,03–0,01 % перекиси водорода эффективно и быстро обесцвечивают кровавые тампоны без образования газа. Следовательно, растворы именно такого состава более всего пригодны для обесцвечивания кровоподтеков. Они обеспечивают полное обесцвечивание окровавленных тампонов за 10–15 секунд без образования пузырьков газа и пены. Данное средство получило название «Отбеливатель кровоподтеков» (решение ФИПС от 28 октября 2014 года о выдаче патента на изобретение по заявке № 2014101094).
Изобретенный нами отбеливатель кровоподтеков состоит из следующих компонентов (в ас. %):
Натрия гидрокарбонат 1,8
Этилендиаминтетраацетат натрия 0,25
Перекись водорода 0,03–0,01
Вода для инъекций Остальное
Вслед за этим нами были проведены первичные испытания отбеливающего средства при внутрикожных инъекциях в области трупных пятен у 2-х трупов. Результаты проведенных исследований подтвердили высокую отбеливающую активность изобретенного «Отбеливателя кровоподтеков» при инъекциях в места трупных пятен без образования газа в тканях.
По нашему мнению поставленная цель достигается за счет следующих физико-химических факторов:
1. За счет водного изотонического раствора, обеспечивающего разбавление (разведение) межклеточной коллоидной жидкости с «красителем» и удаление его с собой при последующем всасывании в кровь;
2. За счет ощелачивающего окислителя, обеспечивающего размягчение, разрыхление межклеточной коллоидной среды и углубление в нее при одновременном ускорении процесса биотрансформации «красителя» без газовой эмболии и эмфиземы тканей;
3. За счет комплексообразователя, обеспечивающего конъюгацию и ускоряющего инактивацию органических и неорганических составных ингредиентов «красителя», а также растворимых и нерастворимых солей железа.
Водный раствор, состоящий из 1,8 % гидрокарбоната натрия, 0,25 % динатриевой соли этилендиамитетрауксусной кислоты и 0,03 – 0,01 % перекиси водорода представляет собой водный изотонический раствор с окислительной, комплексообразующей и щелочной активностью. Предложенный состав ингредиентов и соотношение их концентрации в водном растворе являются оптимальными для придания ему способности извлекать железо из его нерастворимых солей, замещать его при этом на растворимые соли натрия и образовывать хелатные (клещевидные) соединения с железом растворимых и нерастворимых солей железа без образования пузырьков газа и без оказания денатурирующего действия на клетки кожи и подкожно-жировой клетчатки, а также без общего токсического действия на человека, то есть без его отравления.
При этом катионы натрия и предложенное их суммарное количество в растворе обеспечивают условия биофизического (электрофизиологического) покоя для клеток, поскольку концентрация внеклеточных катионов натрия соответствует концентрации, сопровождающей электрофизиологический «потенциал покоя» в мембранах клеток нашего организма.
Гидрокарбонат натрия в предложенной концентрации создает собой аналог физиологического «гидрокарбонатного» буфера, являющегося основным буфером плазмы крови и внеклеточной жидкости человека, придает раствору стабильную щелочную активность в пределах рН 8,4, способность разжижать жир, кровь, межклеточную жидкость, лимфу, а также улучшает диффузию водного раствора в коже и в подкожно-жировой клетчатке, ускоряет рассасывание постинъекционного инфильтрата, появляющегося в тканях при внутрикожной и/или подкожной инъекции. При этом щелочной раствор не вызывает щелочной ожог тканей.
Динатриевая соль этилендиаминтетрауксусной кислоты в предложенной концентрации придает раствору способность связывать 2-х валентные катионы железа из раствора, а также извлекать железо из нерастворимых солей и связывать их за счет комплексообразования с ЭДТУ. Последующее удаление связанного железа из области кровоподтека с рассасывающимся раствором отбеливателя кровоподтеков уменьшает интенсивность окраски области кровоподтека.
Перекись водорода в предложенной концентрации придает раствору достаточную окислительную активность, но исключает образование пузырьков газа кислорода при инъекции раствора в кожу и/или в подкожно-жировую клетчатку в области кровоподтека, то есть исключает холодное кипение в тканях при инъекции в них.
Разработанный нами «Отбеливатель кровоподтеков» может быть введен в кожу и в подкожно-жировую клетчатку с помощью инъекций. Инъекционное введение средства в окрашенную зону кожи и/или подкожно-жировой клетчатки обеспечивает уменьшение интенсивности ее цвета за счет ускоренного окислительного разрушения восстановленного гемоглобина, метгемоглобина, вердохромогена, биливердинибилирубина и других «цветных» органических и неорганических соединений («красителей»). Необходимая окислительная трансформация цветных соединений обеспечивается выделением молекулярного кислорода из перекиси водорода на границе сред под действием каталазы крови в условиях оптимальной щелочной и осмотической активности. Кроме этого, раствор уменьшает интенсивность окраски тканей за счет своей разводящей, проникающей (за счет омыляющей активности) и промывающей активности, обеспеченных его изотонической и оптимальной щелочной активностью. Промывающая и проникающая активность раствора улучшает диффузию раствора в тканях в области кровоподтека и последующее всасывание раствора в общее кровеносное русло вместе с «красителями» из области инфильтрата, образованного инъекцией, за счет ускоренного рассасывания постинъекционного инфильтрата.