какие железоуглеродистые сплавы называют сталями
Особенности и маркировка железоуглеродистых сплавов
Железоуглеродистые сплавы — соединения на основе железа и углерода. Первый выступает главным компонентом, а второй второстепенным. Также в составе присутствуют сторонние примеси — марганец, кремний, фосфор, сера. Эти соединения применяются в разных сферах промышленности.

Общие сведения
Железоуглеродистые сплавы — группа соединений на основе железа, насыщаемые дополнительными компонентами, главным из которых является углерод.
Железоуглеродистые сплавы делятся на 2 больших группы:
В отдельную группу нужно выделить специальные чугуны, второе название которых — ферросплавы. Они содержат марганец и кремний. Применяются для производства стали. С их помощью можно убрать вредную примесь, которая ухудшает технические характеристики.
Промышленное получение
Железоуглеродистые сплавы производятся металлургическими заводами из разных компонентов. Основа — железо с углеродом. Этапы производственного процесса:
Для производства чугуна применяются большие доменные печи. Их высота может достигать 30 м, а внутренний диаметр — 12 м.
Доменная печь (Фото: Instagram / viktormacha)
Компоненты сплавов
Технические характеристики железоуглеродистых сплавов зависят от типа и количества легирующих добавок:
Классификация
Сталь классифицируется по разным признакам. По химическому составу:
Маркировка
Свойства
Характеристики железоуглеродистых сплавов:
Железоуглеродистые сплавы производятся промышленными предприятиями. К ним относятся разные виды стали, чугуна. Они применяются в разных сферах промышленности.
Железоуглеродистые сплавы. Свойства, виды, диаграммы сплавов
1. Железоуглеродистые сплавы
1.1. Железо
Железо относится к главному химическому элементу в группе черных металлов. В чистом виде железо в природе не встречается, а встречается в виде оксидов, образующих так называемую железную руду с различным содержанием железа.
Кристаллическая решетка железа — ОЦК, но при повышении температуры она меняется. При нагревании до температуры 150 … 250 °С чистое железо, взаимодействуя с кислородом, покрывается оксидной пленкой. Технически чистое железо пластично. При незначительных массовых долях примесей (не более 0,01 %) пластичность резко уменьшается. Чистое железо в связи с низкими механическими свойствами практического применения не находит.
Металлургическая промышленность для научных исследований производит несколько сортов технически чистого железа: чистейшее, электролитическое, карбональное, техническое.
Указанные сорта чистого железа имеют различные механические свойства. Например, предел прочности σв = 180 … 320 МПа (18 … 32 кгс/мм 2 ), относительное удлинение δ = 30 … 50 % зависят от сорта железа. Пластичность железа зависит от температуры испытания.
При незначительном нагревании чистое железо становится хрупким. Исследования показали, что железо имеет три зоны хрупкости:
Свойства хрупкости у железа проявляются в зависимости от типа атомной кристаллической решетки и ее параметров. Химические элементы (примеси) увеличивают или понижают температуру ломкости (синеломкости) железа. Так, например, кислород увеличивает, а углерод и марганец понижают температуру ломкости. Кроме того, практика показывает, что прочность и пластичность железа зависят от способа производства исследуемых образцов. Литые образцы имеют пониженную прочность и пластичность по сравнению с образцами, полученными деформированием (прокаткой, ковкой). Деформируемое железо прочнее литого.
Железо в твердом состоянии в зависимости от температуры может находиться в двух модификациях: α-железо и γ-железо. При нагревании и охлаждении происходят аллотропные превращения, в результате которых идет перестройка атомных решеток. Кроме того, важным фактором является способность железа растворять углерод, азот и водород, а также различные металлы. При этом с металлами образуются твердые растворы замещения, а с углеродом, азотом и водородом — растворы внедрения.
Особую роль в образовании твердых растворов внедрения играет углерод, который растворяется как в α-железе, так и в γ-железе. Наибольшая растворимость углерода в γ-железе составляет 2,14 % (на диаграмме состояния Fе— Fе3С критическая температура 1 147 °С).
Чистое железо получить практически невозможно. В настоящее время получают железо с массовой долей различных примесей от 0,01 %. Например, Армко-железо — техническое железо, получаемое в мартеновских печах и применяемое для научных исследований, — имеет массовую долю примесей 0,1 … 0,2 %.
Практика показывает, что углерод, сплавляясь с железом, способствует резкому возрастанию механических свойств — увеличиваются твердость, износостойкость, упругость и прочность. Уменьшается пластичность и ударная вязкость. В связи с этим в практике широкое применение нашли сплавы железа с углеродом и другими элементами.
1.2. Характеристика железоуглеродистых сплавов
Железоуглеродистым сплавом называется сплав железа, насыщенный углеродом и другими химическими элементами в процессе доменной плавки или иного металлургического процесса. Железоуглеродистые сплавы являются основными конструкционными материалами и представляют большую группу, как по объему производства, так и по многообразию различных марок.
Железоуглеродистые сплавы по физико-химическим и механическим свойствам подразделяются на две большие группы: стали и чугуны.
Сталь — это сплав железа с углеродом, в котором массовая доля углерода составляет до 2,14 % (теоретически). На практике обычно массовая доля углерода составляет 1,3 … 1,5 %. Углеродистая сталь — это деформируемый, ковкий и прочный конструкционный материал, предел прочности которого достигает 1 150 МПа, твердость — 285 НВ и относительное удлинение — 32 %. Сталь имеет хорошую обрабатываемость резанием, сваривается и обрабатывается давлением.
Чугун — это сплав железа с углеродом, в котором массовая доля углерода составляет 2,14 … 6,67 % (теоретически). На практике применяются чугуны с массовой долей углерода 2,5 … 5,0 %. Свойства чугуна зависят от его структуры, т. е. от взаимодействия углерода с железом.
В зависимости от структуры чугун будет обладать теми или иными физико-механическими свойствами. При наличии зернистой структуры чугун будет обладать высокой твердостью и прочностью, а также высокой обрабатываемостью.
Большая часть товарного чугуна перерабатывается в сталь.
1.3. Фазы и структуры железоуглеродистых сплавов.
Железоуглеродистый сплав в зависимости от физических условий (температура, давление) может находиться в трех фазовых состояниях:
Каждая из этих фаз, несмотря на однородность химического состава, имеет различные физические и механические свойства. При изучении свойств железоуглеродистых сплавов научно-практический интерес представляют различные структуры твердой фазы, которые при взаимодействии с углеродом образуют железо (например, химическое соединение цементит, твердые растворы аустенит и феррит, механические смеси перлит и ледебурит).
Цементит — это химическое соединение углерода с железом (карбид железа) Fe3C. Структура цементита представляет собой сложную ромбическую атомно-кристаллическую решетку со слабой металлической связью. Температура начала плавления цементита — 1 147 °С, конца плавления — 1 600 °С. Цементит с различными химическими элементами, находящимися в железоуглеродистых сплавах, образует твердые растворы замещения. При определенных условиях (температура и высокое давление) цементит распадается на свободный углерод (графит).
Цементит — ферромагнетик, аллотропных изменений не имеет, при температуре 217 °С теряет магнитные свойства. Количество углерода в цементите всегда постоянно и составляет 6,67 %. Цементит — это самая твердая (700 … 800 НВ) и хрупкая структурная составляющая железоуглеродистых сплавов, режет стекло, не поддается обработке резанием. Пластичность цементита равна нулю. В изломе цементит имеет мелкозернистое или игольчатое строение, белый блестящий цвет и является типичной структурой белых передельных чугунов.
Рис. 1. Микроструктура углеродистых сталей: а — доэвтектоидная сталь — феррит + перлит; б — эвтектоидная сталь — перлит; в — заэвтектоидная сталь — перлит + цементит вторичный
Феррит — твердый раствор внедрения углерода в α-железе. Это малонауглероженное железо с массовой долей углерода до 0,02 %. Феррит имеет твердость 60 … 80 НВ, предел прочности при растяжении σв = 250 МПа (25 кгс/мм2), относительное удлинение при разрыве δ = 50 % и является микроструктурой низкоуглеродистых сталей, которая представляет собой крупные светлые зерна.
Аустенит — твердый раствор внедрения углерода в γ-железе.
Максимальная концентрация углерода в аустените составляет 2,14 %, твердость — 170 … 220 НВ. Аустенит образуется при температуре 727 °С и имеет неустойчивую структуру, при охлаждении распадается. Структура аустенита обладает высокими механическими (прочность, пластичность, вязкость, твердость) и технологическими свойствами.
Перлит — механическая смесь твердого раствора феррита и химического соединения цементита. Такая смесь получила название эвтектоида (легкораспадающийся). Перлит имеет мелкопластинчатую или зернистую структуру.
Массовая доля углерода в перлите составляет 0,83 %, твердость — 200 … 240 НВ, предел прочности при растяжении σв = 1 100 … 1 150 МПа (110 … 115 кгс/мм2). Перлит — структура неустойчивая, при температуре 727 °С распадается на аустенит.
Ледебурит — механическая смесь аустенита и цементита. Ледебурит (эвтектика) содержит 4,3 % углерода, плавится при постоянной температуре 1 147 °С.
Сталь с массовой долей углерода 0,83 % называется эвтектоидной, менее 0,83 % — доэвтектоидной и более 0,83 % — заэвтектоидной. Микроструктуры эвтектоидной (перлит), доэвтектоидной (феррит + перлит) и заэвтектоидной (перлит + цементит вторичный) сталей представлены на рис. 1.
Чугун с массовой долей углерода 4,3 % называется эвтектическим, с массовой долей углерода менее 4,3 % — доэвтектическим, с массовой долей углерода более 4,3 % — заэвтектическим (рис. 2).
Рис. 2. Микроструктура белых чугунов: а — доэвтектический чугун — перлит + ледебурит + цементит; б — эвтектический чугун — ледебурит; в — заэвтектический чугун — ледебурит + цементит первичный
2. Влияние химических элементов на свойства железоуглеродистых сплавов
Железоуглеродистый сплав кроме железа и углерода (постоянных компонентов) содержит полезные, вредные и постоянные (технологические) примеси, которые оказывают различные влияния на свойства конструкционных материалов.
Углерод в железоуглеродистом сплаве может находиться в виде карбида железа Fe3C (цементита) либо в виде графита.
Углерод является основным сплавляемым компонентом, который специально вводят для увеличения прочности, твердости и улучшения технологических и эксплуатационных свойств конструкционных материалов. Влияние углерода на свойства конструкционных материалов зависит от состояния или взаимодействия его с железом, т. е. от образования той или иной структуры железоуглеродистого сплава.
Если при взаимодействии углерода с железом образуется цементит, то сплав будет иметь высокие твердость, хрупкость и практически не будет поддаваться обработке резанием.
Если углерод, взаимодействуя с железом, образует структуры механических смесей (перлита или феррита), то сплав будет иметь высокие механические и технологические свойства.
Кремний и марганец в железоуглеродистых сплавах являются полезными примесями. Кремний в сплав попадает частично из руды, а основная масса — в процессе плавки при раскислении сплава.
Раскисление — это процесс удаления вредных включений оксида железа (FeO) путем введения раскислителей (марганца, кремния и различных ферросплавов). Раскислители, соединяясь с оксидом железа, образуют шлаки, которые подлежат удалению. Незначительная часть раскислителей остается в железоуглеродистом сплаве. Как правило, раскислению подлежит большинство сталей и чугунов.
Кремний полностью растворяется в основной структуре сплава с образованием твердого раствора, повышает предел текучести, уменьшает хрупкость. Высокое содержание кремния (1 … 2 %) придает стали упругость. Кроме того, кремний способствует преобразованию углерода из структуры цементита в свободный углерод в виде графита, уменьшая при этом твердость и хрупкость сплавов. Марганец попадает в сплав при переработке марганцевых руд, а также в процессе раскисления.
Марганец образует с железом твердый раствор, а также способствует образованию химического соединения, поэтому он повышает твердость, износостойкость, прочность. Высокое содержание марганца способствует образованию цементита, что приводит к повышению твердости и хрупкости сплава. Кроме того, марганец нейтрализует вредное влияние серы.
Сера и фосфор в железоуглеродистых сплавах являются вредными примесями.
Фосфор попадает в сплав из руды. Исходный чугун, как правило, имеет высокую массовую долю фосфора. Фосфор ограниченно растворяется в железе, а его избыточное содержание приводит к образованию фосфида железа — очень хрупкого соединения. Фосфор, растворяясь в железе, резко снижает его плотность и приводит к хрупкости в холодном состоянии. Это свойство называется хладноломкостью сплавов. Фосфор также приводит к повышению твердости и уменьшению прочности. Марганец, взаимодействуя с фосфором в процессе раскисления, удаляет его с образованием шлаков.
В отдельных случаях фосфор может быть полезен, так как улучшает обрабатываемость резанием, жидкотекучесть, а при наличии незначительного количества меди повышает коррозионную стойкость.
Сера попадает в сплав из руд, а также из топлива в процессе его горения. Не растворяясь в железе, сера образует с ним легкоплавкую и очень хрупкую механическую смесь (эвтектику) и делает сплав хрупким в районе температур красного каления (это свойство получило название красноломкости), поэтому железоуглеродистые сплавы с высоким содержанием серы не подвергаются горячей обработке давлением.
При высоком содержании в сплаве углерода наличие серы повышает его твердость и хрупкость, ухудшает литейные свойства, снижает жидкотекучесть, увеличивает усадку металла при охлаждении отливок и склонность к образованию микротрещин. Вредное влияние серы нейтрализуется марганцем. При введении в сплав незначительной массовой доли марганца образуется соединение с серой — сульфид марганца (MnS) вместо легкоплавкого сульфида железа (FeS). Сульфид марганца частично удаляется вместе со шлаком.
В железоуглеродистых сплавах могут находиться с очень низкой массовой долей различные газы: азот, водород и кислород. Эти химические элементы являются скрытыми примесями. Из-за сложности их химического анализа массовую долю этих элементов не определяют и в технических условиях не нормируют.
Кроме того, в незначительных количествах встречаются различные металлы (олово, цинк, сурьма, свинец, никель, медь, хром и др.) — случайные примеси. Эти группы металлов попадают как из руд, так и из перерабатываемого при металлургическом процессе стального лома.
Все перечисленные случайные примеси являются неизбежным следствием технологического процесса, т. е. специально не добавляются. В связи с этим получаемые стали с незначительной массовой долей никеля, меди, хрома и других металлов не рассматривают как легированные стали.
Кроме естественных, постоянных, скрытых и случайных химических элементов в железоуглеродистый сплав (особенно в сталь) вводят специальные химические элементы с целью изменения микроструктуры сплава, физико-химических и других свойств.
Специально вводимые в железоуглеродистый сплав химические элементы называют легирующими элементами, а сплавы, полученные на их основе, — легированными сплавами (сталями и чугунами).
В качестве легирующих элементов вводят алюминий, ванадий, вольфрам, молибден, медь, кобальт, кремний, никель, тантал, титан, хром и др.
Государственные стандарты строго регламентируют массовую долю полезных и вредных примесей в железоуглеродистых сплавах.
В сталях, как правило, содержание этих элементов, %, ограничивается следующими верхними пределами:
В чугунах по государственным стандартам допускается более высокая массовая доля, %, полезных и вредных примесей (в зависимости от групп и марок):
3. Диаграммы состояния железоуглеродистых сплавов
Диаграмма состояния железо — углерод — это наглядное универсальное графическое изображение физико-химических процессов, происходящих в железоуглеродистых сплавах.
Так как практическое применение находят железоуглеродистые сплавы с массовой долей углерода до 6,69 %, рассмотрим диаграммы состояния этих сплавов. В металловедении практическое применение нашли два вида диаграмм состояния железо— углерод: стабильная диаграмма — железо— графит (свободный углерод) и метастабильная диаграмма — железо— цементит (карбид железа).
Железо — это аллотропное вещество. Углерод также обладает аллотропией (полиморфизмом).
В природе углерод, находясь в твердом агрегатном состоянии, может существовать в форме графита и в форме алмаза. При нормальных условиях графит является более устойчивой формой существования. При повышении температуры и давления графит приобретает структуру алмаза. Следовательно, алмаз — это метастабильная модификация графита. Графит имеет гексагональную атомно-кристаллическую решетку.
В связи с тем что железоуглеродистый сплав состоит из двух химических веществ, обладающих аллотропией (полиморфизмом), это свойство сохраняется и в сплаве. Таким образом, благодаря полиморфизму железоуглеродистый сплав будет иметь следующие фазы или структуры:
Следует отметить, что феррит, аустенит и ледебурит образуются при первичной кристаллизации, а перлит образуется при вторичной кристаллизации. Кроме того, цементит в сплаве может быть трех модификаций:
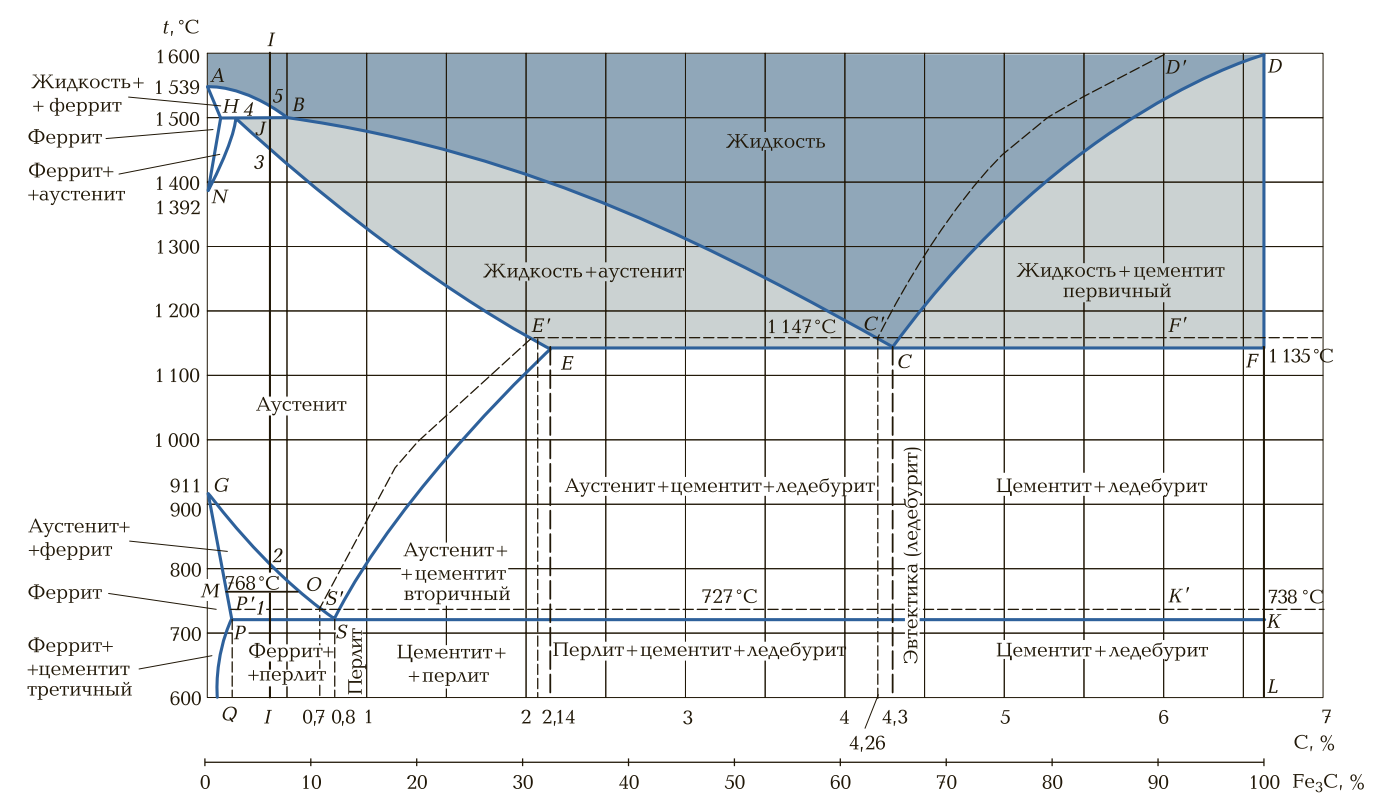
Рассмотрим диаграмму состояния сплава железо — углерод (рис. 3). По диаграмме можно определить структуру сплавов как после медленного охлаждения, так и после нагрева.
Рис. 3. Диаграмма состояния сплава железо— углерод
Критическая точка А соответствует температуре плавления железа (1 539 °С). Критическая точка D — температуре плавления цементита (1 600 °С). Точки H и Р показывают массовую долю углерода в феррите: Н — при температуре 1 499 °С (высокотемпературная концентрация), Р — при температуре 727 °С (низкотемпературная концентрация).
Полиморфное превращение в железе происходит в точках G и N. Критическая точка Е показывает наибольшую массовую долю растворимости углерода в структуре аустенита — 2,14 % (наибольшую концентрацию). Температуре расплавления сплава (1 147 °С) с массовой долей углерода 4,3 % при нагревании соответствует точка С. При охлаждении в этой точке выделяется ледебурит — механическая смесь первичного цементита и аустенита (эвтектика). Критическая точка F соответствует выделению 100 % первичного цементита (температура 1 147 °С).
Соединяя характерные точки, соответствующие фазовым состояниям микроструктур, с критическими точками железа, получаем поверхности раздела (границы), которые раскрывают все физико-химические процессы, происходящие в железоуглеродистых сплавах при нагревании (охлаждении). Рассмотрим эти линии (границы) для сплава с массовой долей углерода 6,67 %.
По достижении температур, соответствующих линии АВСD (линия ликвидуса), стали и чугуны при нагревании расплавляются и при охлаждении начинают затвердевать. Выше этой линии будет жидкая фаза, ниже — полужидкая.
При температурах, образующих линию АНJЕСF (линия солидуса), стали и чугуны начинают плавиться при нагревании и затвердевают при охлаждении.
Линия РSК лежит на горизонтальной прямой, соответствующей температуре 727 °С, при которой происходит первое аллотропное превращение (первичная кристаллизация). Второе аллотропное превращение (вторичная кристаллизация) происходит по линии GSE.
Линия КFD — линия 100 % химического соединения углерода с железом (цементит). Линия QPG — линия низкоуглеродистого твердого раствора феррита и третичного цементита.
Геометрическая фигура АВJHN показывает область перитектического 1 превращения сплава.
1 Перитектика — жидкий раствор, который может находиться при данном давлении в равновесии с двумя и более фазами.
Диаграмма состояния железо — графит (Fe — С) представляет собой диаграмму, аналогичную диаграмме железо — цементит. Для более наглядного изучения диаграммы состояния железо — графит критические точки накладывают на диаграмму железо — цементит, что дает возможность более глубоко понять физико-химические процессы в обоих сплавах. На рис. 6 диаграмма состояния сплава Fe—C показана пунктирной линией.
В сплаве железо — графит несколько изменяются критические температуры аллотропных превращений. Например, эвтектоидное превращение происходит при температуре 738 °С при массовой доле углерода 0,7 % (S′ ). В этом случае эвтектоид называется графитовым, состоящим из феррита и графита. Штриховыми линиями показаны границы раздела состояния системы. При температуре 1 153 °С (линия E′ C′ F′ ) структура начинает расплавляться с
образованием жидкого раствора и первичного графита. Линия S′ Е′ — граница выделения вторичного графита из аустенита. Линия С′ D′ — граница полного расплавления первичного графита. При температуре 1 153 °С образуется эвтектика с массовой долей углерода 4,26 %, имеющая структуру аустенита и графита. Такая структура называется графитовой.
Железоуглеродистые сплавы кристаллизуются при условии медленного охлаждения и наличия в сплаве графитизирующих компонентов (см. диаграмму состояния). Быстрота охлаждения железоуглеродистых сплавов способствует образованию сплава железо — цементит.
Зная конкретную массовую долю углерода в углеродистых сталях и чугунах, по диаграмме Fе — Fе3С на горизонтальной оси находим соответствующую точку. Из этой точки восстанавливаем перпендикуляры, а пересечения перпендикуляров с любыми плоскостями раздела (линиями) дадут нам критические точки для конкретных марок сталей и чугунов.
Рассмотрим пример определения температуры перекристаллизации и плавления стали марки 40 с массовой долей углерода 0,4 %. На диаграмме железо— цементит на оси ординат (концентрация углерода) из точки, соответствующей 0,4 % углерода, восстанавливаем перпендикуляр I— I. Перпендикуляр пересекает кривые диаграммы железо— цементит, образуя критические точки.
Сталь марки 40 с массовой долей углерода 0,4 % при нормальных условиях и до температуры 727 °С (рис. 7) будет иметь структуру 50 % феррита + 50 % перлита. В процессе нагревания при температуре 727 °С (точка 1) структура перлита будет медленно распадаться, образуя структуру аустенита. В связи с тем что в процессе распада структур происходит интенсивное поглощение энергии (теплоты), на кривой будет горизонтальный участок 1 — 1′.
После полного распада перлита в структуре стали до температуры 760 °С никаких изменений не происходит, сталь медленно нагревается (на диаграмме наклонная кривая 1′— 2 ), структура стали будет феррит + аустенит. При пересечении перпендикуляра I— I (см. рис. 3) с линией GS (точка 2) начинает распадаться структура феррита в структуру аустенита. На диаграмме будет горизонтальный участок 2 — 2′ (cм. рис. 7), так как пока происходит распад феррита в аустенит, температура постоянная (происходит поглощение энергии).
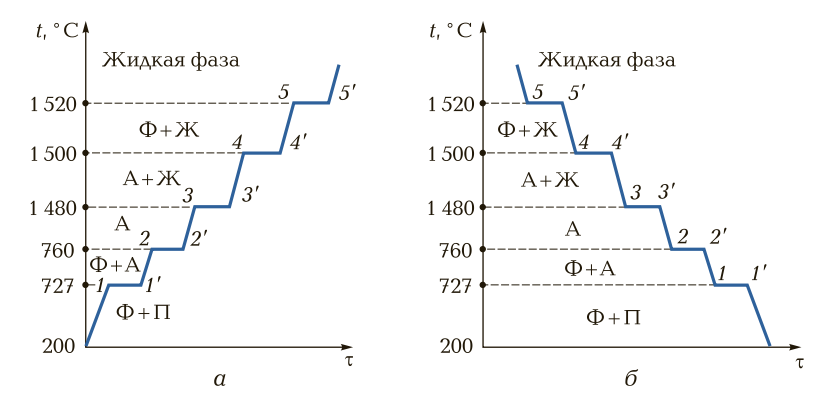
Рис. 4. Кривые нагрева (а) и охлаждения (б) стали марки 40: t — температура; τ — время; Ф — феррит; А — аустенит; П — перлит; Ж — жидкость; 1 — 5, 1¢— 5¢ — критические точки, соответствующие аллотропным превращениям
При дальнейшем нагревании в точке 2 до точки 3 (от 760 °С до 1 480 °С) структура стали будет постоянной — аустенит. В точке 3 (1 480 °С) происходит расплавление части аустенита. Пока часть аустенита расплавляется, температура стали остается постоянной, и на кривой будет горизонтальный участок 3—3′. Между точками 3 и 4 структура стали будет аустенит + жидкая фаза.
В точке 4 при температуре 1 500 °С (на рис. 3 пересечение с горизонтальной прямой JВ) происходит перестройка структур оставшегося аустенита в феррит. На кривой будет горизонтальный участок 4— 4′ (см. рис. 4). До точки 5 (1 520 °С) структура стали будет феррит + жидкая фаза.
В точке 5 оставшийся феррит начинает медленно расплавляться, и температура стали остается постоянной (1 520 °С), на кривой будет снова горизонтальный участок 5—5′. Выше линии 5— 5′ сталь будет иметь жидкую фазу. При охлаждении процесс происходит в обратном порядке (см. рис. 4, б ).
Аналогично структуры и критические точки (температуры) определяются по диаграмме Fe— Fe3C для любой марки стали и чугуна. Кроме того, по диаграмме определяются температуры горячей обработки давлением и температуры различной термической и химико-термической обработки.