какие зоны выделяют при описании очага инфаркта зоны бейли
Какие зоны выделяют при описании очага инфаркта зоны бейли
Больные инфарктом миокарда поступают под наблюдение врача в разные сроки, а следовательно, в различные периоды развития болезненного процесса. В соответствии с этим морфологические функциональные нарушения в поврежденном миокарде будут разнообразны, что отражается на ЭКГ. В зависимости от того, в каком периоде снимается ЭКГ, изменения будут претерпевать или комплекс QRS, или зубец Т, или сегмент S—Т.
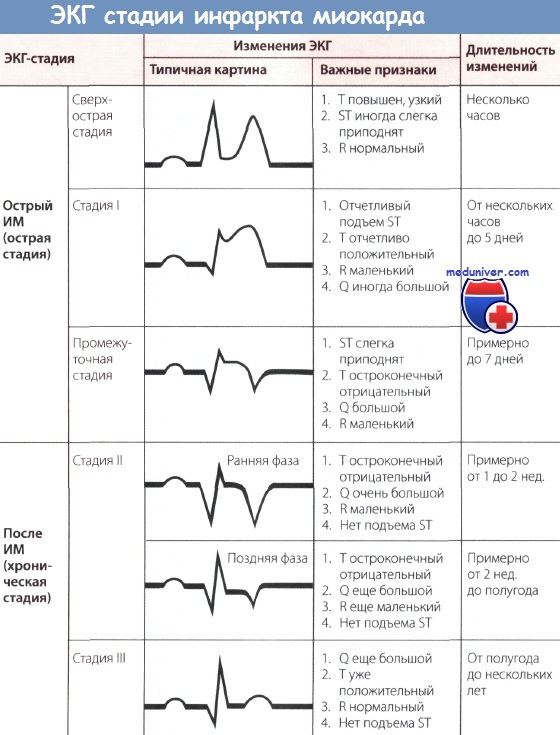
Для инфаркта миокарда в ранних стадиях развития характерна довольно быстрая и очень резкая динамика ЭКГ. В более поздних стадиях его изменения на ЭКГ происходят медленнее. При сопоставлении изменений на ЭКГ, снятых в различные сроки болезни, с патоло-гоанатомическими данными выделено четыре основные стадии электрокардиографических изменений.
Первая стадия изменений на ЭКГ ишемическая. Часть острой стадии по Г. Я. Дехтярю (1966), стадия повреждения, по М. И. Кечкеру и Р. Л. Аврук (1966), связана с образованием очага повреждения в стенке желудочка. Эти изменения появляются уже в течение первого часа прекращения кровоснабжения данного участка миокарда, отмечаются иногда на протяжении 1—2 ч или 1—3 дня. Изменения на ЭКГ в течение этой стадии в отведениях над очагом поражения следующие: сначала увеличивается с заострением амплитуда зубца Т. Обычно сегмент S—Т в этот период совершает быструю эволюцию — вначале слегка опускается, а затем резко приподнимается над изолинией. Изменения формы и высоты зубца Т и смещение сегмента S—Т на фоне болевого приступа в течение 1—2 ч позволяют дифференцировать «гигантский» коронарный зубец Т, от стойко высокого зубца Т как варианта нормы или признака некоронарной патологии. Следующим этапом эволюции ЭКГ в стадии повреждения являются:
— значительный подъем сегмента S—Т над изолинией, на этом первом этапе возможно обратное развитие изменений в сердце и на ЭКГ;
— постепенное снижение зубца Т вследствие расширения зоны повреждения на субэпикардиальные слои миокарда желудочка. ЭКГ в этот период имеет форму монофазной кривой. В отведениях с положительным электродом, расположенным над областью сердца, противоположной очагу поражения, часто отмечается смещение сегмента S—Т вниз от изолинии, иногда отрицательный зубец Т (реципрокные изменения). На этом этапе обычно образуется большой очаг инфаркта или мелкоочаговый некроз.
Вторая (острая) стадия инфаркта связана с образованием зоны некроза в центре очага повреждения и значительной величины зоны ишемии на периферии очага. В некоторых случаях вторая стадия начинается рано, через 2—3 ч после начала приступа, а иногда через 1—3 дня. Продолжается она в течение 2—3 нед. На ЭКГ в отведениях над инфарктом образуется глубокий и широкий зубец Q, а зубец R уменьшается (QRS формы QS, Qr, QrS), или глубоко расщепляется зубец R на восходящем колене. Так как образование зубца Q связано с зоной некроза, то чем оно глубже и шире распространяется в стенке желудочка, тем шире и глубже будет зубец Q. Если вместо высокого зубца Р в отведении регистрируется зубец QRS, то принято считать, что имеет место трансмуральный инфаркт миокарда, то есть некроз развился на всю толщину стенки желудочка в данной области.
Принято считать установление сегмента S—Т на уровне изолинии признаком окончания острой стадии. На протяжении острой стадии наблюдается сложная динамика направления, амплитуды и формы зубца Т. В отведении с положительным электродом над областью инфаркта зубец Т в начале острой стадии отрицательный, симметричный, не очень глубокий. Этот отрицательный коронарный зубец Т связан с зоной ишемии по периферии очага инфаркта. Через 3—5 дней глубина зубца Т уменьшается, он часто сглаживается или становится положительным. По всей вероятности, данные изменения обусловлены уменьшением ишемии. На 10—15-й день от начала инфаркта зубец Т вновь становится отрицательным. В течение всего оставшегося периода острой стадии он довольно быстро углубляется, достигая наибольшей глубины к концу ее или к началу подострой.
Повторное углубление зубца Т во второй половине острой стадии связано, вероятно, с перифокальной воспалительной реакцией миокарда, окружающего очаг инфаркта, вследствие аутоаллергии при рассасывании некротизированной ткани (М. И. Кечкер, Т. А. Наддачина, 1970).
В отведениях с противоположной от инфаркта стороны сердца можно зарегистрировать высокий зубец R, высокий остроконечный зубец Т и смещенный вниз от изолчнии сегмент S—Т. II в этих отведениях наблюдается динамика зубца Т и сегмента S—Т в те же сроки, но в противоположном направлении. Описанная псевдоположительная динамика зубца Т на 3—5-й день и псевдотрицательная его динамика на 7—10-й день после инфаркта не связаны с новым изменением коронарного кровообращения, а обусловлены закономерной динамикой самого инфаркта в острой стадии.
Какие зоны выделяют при описании очага инфаркта зоны бейли
Синонимы: инфаркт миокарда с подъемом сегмента ST, острый инфаркт миокарда (ИМ), острый трансмуральный инфаркт, инфаркт миокарда (ИМ) с зубцом Q.
Патофизиология. Вследствие кровоизлияния в атеросклеротическую бляшку и постепенно нарастающего тромбоза коронарной артерии происходит стенозирование ее просвета с исходом в окклюзию. Это приводит к ишемии миокарда, кровоснабжаемого пораженной коронарной артерией, и его некрозу.
Тщательные многолетние эпидемиологические исследования больных инфарктом миокарда (ИМ) показали, что у них имеются факторы риска. Сочетание этих факторов способствует ускорению атеросклеротического процесса и многократному увеличению риска инфаркта миокарда (ИМ). К известным на сегодняшний день факторам риска относятся курение, повышенный уровень холестерина в крови, высокое АД и сахарный диабет.
Помимо перечисленных четырех главных факторов риска, известны и другие, в частности, избыточная масса тела, стресс, гиподинамия, наследственная предрасположенность.
Симптомы инфаркта миокарда с подъемом сегмента ST (ИМпST):
• Сильная ангинозная боль, длящаяся более 15 мин
• Подъем сегмента ST на ЭКГ
• Положительные результаты анализа крови на креатинкиназу, ее МВ-фракцию, тропонины (I или Т)
Диагностика инфаркта миокарда с подъемом сегмента ST (ИМпST)
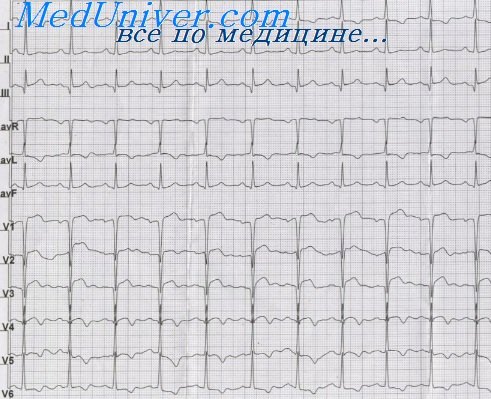
ЭКГ, как правило, имеет решающее значение для установления диагноза. Уже через 1 ч после появления типичного болевого приступа в большинстве случаев на ЭКГ отмечаются четкие признаки ИМ. Поэтому диагностика ИМ является важнейшей задачей электрокардиографии.
При анализе ЭКГ у больных инфарктом миокарда (ИМ) следует обратить внимание на следующие особенности.
• Признаки ИМ должны быть однозначными. В большинстве случаев изменения на ЭКГ бывают настолько типичны, что диагноз можно поставить, не прибегая к дальнейшему обследованию.
• Другие важные заболевания, особенно в острой стадии, например приступ стабильной стенокардии у больного ИБС, перикардит или миокардит, не следует ошибочно интерпретировать как ИМ. Например, при перикардите на ЭКГ нет отчетливых признаков ИМ.
• В процессе диагностики ИМ необходимо установить также стадию ИМ, т.е. следует указать, по крайней мере, идет ли речь об острой фазе или это старый инфаркт. Это важно, так как лечение ИМ имеет свои особенности в зависимости от стадии заболевания.
• В диагнозе следует отразить также локализацию ИМ. В частности, следует дифференцировать инфаркт передней стенки ЛЖ от инфаркта его задней стенки. В зависимости от локализации ИМ можно ориентировочно определить, какая коронарная артерия поражена.
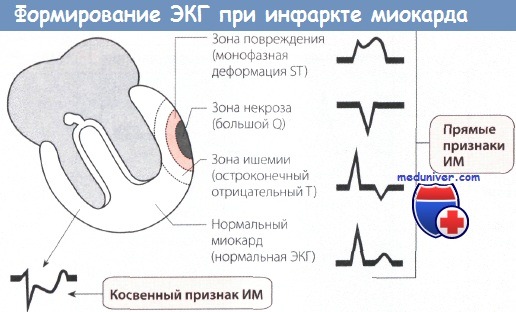
Интерпретация отдельных показателей ЭКГ при инфаркте миокарда (ИМ)
1. Большой зубец Q (зона некроза). Вследствие некроза миокарда в зоне инфаркта ЭДС не возникает. Результирующий вектор ЭДС направлен от зоны некроза. Поэтому на ЭКГ регистрируется глубокий и уширенный зубец Q (зубец Q Парди) в отведениях, которые располагаются непосредственно над зоной ИМ.
2. Подъем сегмента ST. Зона некроза миокарда окружена зоной повреждения. Поврежденная ткань по сравнению со здоровой в конце деполяризации желудочка несет меньший отрицательный заряд, поэтому менее возбудима. Поэтому в зоне повреждения возникает вектор, который соответствует сегменту ST и направлен от электрически отрицательного миокарда к электрически менее отрицательному, т.е. к части миокарда, которая заряжена относительно положительно. Поэтому на ЭКГ, соответствующей зоне повреждения, регистрируется подъем сегмента ST.
3. Остроконечный отрицательный зубец Т. ЭКГ зоны ишемии обнаруживает изменения в фазе реполяризации. Вектор реполяризации направлен от зоны ишемии к здоровому миокарду. При повреждении эпикардиальных слоев миокарда вектор ЭДС направлен снаружи внутрь. Поэтому в отведениях, в которых в норме регистрируются положительные зубцы Т, теперь появляются симметричные остроконечные отрицательные зубцы Т (коронарные зубцы Т Парди).
Результаты исследования сывороточных маркеров некроза миокарда становятся положительными через 2-6 ч после развития ишемии.
Появление тропонинов в сыворотке крови отражает образование тромба в коронарной артерии. Поэтому анализ крови на тропонины из-за высокой чувствительности (90% при выполнении через 6 ч) и специфичности (примерно 95%) является стандартным исследованием в экстренной диагностике острого инфаркта миокарда (ИМ).
Определение сывороточных маркеров некроза миокарда играет важную роль не только в диагностике острого инфаркта миокарда (ИМ), но и позволяет судить о его динамике. Особенно велико их значение в тех случаях, когда данные ЭКГ стертые или маскируются блокадой ножки ПГ либо синдромом WPW. Затруднительна диагностика инфаркта миокарда (ИМ) и в тех случаях, когда инфаркт локализуется в бассейне огибающей ветви левой коронарной артерии.
В настоящее время в диагностике инфаркта миокарда (ИМ) применяют оба указанных метода исследования: ЭКГ и анализ крови на сывороточные маркеры некроза миокарда. Причем они не конкурируют, а дополняют друг друга.
Несмотря на это, как показали ранее выполненные нами исследования, предсказательная ценность ЭКГ более высокая по сравнению с анализом крови на сывороточные маркеры некроза миокарда, так как в большинстве случаев острого ИМ изменения на ЭКГ при внимательном ее чтении появляются уже в течение 1-го часа после начала ишемии и являются надежными диагностическими признаками, в то время как повышение уровня сывороточных маркеров во многих случаях не связано с ишемическим повреждением миокарда.
Кроме того, существенное преимущество ЭКГ состоит также в том, что ее можно выполнять столько раз, сколько нужно, не причиняя больному какого-либо неудобства.
При появлении боли в груди следует во всех случаях зарегистрировать ЭКГ. При подозрении на ИМ рекомендуется выполнять контрольную ЭКГ по меньшей мере каждые 3 дня в сочетании с анализом крови на сывороточные маркеры некроза миокарда.
На ЭКГ при остром инфаркте миокарда (ИМ) появляются следующие изменения: независимо от локализации ИМ, т.е. как при инфаркте передней стенки, так и при инфаркте задней стенки в острой фазе происходит значительное изменение сегмента ST. В норме подъем сегмента ST отсутствует, хотя иногда возможны его незначительные подъем или депрессия даже у практически здоровых людей.
При остром инфаркте миокарда (ИМ) первым признаком на ЭКГ бывает отчетливый подъем сегмента ST. Этот подъем сливается со следующим за ним положительным зубцом Т, и, в отличие от нормы, граница между ними исчезает. В таких случаях говорят о монофазной деформации сегмента ST. Такая монофазная деформация патогномонична для острой фазы, т.е. для «свежего» ИМ.
Дифференциальная диагностика инфаркта миокарда с подъемом сегмента ST (ИМпST) с положительным зубцом Т показана на рисунке ниже.
Незадолго до появления монофазной деформации сегмента ST при внимательном анализе ЭКГ можно отметить чрезвычайно высокие остроконечные зубцы Т (так называемые асфиксические Т, или сверхострые Т), обусловленные острой субэндокардиальной ишемией.
Острый и уширенный зубец Q может регистрироваться уже в острой стадии ИМ, однако этот признак не является обязательным. Отрицательный зубец Т в острой стадии может еще отсутствовать.
При «старом» инфаркте миокарда (ИМ) имевший место ранее подъем сегмента ST уже не определяется, но появляются другие изменения, затрагивающие зубцы Q и Т.
В норме зубец Q неширокий (0,04 с) и неглубокий, не превышая по высоте четвертой части зубца R в соответствующем отведении. При «старом» ИМ зубец Q уширен и глубокий.
Зубец Т в норме положительный и составляет не менее 1/7 высоты зубца R в соответствующем отведении, что отличает его от зубца Т при ИМ после острой стадии (т.е. в ранней фазе II стадии), когда он становится глубоким, остроконечным и отрицательным (коронарный зубец Т Парди), кроме того, отмечается депрессия сегмента ST. Однако иногда зубец Т расположен на изолинии и не снижен.
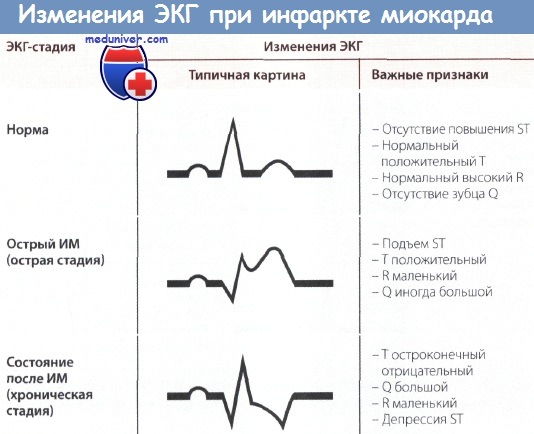
Обычно для определения ЭКГ-стадии инфаркта миокарда (ИМ) бывает достаточно классификации, представленной на рисунке ниже. Классификация, представленная на рисунке выше, позволяет точнее оценить динамику ИМ.
В целом считается, что чем больше отведений, в которых отмечаются патологические изменения, тем обширнее зона ишемии миокарда.
Изменения ЭКГ, а именно большой зубец Q (признак некроза, зубец Q Парди) и отрицательный зубец Т с депрессией сегмента ST или без нее являются типичными для сформировавшегося рубца при «старом» ИМ. Эти изменения проходят по мере улучшения состояния больного. Однако известно, что, несмотря на клиническое улучшение и заживление, признаки старого инфаркта, особенно большой зубец Q сохраняются.
Подъем сегмента ST с положительным зубцом Т, т.е. монофазная деформация сегмента ST с большим зубцом Q, сохраняющаяся более 1 нед., и переход сегмента ST в медленно поднимающуюся дугу должны вызвать подозрение на аневризму сердца.
Дальнейшая тактика после диагностики инфаркта миокарда с подъемом ST (ИМпST) такая же, как и при инфаркте миокарда без подъема сегмента ST (ИМбпST).
Особенности ЭКГ при инфаркте миокарда с подъемом сегмента ST (остром трансмуральном инфаркте):
• Некроз миокарда, обусловленный окклюзией коронарной артерии
• Длительный приступ интенсивной сжимающей загрудинной боли
• В острой стадии: подъем сегмента ST и положительный зубец Т
• В хронической стадии: глубокий остроконечный отрицательный зубец T и большой зубец Q
• Положительный результат анализа крови на креатинкиназу и тропонины
Учебное видео ЭКГ при инфаркте миокарда
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Острый инфаркт миокарда (субэндокардиальный и трансмуральный)
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Электрокардиограмма позволяет выявить очаг некроза в мышце сердца, его глубину и локализацию, состояние переинфарктной зоны, динамику процесса. На ЭКГ отведениях, активный электрод которых располагается над зоной некроза, образуется патологический зубец Q и снижается высота зубца R вплоть до полного его исчезновения. Изменения зубца Q сочетается с характерной для ИМ ЭКГ динамикой, отражающей временную динамику заболевания.
Электрокардиографические признаки можно систематизировать следующим образом:
Дифференциальный диагноз
Особенно трудно дифференцировать инфаркт миокарда и поражение грудного отдела аорты. В последнем случае боль в грудной клетке, как правило, сильная, нестерпимая. Она начинается внезапно, сразу с максимальной интенсивностью, иррадиирует вдоль позвоночника, имеет волнообразное течение.
При дифференциальной диагностике следует учитывать резкое несоответствие интенсивности и длительности боли скудным изменениям ЭКГ. Во всех сложных диагностических случаях серьезным подспорьем является экспресс-тест с тропонином-Т или гликоген-фосфорилазой ВВ.
Лечение
3. Стабилизация артериального давления и ритма сердца.
Информация
Источники и литература
Информация
Сотрудники кафедры скорой и неотложной медицинской помощи, внутренних болезней №2 Казахского национального медицинского университета им. С.Д. Асфендиярова: к.м.н, доцент Воднев В.П.; к.м.н., доцент Дюсембаев Б.К.; к.м.н., доцент Ахметова Г.Д.; к.м.н., доцент Бедельбаева Г.Г.; Альмухамбетов М.К.; Ложкин А.А.; Маденов Н.Н.
Заведующий кафедрой неотложной медицины Алматинского государственного института усовершенствования врачей – к.м.н., доцент Рахимбаев Р.С.
Сотрудники кафедры неотложной медицины Алматинского государственного института усовершенствования врачей: к.м.н., доцент Силачев Ю.Я.; Волкова Н.В.; Хайрулин Р.З.; Седенко В.А.
Классификация инфаркта миокарда
Автор материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
На сегодняшний день расширенная классификация инфаркта миокарда помогает четко определить прогноз течения болезни и ее стадию, что позволяет определить правильную тактику лечения.
Так, по объему поражения выделяют:
С учетом глубины поражения существуют такие виды инфаркта миокарда:
Инфаркты миокарда классифицируют по по ЭКГ-изменениям:
По локализации очага некроза выделяют:
Согласно кратности и срокам развития инфаркты бывают:
И, наконец, по этапам развития инфаркта определяют:
Многие кардиохирурги считают неправильной систематизацию инфаркта миокарда на мелко- и крупноочаговый. Согласно классификации ВОЗ инфарктом миокарда принято считать только крупноочаговые некрозы сердечной мышцы.
При проведении комплексного лечения в расчет берутся три основные классификации инфаркта миокарда. В первую очередь учитывается глубина поражения миокарда, что определяется на основании данных, полученных при электрокардиографическом исследовании. Также существенным является определение инфаркта миокарда по локализации и клиническому течению.
Диагностика и лечение инфаркта миокарда на догоспитальном этапе
Как проводится купирование болевого приступа? В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная? Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии? Инфаркт миокарда —
Как проводится купирование болевого приступа?
В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная?
Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии?
Инфаркт миокарда — неотложное клиническое состояние, обусловленное некрозом участка сердечной мышцы, развившимся в результате нарушения ее кровоснабжения. Поскольку в первые часы (а иногда и сутки) от начала заболевания бывает сложно дифференцировать острый инфаркт миокарда и нестабильную стенокардию, для обозначения периода обострения ишемической болезни сердца (ИБС) в последнее время пользуются термином «острый коронарный синдром», под которым понимают любую группу клинических признаков, позволяющих заподозрить инфаркт миокарда или нестабильную стенокардию. Острый коронарный синдром может рассматриваться как первичный диагноз; он диагностируется на основании болевого синдрома (затяжной ангинозный приступ, впервые возникшая, прогрессирующая стенокардия) и изменений ЭКГ. Различают острый коронарный синдром с подъемом сегмента ST или остро возникшей полной блокадой левой ножки пучка Гиса (состояние, требующее проведения тромболизиса, а при наличии технических возможностей — ангиопластики) и без подъема сегмента ST — с его депрессией сегмента ST, инверсией, сглаженностью псевдонормализацией зубца Т, или вообще без изменений на ЭКГ (тромболитическая терапия не показана). Таким образом, диагноз «острый коронарный синдром» позволяет оперативно оценить объем необходимой неотложной помощи и выбрать адекватную тактику ведения пациентов.
С точки зрения определения объема необходимой лекарственной терапии и оценки прогноза представляют интерес три классификации. По глубине поражения (на основе данных электрокардиографического исследования) различают трансмуральный и крупноочаговый («Q-инфаркт» с подъемом сегмента ST в первые часы заболевания и формированием зубца Q в последующем) и мелкоочаговый («не Q-инфаркт», не сопровождающийся формированием зубца Q, а проявляющийся отрицательными зубцами Т); по клиническому течению — неосложненный и осложненный инфаркт миокарда; по локализации — инфаркт левого желудочка (передний, задний или нижний, перегородочный) и инфаркт правого желудочка.
Диагностика инфаркта миокарда на догоспитальном этапе
Наиболее типичным проявлением инфаркта миокарда является приступ боли в грудной клетке. Диагностически значимы такие параметры, как интенсивность болевого синдрома (если аналогичные боли возникали ранее, то при инфаркте они бывают необычно интенсивными), его продолжительность (необычно длительный приступ, продолжающийся более 15-20 мин), неэффективность сублингвального приема нитратов. При анализе клинической картины необходимо получить ответы на следующие вопросы:
По симптоматике острейшей фазы инфаркта миокарда, помимо болевого, выделяют и другие клинические варианты инфаркта миокарда (см. таблицу).
Данные физикального обследования (гипергидроз, резкая общая слабость, бледность кожных покровов, признаки острой сердечной недостаточности) при любом клиническом варианте инфаркта миокарда имеют только вспомогательное диагностическое значение.
Электрокардиографическими критериями инфаркта миокарда являются изменения, служащие признаками:
При инфаркте передней стенки подобные изменения выявляются в I и II стандартных отведениях, усиленном отведении от левой руки (aVL) и соответствующих грудных отведениях (V1, 2, 3, 4, 5, 6). При высоком боковом инфаркте миокарда изменения могут регистрироваться только в отведении aVL, и для подтверждения диагноза необходимо снять высокие грудные отведения. При инфаркте задней стенки (нижнем, диафрагмальном) эти изменения обнаруживаются во II, III стандартном и усиленном отведении от правой ноги (aVF). При инфаркте миокарда высоких отделов задней стенки левого желудочка (заднебазальном) изменения в стандартных отведениях не регистрируются, диагноз ставится на основании реципрокных изменений — высоких зубцов R и Т в отведениях V1-V2.
Кроме того, косвенным признаком инфаркта миокарда, не позволяющим определить фазу и глубину процесса, является остро возникшая блокада ножек пучка Гиса (при наличии соответствующей клиники).
Наибольшей достоверностью обладают электрокардиографические данные в динамике, поэтому электрокардиограммы по возможности должны сравниваться с предыдущими.
Таким образом, на догоспитальном этапе оказания медицинской помощи диагноз острого инфаркта миокарда ставится на основании клинической картины и изменений электрокардиограммы. В дальнейшем диагноз уточняется в стационаре после определения уровня маркеров некроза миокарда в крови и на основании динамики ЭКГ. В большинстве случаев острого коронарного синдрома с подъемом сегмента ST формируется инфаркт миокарда с зубцом Q; при остром коронарном синдроме без подъема сегмента ST при повышении уровня маркеров некроза диагностируется инфаркт миокарда без зубца Q, а при нормальном их уровне — нестабильная стенокардия.
Ведение больных на догоспитальном этапе
Для купирования тошноты и рвоты рекомендуют в/в введение 10-20 мг метоклопрамида (церукала, реглана). При выраженной брадикардии показано использование атропина в дозе 0,5 мг (0,5 мл 0,1%-ного раствора) в/в; терапия артериальной гипотензии проводится по общим принципам коррекции гипотензии при инфаркте миокарда.
Недостаточная эффективность обезболивания наркотическими анальгетиками служит показанием к в/в инфузии нитратов (см. ниже). При низкой эффективности нитратов в сочетании с тахикардией дополнительный обезболивающий эффект может быть получен благодаря введению бета-адреноблокаторов (см. ниже). Боль может быть купирована в результате эффективного тромболизиса (см. ниже).
Продолжающиеся интенсивные ангинозные боли служат показанием к применению масочного наркоза закисью азота (обладающей седативным и анальгезирующим действием) в смеси с кислородом. Начинают с ингаляции кислорода в течение 1-3 мин, затем используют закись азота (20 %) с кислородом (80 %) с постепенным повышением концентрации закиси азота до 80 %; после засыпания больного переходят на поддерживающую концентрацию газов — 50:50. Закись азота не снижает выброса левого желудочка. Возникновение побочных эффектов (тошноты, рвоты, возбуждения или спутанности сознания) является показанием для уменьшения концентрации закиси азота или отмены ингаляции. При выходе из наркоза ингалируют чистый кислород в течение 10 мин для предупреждения артериальной гипоксемии.
А. Показаниями к проведению тромболизиса служит подъем сегмента ST более чем на 0,1 мВ по крайней мере в двух стандартных отведениях ЭКГ и более чем на 0,2 мВ в двух смежных грудных отведениях или остро возникшая полная блокада левой ножки пучка Гиса в период от 30 мин до 12 ч от начала заболевания. Применение тромболитических средств возможно и позднее, если сохраняется подъем ST на ЭКГ, продолжается болевой приступ и/или наблюдается нестабильная гемодинамика.
В отличие от внутрикоронарного системный тромболизис (осуществляется внутривенным введением тромболитических средств) не требует каких-либо сложных манипуляций и специального оборудования. При этом он достаточно эффективен, если проводится в первые часы развития инфаркта миокарда (оптимально — на догоспитальном этапе), поскольку сокращение летальности напрямую зависит от сроков достижения реперфузии.
При отсутствии противопоказаний решение вопроса о проведении тромболизиса принимается на основании анализа фактора времени: при транспортировке более 30 мин или при отсрочке внутрибольничного проведения тромболизиса более чем на 60 мин введение тромболитических средств должно осуществляться на догоспитальном этапе. Во всех остальных случаях оно должно быть отложено до стационара.
Наиболее часто для проведения тромболизиса используется стрептокиназа внутривенно только через периферические вены, попытки катетеризации центральных вен недопустимы; перед инфузией возможно внутривенное введение 5-6 мл 25%-ного магния сульфата либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 мин); «нагрузочная» доза аспирина (250-300 мг разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан (аллергические и псевдоаллергические реакции); 1 500 000 Ед стрептокиназы разводятся в 100 мл изотонического раствора хлорида натрия и вводятся внутривенно за 30 мин.
Одновременного назначения гепарина при использовании стрептокиназы не требуется — предполагают, что стрептокиназа сама обладает антикоагуляционными и антиагрегационными свойствами. Показано, что внутривенное введение гепарина не снижает летальности и частоты рецидивов инфаркта миокарда, а эффективность подкожного введения препарата сомнительна. Если гепарин по каким-либо причинам был введен ранее, это не является препятствием к проведению тромболизиса. Рекомендуется назначение гепарина через 12 ч после прекращения инфузии стрептокиназы. Практиковавшееся ранее использование гидрокортизона для профилактики анафилаксии признано не только малоэффективным, но и небезопасным в острейшей стадии инфаркта миокарда (глюкокортикоиды увеличивают риск разрыва миокарда).
Основные осложнения тромболизиса:
Клинические признаки восстановления коронарного кровотока: прекращение ангинозных приступов через 30-60 мин после введения тромболитика, стабилизация гемодинамики, исчезновение признаков левожелудочковой недостаточности, быстрая (в течение 2-3 ч) динамика ЭКГ с приближением сегмента ST к изолинии на 50% от исходного уровня подъема и ранним формированием патологического зубца Q и/или отрицательного зубца Т, появление реперфузионных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.), быстрая динамика МВ-КФК.
Для решения вопроса о возможности использования тромболитических средств следует уточнить ряд моментов:
Следует также обратить внимание на другие состояния, чреватые развитием геморрагических осложнений и служащие относительными противопоказаниями к проведению системного тромболизиса: тяжелые заболевания печени и почек; подозрение на хроническую аневризму сердца, перикардит, инфекционный миокардит, тромб в сердечных полостях; тромбофлебит и флеботромбоз; варикозное расширение вен пищевода; язвенная болезнь в стадии обострения; беременность.
В сомнительных случаях проведение тромболитической терапии должно быть отложено до поступления больного в стационар (при атипичном развитии заболевания, неспецифических изменениях ЭКГ, давно существующей блокаде ножки пучка Гиса или ЭКГ-признаках несомненного предшествующего инфаркта миокарда, маскирующих типичные изменения).
Б. При отсутствии показаний к тромболитической терапии (поздние сроки, так называемый мелкоочаговый или «не-Q-инфаркт») проводится антикоагулянтная терапия. Ее цель заключается в предупреждении или ограничении тромбоза венечных артерий, а также в профилактике тромбоэмболических осложнений (особенно часто развивающихся у больных передним инфарктом миокарда, при низком сердечном выбросе, мерцательной аритмии). Для этого на догоспитальном этапе внутривенно болюсно вводится гепарин в дозе до 5000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то начинается длительная внутривенная инфузия гепарина со скоростью 800-1000 МЕ/ч под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в «лечебной» дозе. Введение гепарина на догоспитальном этапе не препятствует проведению тромболизиса в стационаре.
В. С первых минут от начала развития инфаркта миокарда всем больным при отсутствии противопоказаний следует назначать малые дозы ацетилсалициловой кислоты (аспирина). Антитромбоцитарный эффект препарата максимально проявляется уже через 30 мин, а своевременное начало применения аспирина позволяет существенно снизить летальность. Назначение ацетилсалициловой кислоты перед проведением тромболизиса дает наибольший клинический эффект. Доза для первого приема на догоспитальном этапе составляет 160-325 мг (разжевать). На стационарном этапе препарат назначается 1 раз в сутки по 100-125 мг.
А. Внутривенное введение нитратов при остром инфаркте миокарда способствует купированию болевого синдрома, гемодинамической разгрузке левого желудочка, снижает АД. Растворы нитратов для внутривенного введения готовят ex tempore: каждые 10 мг нитроглицерина (например, 10 мл 0,1%-ного раствора в виде препарата перлинганит) или изосорбида динитрата (например, 10 мл 0,1%-ного раствора в виде препарата изокет) разводят в 100 мл физиологического раствора (20 мг препарата — в 200 мл физиологического раствора и т. д.); таким образом, 1 мл приготовленного раствора содержит 100 мкг препарата. Нитраты вводят капельно под постоянным контролем АД и ЧСС с начальной скоростью 5-10 мкг/мин и последующим увеличением скорости на 20 мкг/мин каждые 5 мин до достижения желаемого эффекта или максимальной скорости введения — 400 мкг/мин. Обычно эффект достигается при скорости инфузии 50-100 мкг/мин. При отсутствии дозатора приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле (см. выше) с начальной скоростью 2-4 капли в минуту, при условии стабильной гемодинамики и сохранения болевого синдрома скорость может постепенно увеличиваться вплоть до максимальной — 30 капель в минуту. Введение нитратов начинают как линейные, так и специализированные бригады СиНМП и продолжают в стационаре. Продолжительность внутривенного введения нитратов — 24 ч и более; за 2-3 ч до окончания инфузии назначается первая доза нитратов внутрь. Передозировка нитратов, вызывающая падение сердечного выброса и снижение САД ниже 80 мм рт. ст., может привести к ухудшению коронарной перфузии и к увеличению размеров инфаркта миокарда.
Б. Внутривенное введение бета-адреноблокаторов, так же как и применение нитратов, способствует купированию болевого синдрома. Ослабляя симпатические влияния на сердце (усиливающиеся в первые 48 ч от начала развития инфаркта миокарда как вследствие самого заболевания, так и в качестве реакции на боль) и снижая потребность миокарда в кислороде, они способствуют уменьшению размеров инфаркта миокарда, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов. Очень важно, что, согласно экспериментальным данным, бета-адреноблокаторы позволяют отсрочить гибель ишемизированных кардиомиоцитов (они увеличивают время, в течение которого эффективна реперфузионная терапия).
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным острым инфарктом миокарда. На догоспитальном этапе показаниями к их внутривенному введению для линейной бригады служат соответствующие нарушения ритма, а для специализированной — упорный болевой синдром, тахикардия, артериальная гипертензия. В первые часы заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 мин под контролем АД и ЭКГ до достижения ЧСС 55-60 в минуту или до достижения общей дозы 0,1 мг на кг массы тела пациента. При брадикардии, признаках сердечной недостаточности, AV-блокаде и снижении САД менее 100 мм рт. ст. пропранолол не назначается, а при развитии указанных изменений на фоне его применения введение препарата прекращается.
Отсутствие осложнений терапии бета-адреноблокаторами на догоспитальном этапе служит показанием для обязательного ее продолжения в условиях стационара с переходом на прием пропранолола внутрь в суточной дозе 40-320 мг в 4 приема (первый прием — спустя 1 ч после внутривенного введения).
В. Внутривенная инфузия магния сульфата проводится у больных с доказанной или вероятной гипомагнезиемией или при синдроме удлиненного QT, а также в случае осложнения инфаркта миокарда некоторыми вариантами аритмий. При отсутствии противопоказаний магния сульфат может служить определенной альтернативой применению нитратов и бета-адреноблокаторов, если их введение по какой-то причине невозможно (из-за противопоказаний или отсутствия препаратов). Согласно результатам ряда исследований, он снижает летальность при остром инфаркте миокарда, а также предотвращает развитие аритмий (в том числе реперфузионных при проведении системного тромболизиса) и постинфарктной сердечной недостаточности.
Этой же цели служит оксигенотерапия, показанная при остром инфаркте миокарда всем больным в связи с частым развитием гипоксемии даже при неосложненном течении заболевания. Ингаляция увлажненным кислородом проводится (если это не причиняет чрезмерных неудобств) с помощью маски или через носовой катетер со скоростью 3-5 л/мин и целесообразна в течение первых 24-48 ч от начала заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
Тактика ведения больного с различными вариантами инфаркта миокарда на догоспитальном этапе представлена на рис. 1 и рис. 2.
Острый инфаркт миокарда является прямым показанием к госпитализации в отделение (блок) интенсивной терапии или кардиореанимации. Транспортировка больного осуществляется на носилках.
А. Л. Верткин, доктор медицинских наук, профессор
В. В. Городецкий, кандидат медицинских наук
О. Б. Талибов, кандидат медицинских наук