субтотальный стеноз что это
Атеросклероз подключичной артерии (окклюзия и стеноз)

Лечение закупорки (окклюзии) подключичной артерии только хирургическое, однако возможен как открытый, так и эндоваскулярный подход. Необходимость лечения определяется развитием хронической недостаточности кровообращения в руке и признаки нарушений мозгового кровообращения.
Причины возникновения и факторы риска
Причины развития атеросклероза подключичной артерии такие же как и других атеросклеротических бляшек. Чаще всего это высокий уровень холестерина, сахарный диабет, ожирение, курение. Поражения чаще всего встречаются в начальном отделе (проксимально) подключичной артерии, однако могут быть и в других сегментах.
Поражение подключичной артерии может быть связано с сдавлением ее между I ребром и ключицей (синдром сдавления на выходе из грудной клетки). Проксимальные поражения подключичной артерии могут протекать скрытно и обнаруживаются при измерении артериального давления на разных руках или пульсации. Однако нередко развиваются осложнения, связанные с кровообращением в руке или головном мозге.
Течение болезни
Атеросклеротическая окклюзия постепенно приводит к усугублению симптомов хронической артериальной недостаточности руки. Наступает постепенная атрофия мышц, возможно развитие нарушений мозгового кровообращения.
В целом окклюзия подключичной артерии мало угрожает продолжительности жизни, однако серьезно влияет на ее качество, поэтому лечение показано при наличии симптомов.
Заболевание можно разделить на несколько стадий:
I (компенсация). Изредка пациент жалуется на повышенную чувствительность к холоду, чувство онемения, слабость при физической нагрузке.
III – (декомпенсация). Постоянная артериальная недостаточность руки. Пациент жалуется на постоянное онемение руки, уменьшение объема плеча и предплечья по сравнению с другой стороной, снижением мышечной силы, невозможностью выполнения пальцами рук тонких движений.
IV – (трофические язвы и гангрена). Появляется синюшность кисти, отечность фаланг, трещины, трофические язвы, некрозы и гангрена пальцев рук.
К счастью, такие крайние проявления встречаются довольно редко.
Осложнения
Иногда могут возникать атероэмболические осложнения. Кусочки атеросклеротической бляшки могут переносится вниз по течению кровотока в руку. Это проявляется резким ухудшением кровообращения в кисти, посинением и болью в пальцах. При несвоевременной помощи может развиться омертвение пальца, что потребует его ампутации.
Прогноз
Без лечения атеросклеротическая окклюзия подключичной артерии приводит к постепенному снижению трудоспособности, увеличивается вероятность ишемического инсульта, гангрены кисти.
После восстановления кровообращения любым методом проблема полностью устраняется. Нормальный кровоток способствует нормальной деятельности руки и исключает синдром обкрадывания головного мозга.
Рецидивы после стентирования подключичной артерии возникают примерно в 10% случаев, за счет развития новых бляшек внутри стента (рестеноз). Если выполнялась операция сонно-подключичного шунтирования, то вероятность рецидива не более 2% случаев.
Поражение коронарного русла и изменения фракции выброса левого желудочка сердца у больных с первичным инфарктом миокарда “без зубца q”
Опубликовано в журнале:
Крылов В.В., Филатов А.А., Лебедева А.Ю., Клыков Л.Л., Гордеев И.Г.
Городская клиническая больница №15 им. О.М. Филатова, 2-е кардиологическое отделение с блоком интенсивной терапии, Москва
Резюме
Проведен анализ результатов коронароангиографии, выполненной 90 больным с острым “не-Q” инфарктом миокарда” в возрасте от 32 до 78 лет – 68 мужчинам и 22 женщинам. Cредний возраст больных – 64,5±2,2 лет.
При проведении эндоваскулярных процедур использовалась транслюминарная ангиопластика и/или стентирование коронарных артерий, баллонные катетеры и стенты B x Sonic корпорации “Johnson and Johnson”. Всем больным проводилась стандартная терапия аспирином, бета-адреноблокаторами, ингибиторами АПФ, антикоагулянтами, клопидогрелем.
Проведено сопоставление характера поражения коронарного русла и изменения ФВ левого желудочка. Наиболее часто у пациентов с инфарктом миокарда “без зубца Q” встречается однососудистое поражение; частота встречаемости двух- и трехсосудистого поражения у этих пациентов приблизительно одинакова. В 8,9% случаев не выявлено гемодинамически значимого поражения коронарного русла.
Ключевые слова: инфаркт миокарда “без зубца Q”, коронароангиография, фракция выброса левого желудочка сердца, стеноз, коронарные артерии, вентрикулография левого желудочка сердца.
В ХХI веке во всем мире, включая Россию, наблюдается тенденция к увеличению числа больных молодого возраста с острым коронарным синдромом, который является одним из вариантов течения ИБС. Из всех больных, перенесших инфаркт миокарда, более 10% составляют лица молодого возраста и, в основном, мужчины. Нестабильная стенокардия и инфаркт миокарда “без зубца Q” составляет 54,3 на 100000 человек [5].
Несмотря на большое количество работ, посвященных инфаркту миокарда, ангиографическая картина инфаркта миокарда “без зубца Q” на ЭКГ, встречается в научных трудах крайне редко [4], поэтому актуальность данной темы не вызывает сомнения.
В настоящее время у врачей – кардиологов отсутствует единое мнение не только о роли эндоваскулярных методов лечения, но и о целесообразности раннего ангиографического обследования этой категории пациентов. Преимущество проведения коронароангиографии и проведения по показаниям эндоваскулярного лечения инфаркт – зависимой артерии в острый период ИМ без подъема сегмента ST и у больных с ранней постинфарктной стенокардией очевидно. В этих случаях выполнение КАГ рекомендуется через 6 месяцев после ИМ. Интенсивное развитие эндоваскулярных технологий и появление стентов с лекарственным покрытием существенно расширили возможности и показания к раннему эндоваскулярному лечению у больных, перенесших инфаркт миокарда без зубца Q на ЭКГ [1–4, 6].
Актуальным и недостаточно освященным в современной научной литературе является вопрос, каким образом выполненное в госпитальном периоде эндоваскулярное лечение влияет на частоту рецидивов стенокардии, частоту повторного инфаркта миокарда, динамику фракции выброса левого желудочка сердца, на показатель выживаемости в отдаленные сроки после вмешательства у этих пациентов [4].
Пациенты с перенесенным инфарктом миокарда “без зубца Q” остаются одной из наиболее сложных категорий для инвазивного лечения, что требует систематизации накопленного опыта и выработки алгоритма ведения таких больных. С одной стороны, перенесенный “не-Q инфаркт миокарда”, как правило, свидетельствует о наличии атеросклеротического коронарного поражения коронарных артерий, с другой стороны, наличие сохранного миокарда требует определения оптимальной тактики для предотвращения повторных инфарктов и улучшения отдаленного прогноза. Отсутствие зубца Q на ЭКГ после перенесенного острого коронарного синдрома свидетельствует об отсутствии трансмуральных изменений миокарда [4,6, 9,10,11]. Тем не менее, отдаленный прогноз пациентов с перенесенным инфарктом миокарда “без зубца Q” остается неудовлетворительным и связан с повышенным риском повторных коронарных осложнений [4]. У больных с достигнутой реперфузией остается морфологический субстрат поражения (стенозирующая атеросклеротическая бляшка) и жизнеспособный миокард в бассейне кровоснабжения инфаркт-связанной артерии. Как правило, наличие гемодинамического поражения в коронарном сосуде и сохранный миокард в бассейне его кровоснабжения – причина сохранения постинфарктной стенокардии. Инфаркт миокарда “без зубца Q” не настолько обширен и не столь часто вызывает летальный исход в раннем постинфарктном периоде, по сравнению с инфарктом миокарда “с зубцом Q”, но он чаще вызывает нестабильность миокарда, что ведет к повышению частоты повторных инфарктов и рекуррентной стенокардии [4, 9].
Материал и методы
В исследование были включены 90 больных острым “Q-необразующим” инфарктом миокарда в возрасте от 32 до 78 лет – 68 мужчин, 22 женщины. Cредний возраст больных составил 64,5±2,2 лет.
Анамнез ИБС в среднем составил от 0 до 8 лет. При поступлении оценивались клинические и биохимические показатели крови (креатинфосфокиназа и ее изоферменты, тропонин Т), динамика на ЭКГ. В течение 2-х – 30 дней после госпитализации всем больным была проведена коронароангиография. При рецидиве болевого синдрома проведение коронароангиографии осуществляли в течение суток. Все пациенты получали стандартную терапию: дезагреганты, антикоагулянты, бета-блокаторы, антагонисты Са, ингибиторы АПФ, нитраты, клопидогрель.
По критериям ВОЗ, при постановке диагноза острого инфаркта миокарда использовали наличие двух из трех следующих признаков: характерная клиническая картина боли за грудиной, динамика на серии ЭКГ и повышение – с последующим снижением – кардиальных ферментов в плазме (креатинфосфокиназа и ее изоферменты, тропонин Т).
Больных разделили на группы по срокам проведения эндоваскулярных процедур и характера поражения коронарного русла.
Коронароангиография и левая вентрикулография
Селективная коронароангиография и левая вентрикулография выполнялась всем больным в течение госпитализации по методике Judkiens (1967) на аппарате “Bicor-TOP” фирмы Siemens. Профилактика возможных осложнений достигалась следующими обязательными мероприятиями:
Исследование проводилось в присутствии врачей – анестезиолога, реаниматолога и кардиолога.
Введение катетера осуществлялось путем чрескожной пункции бедренной артерии по модифицированной методике Сельдингера. Пункция бедренной артерии осуществлялась в асептических условиях под местной анестезией 0,5% раствором новокаина, односекционной остроконечной иглой размером 18 inch под углом 45є к длинной оси сосуда. Чаще всего проводили пункцию правой бедренной артерии. Использовались интрадьюсеры размером 6 – 7 F.
Для проведения селективной коронароангиографии использовались катетеры Джадкинса. В качестве контрастного вещества использовался 76% урографин (Shering) или Омнипак 350 мг/мл (Nykomed).
Оценка степени восстановления коронарного кровотока по данным коронарографии, предложенная в исследовании TIMI (Thrombolysis in Myocardial Infarction)
| Степень | Данные коронарографии |
|---|---|
| 0 | Отсутствие кровотока: контрастное вещество не проходит ниже места окклюзии |
| 1-я | Минимальный кровоток: контрастное вещество просачивается ниже места окклюзии коронарного сосуда, но не заполняет сосудистое русло |
| 2-я | Частичный кровоток: контрастное вещество проходит через место окклюзии и заполняет сосудистое русло, однако это происходит медленнее, чем в нормальных сосудах |
| 3-я | Полное восстановление кровотока: контрастное вещество заполняет сосуд ниже места закупорки так же быстро, как это происходит выше места окклюзии; контрастное вещество быстро покидает сосуд |
При анализе стенотического поражения коронарных артерий использовалась классификацию Петросяна Ю.С. – Зингермана Л.С. (1973г).
Анализ сократимости левого желудочка проводился автоматически при помощи системы HICOR. Оценивался конечный диастолический, конечный систолический объемы, рассчитывалась фракция выброса.
Результаты и обсуждение
В табл.1 приведены половозрастные характеристики групп больных. Средний возраст больных в первой группе составил 53,7±4,6 лет, во второй – 58,7±6,3 лет, в третьей – 62,4±5,4 лет, в четвертой – 59,5±4,7.
Группы были сопоставимы по возрасту (для критерия Крускалла-Уоллиса р>0,05) и полу (для критерия χ 2 р>0,05 при парном сравнении групп).
Передний инфаркт наблюдался у 57 больных (63,3%), нижний – у 22 (24,4%), нижний боковой – у 11 (12,2%). Полученные данные согласуются с данными литературы о локализации “не Q” – инфаркта миокарда [4,8,11,14]. Статистически значимые различия групп по локализации поражения отсутствовали (для критерия χ 2 р>0,05 при парном сравнении групп).
Таблица 1
Характеристика групп больных по возрасту и полу
| Показатель | Группа 1 (n-25) | Группа 2 (n-38) | Группа 3(n-19) | Группа 4 (n-8) | ||||
|---|---|---|---|---|---|---|---|---|
| Пол | 19 мужчин | 6 женщин | 27 мужчин | 11 женщин | 16 мужчин | 3 Женщины | 4 мужчин | 2 женщины |
| Возраст, лет | 53,7 | 58,7 | 62,4 | 59,5 | ||||
| Отклонение | 53,7±4,6 | 58,7±6,3 | 62,4±5,4 | 59,5±4,7 | ||||
Табл.2 иллюстрирует локализацию инфаркта миокарда в различных группах лечения: в первой группе больных преобладал передний инфаркт. Он был отмечен у 56% больных. Нижний инфаркт выявлен у 32%, нижний боковой – у 12% больных. Сопоставимые данные получены для второй, третьей и четвертой групп. Во всех группах больных преобладал передний инфаркт миокарда.
Таблица 2
Локализация инфаркта миокарда в группах больных
| Группа 1(n-25) | Группа 2(n-38) | Группа 3(n-19) | Группа 4 (n-8) | |||||
|---|---|---|---|---|---|---|---|---|
| Локализация инфаркта микарда | Число случаев | % | Число случаев | % | Число случаев | % | Число случаев | % |
| Нижний | 8 | 32,0% | 10 | 26,3% | 2 | 10,5% | 2 | 25,0% |
| Передний | 14 | 56,0% | 24 | 63,2% | 15 | 78,9% | 4 | 50,0% |
| Нижний боковой | 3 | 12,0% | 4 | 10,5% | 2 | 10,6% | 2 | 25,0% |
| Всего | 25 | 100% | 38 | 100% | 19 | 100% | 8 | 100% |
Табл. 3 свидетельствует о том, что по частоте поражения различных коронарных артерий у обследованных больных сохраняются те же закономерности, что и в целом по ИБС: в преобладающем большинстве случае сосудистая катастрофа происходила в передней межжелудочковой (54,9%) и правой коронарной (19,9%) артериях; в огибающей артерии – в 8,5% случаев, в общем стволе левой коронарной артерии – также в 8,5% случаев. Поражение ветвей второго порядка мы наблюдали относительно редко: ветвь тупого края – 4,9% случаев, диагональная ветвь – 3,7% случаев.
Таблица 3
Инфаркт-зависимые артерии в группах больных
Таблица 4
Локализация поражения в инфаркт-зависимой артерии
| Группа 1 (n=25) | Группа 2 (n=38) | Сумма | ||||
|---|---|---|---|---|---|---|
| Локализация в артерии | Число случаев | % | Число случаев | % | Число случаев | % |
| Проксимальное | 11 | 44,0% | 17 | 44,7% | 28 | 44,4% |
| Среднее | 13 | 52,0% | 20 | 52,6% | 33 | 52,4% |
| Дистальное | 1 | 4,0% | 1 | 2,6% | 2 | 3,2% |
В четвертой группе больных после проведения коронароангиографии не выявлено гемодинамически значимого поражения инфаркт-зависимой артерии. В этой группе инфаркт-зависимые артерии распределились следующим образом: передняя межжелудочковая артерия – 50,0% случаев, огибающая артерия – 12,5% случаев, правая коронарная артерия – 37,5% случаев. Следует отметить, что в 91,4% случаев поражены магистральные артерии и только в 8,6% случаев локализация поражения – ветви второго порядка.
Преобладающее поражение инфаркт-зависимых артерий у больных 1-й группы – в проксимальной и средней частях с высокой степенью стеноза (≥90%).
Среднее количество пораженных артерий у больных 1-й группы составило 1,12±0,25. Сочетанное поражение коронарных артерий отмечалось у 3-х (12%) пациентов: в 2-х случаях это было сочетание передней межжелудочковой и правой коронарной артерии, в одном случае – правой коронарной и огибающей артерий.
В первые сутки инфаркта миокарда “без зубца Q” было проведено 9 (36,0%) эндоваскулярных процедур, во вторые сутки – 16 (64,0%).
Наиболее часто в первой группе пациентов (48%) встречалось изолированное поражение передней межжелудочковой артерии. Особо следует отметить, что при оценке кровотока по TIMI, у 8 (32%) больных определяется снижение кровотока, наличие спазма инфаркт – зависимой артерии, который купируется после введения внутрикоронарно 0,1% спиртового раствора нитроглицерина – 11 (44%) больных.
Характер поражения инфаркт – зависимой артерии у пациентов в 2-й группы отличался практически равным поражением как проксимального отдела артерии, так и среднего ее отдела (44,7% и 52,4% соответственно). Частота встречаемости стенозов – более 75% и более 90% – была примерно одинаковая.
Среднее количество пораженных артерий составило 1,57±0,27. Во второй группе пациентов большее разнообразие видов сочетанного поражения инфаркт – зависимых артерий по сравнению с больными первой группы. Во второй группе сочетанное поражение артерий отмечалось у 21 больного (55,3% против 12% в первой группе). В 4-х случаях, это было сочетание передней межжелудочковой артерии и правой коронарной артерии. В 5-ти случаях – передней межжелудочковой артерии и огибающей артерии. В 2-х случаях – передней межжелудочковой артерии, огибающей артерии и правой коронарной артерии. В 3-х случаях – передней межжелудочковой артерии и диагональной ветви ПМЖВ. В одном случае сочетание поражения ствола левой коронарной артерии, передней межжелудочковой ветви и огибающей артерии. В 2х случаях – сочетание поражения огибающей артерии и ветви тупого края. В 4-х случаях – сочетание поражения правой коронарной артерии и огибающей артерии. Во второй группе больных чаще встречается сочетанное поражение коронарных артерий (для критерия χ 2 р=0,012, p 2 р=0,033, p 2 р=0,026, p 2 p=0,044, р 2 p=0,026, р 2 p=0,006, р 2 p=0,038, p 0,05).
Согласно данным таблицы 8, фракция выброса левого желудочка сердца не зависит от количества пораженных артерий (для критерия Спирмена r=0,00014, р>0,05).
Таблица 8
Показатели фракции выброса левого желудочка сердца и число пораженных артерий
| Показатель | Однососудистое поражение | Двухсосудистое поражение | Трехсосудистое поражение |
|---|---|---|---|
| Средний возраст больных | 55,78 | 58,23 | 62,36 |
| Фракция выброса левого желудочка сердца | 58,44% | 57,18% | 56,34% |
Мы также рассмотрели влияние на изменение ФВ ЛЖ степени обструкции инфаркт-зависимой артерии (табл.9). Статистически подтвердить наличие коррелятивной связи не удалось (для критерия Спирмена r=0,024, р>0,05). Оказалось, что у больных со стенозом II степени и субтотальным стенозом, показатели ФВ ЛЖ статистически не различаются (для критерия Крускалла-Уоллиса p=0,446, p>0,05).
Таблица 9
Фракции выброса левого желудочка сердца в зависимости от степени обструкции инфаркт – зависимой артерии
| Показатель | Стеноз 2-й степени | Субокклюзия | Окклюзия | Без поражения |
|---|---|---|---|---|
| Фракция выброса левого желудочка сердца | 55,83% | 54,84% | 52,80% | 58,24% |
В то же время, наличие развитого коллатерального кровотока благотворно влияет на сократительную функцию миокарда, о чем свидетельствуют более высокие в данном случае значения ФВ ЛЖ, что отражается в более высоком значении последнего у больных второй группы, в которой коллатеральный кровоток более развит (табл.10).
Таблица 10
Изменения фракции выброса левого желудочка сердца в зависимости от наличия коллатералей
| Показатель | С коллатералями | Без коллатералей |
|---|---|---|
| Фракция выброса левого желудочка сердца | 57,30% | 52,10% |
Выводы
Литература
Abstract
Coronary angiography was performed in 90 patients with acute non-Q wave myocardial infarction (non-Q MI) – 68 men and 22 women aged 32–78 years (mean age 64,5±2,2 years).
Endovascular intervention included transluminal angioplasty and/or coronary artery stenting, with balloon catheters and B x Sonic stents (Johnson and Johnson Corp.). All patients received standard therapy of aspirin, beta-blockers, ACE inhibitors, anticoagulants, and clopidogrel.
For patients with non-Q MI, one-vessel coronary artery pathology was most typical; two- and three-vessel pathology prevalence was similar. In 8,9% of the cases, no hemodynamically significant coronary artery pathology was observed.
Keywords: Non-Q myocardial infarction, coronary angiography, left ventricular ejection fraction, stenosis, coronary arteries, left ventricular ventriculography.
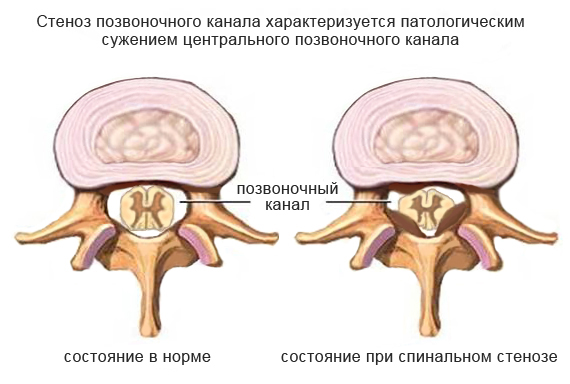
Поясничный стеноз
Наши специалисты свяжутся с вами в ближайшее время
Поясничный спинальный стеноз является хроническим патологическим состоянием, при котором суженный спинномозговой канал оказывает давление на структуры, находящиеся внутри него. Патология прогрессирует медленно, без лечения улучшений быть не может. С течением времени и усугублением ситуации пациентам требуется оперативное вмешательство. В основном от стеноза страдают возрастные пациенты, наиболее частая его локализация – поясница. Без лечения стеноз неуклонно развивается, в результате приводя к потере трудоспособности.
Виды стеноза
Классификация основывается на характере нарушения, расположения и степени выраженности:
Почему возникает
Возникновение стеноза позвоночника может быть обусловлено как врожденными особенностями, так и приобретенными. Врожденный стеноз появляется вследствие утолщения или уменьшения длины позвоночной дуги, укорочения тела позвоночника или ножки. Такие изменения возникают редко, гораздо чаще пациенты сталкиваются с приобретенным стенозом спинномозгового канала. Причины появления приобретенного стеноза следующие:
Проявления патологии
Спинальный стеноз поясничного отдела имеет целый ряд характерных признаков, среди них:
Есть несколько признаков, определяющих последнюю стадию стеноза:
Постановка диагноза
Диагноз ставится после опроса, осмотра и обследования. В качестве дополнительных методов диагностики используются:
Лечение стеноза без операции
Если неврологические изменения не отмечаются, заболевания можно ле6чить консервативными методами без оперативного вмешательства. Когда пациент жалуется только на боли и его обращение к врачу оказалось своевременным, могут применяться следующие методики:
При комплексном подходе и грамотном комбинировании методик достигается требуемый результат. Выбор методов проводится строго индивидуально с рассмотрением особенностей пациента, противопоказаний и других факторов.
Операция для коррекции сужения
Операция необходима для прекращения сдавливания нервных корешков и возобновления нормального функционирования тканей. Проводиться могут как закрытые, или эндоскопические, так и полномасштабные открытые вмешательства. Чаще используются методики:
Возможные последствия спинального стеноза
При несвоевременном или полностью отсутствующем лечении патология может давать серьезные осложнения:
Профилактические меры
Некоторые простые действия помогут предупредить развитие спинального стеноза поясничного отдела или быстро избавиться от проблемы, если она уже возникла:
Стеноз снижает качество жизни пациента и неизбежно приносит дискомфорт. Если к врачу обратиться вовремя, когда патология не переросла в серьезную стадию, ее можно устранить консервативными методами, без операции. Оперативное вмешательство требуется тогда, когда ситуация запущена, стеноз прогрессирует и выводит из строя весь организм.
Пациенты, перенесшие операцию, отмечают, что своевременное обращение за квалифицированной помощью могло существенно упростить ситуацию. Для полного выздоровления важно соблюдать здоровый образ жизни и вовремя обращаться к врачу.